LF対談
細胞内輸送を担うモーター分子は、
細胞にとって基本的な要素なのだと考えています No.73(2014.10)

東京大学大学院医学系研究科 分子構造・動態学講座 特任教授
廣川信隆 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
生体を一瞬で凍結させて“瞬間”の状況を捉える
岸本 廣川先生は、まず医師として脳神経外科の道を歩まれたのですよね。
廣川 はい。東大医学部の学生だったとき、ヒトの体のしくみはまだわからないことだらけだと知り、研究したいと考えていました。でも、医学部は卒業まで6年かかる上、大学紛争で卒業が1年遅れることになったため、理学部の卒業者たちが研究をどんどん進めているのをまだ学生として横目で見ているような状況でした。それで、私は臨床と並行して病気の研究をやろうと考え、興味のあった脳神経外科に研修医として入ったのです。
ところが、脳神経外科に入ってみると患者さんをずっと診るため病院に泊まり込みの日々が続きました。そこで、1年が経つところで、基礎的な研究に集中しようと決断をしたんです。
岸本 私も医学部にいました。だから遺伝子の実験をしたのは30歳を過ぎてから。でも、医学部だったから病気のことは知っている。それを生かさねばと思いました。
廣川 同じ思いがあります。複雑で多様な生体のしくみが統合されて、われわれは生きている。その全体像を医学部の教育は教えてくれたと思うんですね。振り返ると、医学部で学んだ基礎が生きていると思います。
岸本 先生はその後、先生の代表的な成果の一つである「急速凍結法」による生体の観察法を開発されましたね。『Cell』『Nature』『Science』といった雑誌の数々の表紙も飾っていて、とても印象的です。それまでの観察法とどう違うんですか。
廣川 従来の光学顕微鏡や電子顕微鏡では、生体をホルマリンなどの化学薬品で変性させて固定させていたんです。でも、固定させるのにどれだけ時間がかかっているか分からない。そのようにして見た像が、生体の瞬間の状況を反映しているのかというと疑問でした。
私は助手時代、中井準之助先生の解剖学教室で、βバンガロトキシンというヘビ毒を利用してニューロンを壊して、感覚細胞の分化がどうなるかを見ようとしていたんです。この毒が神経伝達物質の放出を抑えていることがわかってきたため、そのダイナミックな過程を見たいと思いました。生体の現象を瞬時にストップさせて、コマ撮りのようにして観察することで、生体が動く過程を忠実に知りたいと考えたのです。
細胞の構造を破壊しないで細胞を凍結させるには、1秒間で1万℃という急激な温度低下が必要なのです。それを実現するため、熱伝導性のよい金属のブロックを液体ヘリウムや液体窒素で冷却すると、−100℃以下になったところで熱伝導率が10倍に跳ね上がるんです。金属材料としては99.999%の純銅が最適でしたが、市販していないので中井先生に相談して、東大の金属工学の教授に分けていただき、急速凍結できる装置を作ったんです。
岸本 それで、細胞がきれいなままで瞬間的に固まるんですね。鉄板がぬるいままより、熱くしておいて肉を一気に焼くほうが美味いのと似ていますね。
廣川 そうです、そうなんです。
再び東京大学へ ニューロン研究を深化
岸本 急速凍結法を携えて、先生はアメリカに行かれたのですね。
廣川 ええ。1979年のことでした。自分で立ち上げた方法論を生かせる研究をしたいと考えていたところ、NIH(国立衛生研究所)のトム・リース教授のグループが唯一、同様の方法で研究していたんです。「日本にも同じようなことをやっているヤツがいたとは」と受け入れられ、意気投合しました。リース教授のグループのポスドクだったジョン・ホイザー博士が独立して、カリフォルニア州立大学サンフランシスコ校に研究室をもつことになったので、私もそこの所属となりました。その後、ホイザー博士とともにワシントン大学に移りました。
留学時代、急速凍結法を用いた電子顕微鏡観察にはもう一つ、利点があるということに気づいたんです。それは、立体的かつ高分解能に細胞内・外の構造を見ることができるということです。この利点を生かした研究を発展させようと考えました。
岸本 留学されていた頃、アメリカと日本では、まだ研究面に格差があると先生も思っていらっしゃったでしょう。でも、先生は日本に戻ってこられた。どうしてですか。
廣川 たしかに研究環境はよかったですし、ワシントン大学では独立して、准教授の職を提供されていたんです。私自身、「ここで研究をがんがんやろう」と思っていました。
その直後に東大から「戻ってこないか」と打診されました。とても悩みましたね。それで、アメリカと日本で研究されたご経験のある方に相談したんです。「アメリカにいれば何回も『日本に戻ってこないか』と言われるだろう。でも、この若いうちに日本に帰って、あなたのシューレ(学舎)を開きなさい。日本人の弟子を育てながら研究を発展すべきだ」と言われました。この言葉が、とても重かったんですね。
岸本 そうですか。それで東大に戻られて、いよいよ先生は、急速凍結法も使って、細胞内の分子が輸送されるメカニズムの研究に着手されたんですね。
廣川 そうです。
岸本 細胞の中でもニューロンをご研究対象にされたと聞きます。ニューロンには1mに達するものもあるけれど、軸索の端のシナプスで放出に必要な物質は、ニューロンの中心の細胞体でしかつくられないから、それがどう輸送されるかを観察するにはそのような長い細胞が都合よいわけですね。
廣川 その通りです。それに、脳神経系は自分の研究のルーツでもあります。
東大に戻ると、まず、微小管とタウタンパク質などの微小管関連タンパク質が結合して細胞骨格を形成するメカニズムに興味をもちました。並行して、それらの物質の生体内での働きを知るため、ノックアウトマウス法も導入して方法論を立ち上げました。
それらと同時に、やはり1mもある軸索の中で、タンパク質がどう輸送されるかは知りたくなりましたね。私は電子顕微鏡のなかで見た細胞の微小管と膜小器官の間にある足のような構造ががカギを握っていると直観しました。それで、生化学や分子生物学を導入して、モーター分子の研究に発展していったんです。

廣川信隆 氏
東京大学大学院医学系研究科 分子構造・動態学講座 特任教授
1946年、神奈川県生まれ。71年東京大学医学部卒業。72年〜79年同大学医学部助手。79年カリフォルニア大学医学部研究員。80年ワシントン大学医学部研究員、82年同助教授、83年同准教授。83年東京大学医学部教授、2003年〜07年同大学大学院医学系研究科長・医学部長、10年研究科特任教授。専門分野は、分子細胞生物学。細胞骨格の分子細胞生物学および分子遺伝学的研究、また、細胞内物質輸送および細胞の形作りの機構の研究などを行う。細胞構造を非破壊的に観察するための「急速凍結法」を開発。この手法を用いるなどして、ニューロン内のモーター分子の働きを解明し、モーター分子群をキネシンスーパーファミリータンパク質(KIFs)と命名。KIFのすべて45種類を発見し、各機能や動態のメカニズムを解明してきた。受賞は、日本電子顕微鏡学会瀬藤賞、塚原仲晃賞、日本医師会医学賞、上原賞、朝日賞、武田医学賞、日本学士院賞、藤原賞、文化功労者。ヨーロッパ分子生物学機構外国人会員、AAAS(American Association for the Advancement of Science) Fellow、日本学士院会員を歴任。
モーター分子群「KIFs」の多様で精緻な働きを解明
岸本 そのモーター分子の一群が、キネシンスーパーファミリータンパク質(KIFs)と呼ばれているものですね。それを先生は何十種類も見つけられたわけでしょ。
廣川 ええ、ヒトやマウスでは合計45個のKIF遺伝子があります。どの細胞にも普遍的に存在するもの、特定の細胞に多くあるもの、時間的に偏在するものなど、種類によって異なるものの、KIFsはニューロンだけでなくすべての細胞にあります。細胞にとって基本的な要素なのだと考えています。
岸本 実際、KIFsはどのようにタンパク質を輸送しているんですか。
廣川 私たち人が歩くように、モーター分子が“2本足”で交互にステップして微小管のレールの上を進んでいくものもあります。でも、興味深いことに“1本足”で進むモーター分子もあったんです。例えば、シナプス小胞を輸送するKIF1Aという種類は、いちばん輸送スピードが速いのですが、1本足です。1本足では微小管のレールから外れたりして進めないだろうと考えられていたのですが、じつは進めることがわかりました。
岸本 それに、KIFsは自分が輸送する荷物をどうやって見つけるのですか。もし宅配便で、荷物まちがいがあったら大変です。
廣川 そうですよね。モーター分子のモータードメインとよばれる領域が微小管のレールにくっつくのですが、尻尾のような領域は、アダプタータンパク質または足場タンパク質がくっついていて、それらが特定の荷物を認識して結合する、というのが多く見られるメカニズムです。
岸本 輸送するにあたっては、行き先も間違えないようにしないとなりませんね。
廣川 ええ。細胞体から樹状突起のほうへ向かうのと、軸索のほうへ向かうのとは、どうやって決まるのか。これにはいくつかメカニズムがあるのですが、一つは微小管のレールのちがいによるものです。軸索へと向かう微小管には、微小管を形成するβチューブリンのうちGTP(グアノシン三リン酸)型が多くあります。一方、樹状突起のほうは同じβチューブリンでもGDP(グアノシン二リン酸)型が多いんです。それで、KIFsはどちらが多いかを認識して、その方向に向かうんです。例えば、KIF5というモーター分子は、そのモーター領域自身はGTP型のβチューブリンと親和性が高いので、GTP型の多い軸索の微小管のほうへと向かうんです。
もう一つ、輸送する荷物によっても向かう方向が決まるという機構もあります。でも、どのように規定しているのかまだ謎も多く、これは今後、深く解明していかなければなりません。
岸本 そうしたら、荷物の積み下ろすときはどうやって……。
廣川 これにも巧妙な機構があって、大きく二つの方法があります。
一つはモーター分子あるいは荷物のタンパク質のリン酸化によって荷物が外れるんです。例えば、カルシウム濃度の上昇といった外からのシグナルによって、モーター分子の尻尾がリン酸化して荷物が外れます。
それからもう一つ、荷物に含まれるスモールGプロティンのGTPが加水分解してGDPになることで外れることもあります。
岸本 先生が発見された45種類は、それぞれにいろいろな特徴もあるようですね。例えば、多くあると“頭がよくなる”種類もあると聞きました。
廣川 ええ、KIF17のことですね。記憶や学習に関わるグルタミン酸などの神経伝達物質のNMDA型受容体を輸送する役割をもっています。受容体を輸送するのですから、軸索でなく、神経伝達物質を受ける側の樹状突起のほうへと向かっていきます。KIF17を多く発現するマウスは、記憶・学習能力に優れています。これはシナプス伝達が活性化され、KIF17とNMDA型受容体が転写・蛋白合成ともに亢進する為です。
岸本 KIFsの中で、病気との関連性も、なにかわかっているのですか。
廣川 ええ、わかっています。典型的な例として、KIF1Bβというモーター分子があります。KIF1Bβの遺伝子をノックアウトさせたマウスをつくると、生後すぐ死んでしまいます。呼吸ができないんですね。肺は正常なのですが、肺呼吸を司る中枢神経系の数が通常の25%しかないんです。それで死んでしまう。
では、KIF1Bβの遺伝子をヘテロにしたマウスはというと、生き残ります。ですが生後1年もすると、歩行障害や筋力低下などの症状が現れてきます。この症状は、ヒトの神経変性疾患にとてもよく似ているんですね。それで、詳しく調べてみると、筋萎縮の症状があるシャルコー・マリー・トゥース病2A型というヒトの神経変性疾患との関連性がわかってきました。この病気をもった家系を調べたところ、欠損している遺伝子の場所が、KIF1Bβの遺伝子の場所と一致していたんです。この家系の異常はモーター領域にあり、KIF1Bβモーターが動けない事による事が分かりました。さらにKIF1Bβの遺伝子異常については、アメリカの臨床医と共同研究が進んでおり、荷物のタンパク質が結合するモーター分子の尻尾に障害が起きて、うまく輸送できない異常もあることがわかってきています。
岸本 そうですか。
廣川 腫瘍との関係についても研究を進めています。
KIF3というモーター分子には、荷物とくっつくアダプタータンパク質がありますが、その遺伝子をマウスの脳に限定して発現しないように欠損させると、このノックアウトマウスは脳腫瘍で死んでしまいます。
どうして脳腫瘍ができるのか調べたところ、KIF3で輸送されるはずのβカテニンという物質が輸送されなくなることがわかりました。するとβカテニンがどんどん細胞核に貯まっていってしまうんですね。そして、転写因子として細胞を増殖させる遺伝子群に異常に働いて腫瘍が生じてしまうんです。脳で実験したので脳腫瘍になりましたが、例えば肝臓で実験すれば肝癌になるでしょう。
岸本 そのKIF3というのは、他にも興味深い特徴があるみたいですね。体の左右を決定するのに関係しているとか……。
廣川 ああ、そうです。私たち自身も発見したときはすごく驚きましたが、体にある左右非対称な構造を、このKIF3が決めていたことがわかったんです。
KIF3は体のほとんどの細胞で発現しているモーター分子です。この遺伝子をノックアウトさせたマウスは、生まれる前に死んでしまうんですね。それで、死んだ胎児マウスを調べてみると、半分の個体では、心臓が右側にあったんです。つまり、全体では、体の左右決定がランダムになっていたわけです。
どうしてKIF3がないと、体の左右の決定がランダムになってしまうのか。そのときすでに、胎児初期のお腹にノード(結節)という三角形の凹みがあって、左右を決定する遺伝子を左側だけに発現することがわかっていました。しかし、その上流にどんな現象があるのかはわかっていませんでした。
それで、ノードを見たところ、野生型のノードには繊毛という毛のような突起が出ています。ところが、KIF3の遺伝子を欠損させたマウスには、その繊毛が見られません。違いは見つけましたが、まだ、その違いが、左右決定のメカニズムとどう関係するのかは謎でした。
さらに調べてみてわかったのは、この繊毛の材料となる荷物を、繊毛内でKIF3が運んでいたということです。だから、もしKIF3がなくなると、繊毛の材料が運ばれないことになります。
岸本 つまり、繊毛ができないわけですね。
廣川 はい。では、繊毛はなにをやっているのか。胎児マウスのノードから出ている繊毛をビデオ顕微鏡で観察すると、驚いたことに、繊毛が回転運動をしていました。繊毛は100本ほどあってみんな回っているので、そこに貯まっている胎児外液に蛍光のビーズを入れてみました。すると、野生型ではビーズがすべて右から左へと流れていきます。つまり野生型では胎児外液の左向きの流れがある。でも、繊毛のない胎児マウスでは回転運動が起きないので、ブラウン運動の影響を受けるのみ。
岸本 つまり、繊毛がないと左向きの流れが出来ないので、左右決定が出来ないのですね。
廣川 そのとおり、ランダムなんです。KIF3が必要な荷物を運ばず繊毛がつくられないことが、左右決定をランダムにさせることのメカニズムであるとわかったのです。KIF3が働いて繊毛がつくられれば、体の左右は必然的に決定します。
研究の対象と病気がつながってきた
岸本 これだけKIFsに種類があって、それぞれ特徴もあれば発見もある。となると、先生はまだまだすべきことがたくさんありますね。最近は、どのようなことに取り組んでおられるのですか。
廣川 KIF19Aというモーター分子に着目しています。いま、繊毛の話しをしましたが、このKIF19Aは繊毛の頂端まで来ると、微小管を脱重合する、つまり繊毛をそれ以上は伸びなくさせます。ということは、KIF19Aの遺伝子を欠損させると、繊毛が2倍にも3倍にも長くなります。すると、体液の流れをうまく統合できなくなり、結局、脳髄液の流れができずに水頭症になってしまうんですね。
この他にも、KIF5Aと癲癇、KIF13Aと不安神経症、KIF12と糖尿病等、KIFsと病気の関連が明らかになってきています。私自身は、冒頭のお話のように医学部に入って、その後、好奇心のままに研究をここまで続けてきました。でも当然、病気の治療などと関係が見えてくればいいなと思っています。
岸本 世界的に見ると、KIFsの研究状況はいかがですか。
廣川 多くの研究室はありますが、私たちのように分子生物学、分子遺伝学、構造生物学などを総合的に行えるところは見当たりません。
現在は、構造、物質、機能及び、遺伝子、分子、細胞、組織、個体、行動などがつながってきましたので、研究がものすごくおもしろい状況になってきました。
岸本 やることは尽きそうもないですね。これからもご活躍を期待しています。ありがとうございました。
EYES
細胞内輸送を担うモーター分子群
「キネシンスーパーファミリータンパク質」を解明
ダイナミックに変化する細胞内の動態を、
独自開発の「急速凍結法」を駆使して詳しく、そして美しく、観察する
人間が橋や港などを建設しようとするときは、物資を載せて現場まで輸送する必要があります。実は、細胞の中にも、これと同様に、必要な物質を必要な場所まで輸送する極めて精緻なメカニズムがあるのです。
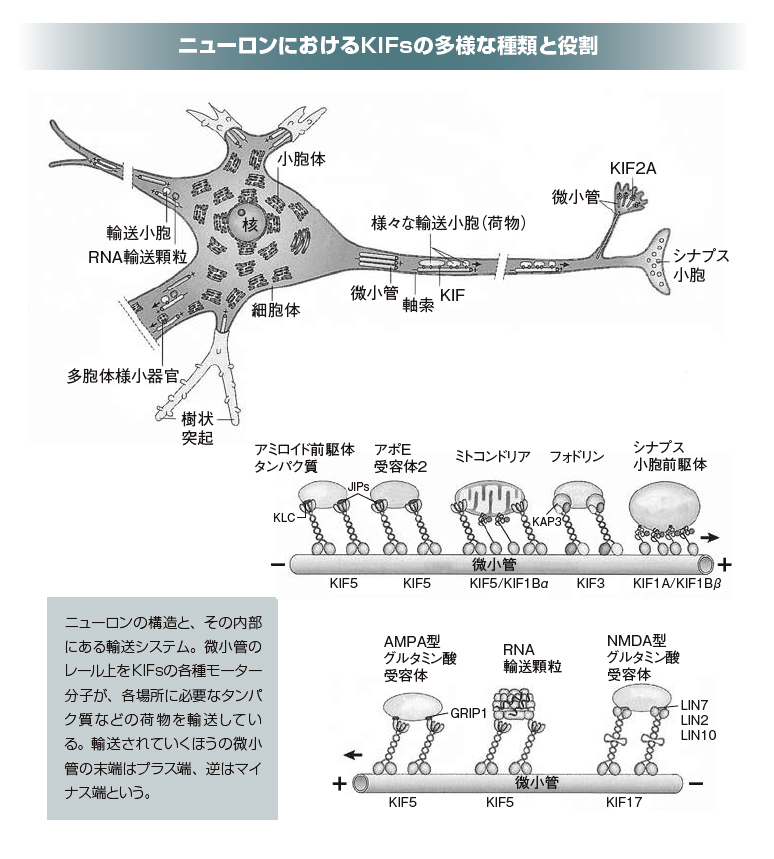
この細胞内輸送システムを、ニューロン(神経細胞)を舞台に見てみます。
ニューロンは刺激を受容・伝達するための細胞であり、三つの要素、つまり、刺激を受け取る何本もの樹状突起、刺激を隣のニューロンに伝達する1本の軸索、それに核のある細胞体で構成されています。伸びた軸索の先端にあるシナプスから、神経伝達物質が隣のニューロンの樹状突起に放出されると、刺激が伝わります。
ヒトの坐骨神経などのニューロンは、長さ1mに達するものもありますが、その長さまで伸びるには材料が必要です。また、伸びた軸索の先端にシナプスが存在するのにも材料が必要です。それらの材料はどこでつくられるのかというと、ニューロンの中心の細胞体です。細胞体で合成されたタンパク質などの材料がニューロン内で輸送されることで、樹状突起や軸索がつくられたり、働いたりするようになっているのです。
では、細胞内の輸送システムとはどのようなものでしょう。そのシステムも、人間がモノを運ぶ営みと極めてよく似ています。荷物にあたるものはタンパク質複合体や膜小器官など多彩です。荷物の運搬役にあたるものは「モーター分子」とも呼ばれるキネシンなどのタンパク質。荷台にあたるものはアダプタータンパク質や足場タンパク質。そして、輸送のための経路にあたるものは「微小管」という中空の管などが該当します。
これらの各要素によって細胞内の輸送システムが成り立っています。もし、運搬役のモーター分子が人間ほどの大きさだとすると、モーター分子が直径5mの土管の上を、10t程の荷物を担いで秒速100m以上で走っていることになります。
今回の対談に登場する廣川信隆氏は、ニューロンを対象に、こうした細胞内の輸送システムを解明してきました。
まず、東京大学での助手時代、細胞内部の動態を精緻に観察するための手法として、独自に「急速凍結法」を開発しました。この方法では、1秒間に1万℃以上という急激な温度低下で、細胞を凍結させることができます。動いていた細胞が一瞬にして止まるため、細胞内の動的な変化の“断片シーン”を切り取るように電子顕微鏡などで観察することができるわけです。これをコマ撮りのように撮影すれば、細胞内部の動的な現象を細部にわたり観察することができます。従来の細胞固定法で使っていた薬品による細胞損傷なども防ぐことができます。
廣川氏は、アメリカ留学から帰国後、再び東京大学で、この急速凍結電子顕微鏡法などを駆使して、ニューロンの細胞内輸送システムのメカニズム解明に本格的に着手しました。ニューロンの軸索にある微小管の上を、ミトコンドリアなどの膜小器官が行ったり来たりしている様子から、微小管と膜小器官をつないでいる運搬役、つまりモーター分子があると確信し、そのメカニズムを研究しようとしました。
モーター分子は、化学エネルギーを運動エネルギーに変換することで動くタンパク質の総称です。当時、筋肉の収縮に関係するミオシンなどのモーター分子はすでに知られていましたが、廣川氏は、細胞内の輸送システムを担うモーター分子を徹底的に解明したいと考えたのです。
研究を進め、マウスのニューロンで働いているモーター分子をまず10種類、発見しました。このとき廣川氏は、その頃に同定されたキネシンと共通的な構造をもっていることから、これらモーター分子群を「キネシンスーパーファミリータンパク質」(KIFs:KInesin superFamily proteins)と命名。その後も研究を進め、ゲノム解析などの結果からマウスやヒトを含む哺乳類のすべてのモーター分子を発見しました。モーター分子のKIF遺伝子は45個、存在することがわかっています。KIFsには、種類によって“足”の本数などの構造のちがい、輸送する荷物のちがい、スピードのちがいなどがあって個性的です。また、ニューロンだけでなく全細胞にKIFsが存在していることもわかっています。
実験のための手段や技術を自分たちでものにして、自分たちで実験をする。これが、廣川氏の研究の進め方の特徴です。研究の結果、細胞内輸送システムのメカニズムとともに、病気などとの関連性も明らかになってきました(対談記事参照)。