LF対談
生殖細胞の研究をヒトに応用するのは、
とてもチャレンジングな課題です No.74(2015.2)

京都大学大学院医学研究科 教授
斎藤通紀 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
ほぼ手付かずだった生殖細胞の分野の研究に着手
岸本 『LFニュース』歴代の対談者の中で、断とつにお若い斎藤通紀先生におこしいただきました。2013年に大阪科学賞を受賞されたときのご講演を聴いて、非常におもしろい研究をされていると思っていました。
斎藤 ありがとうございます。
岸本 先生は灘高校を卒業し、京都大学医学部に入学されたと聞きます。エリートコースですね(笑)。
斎藤 いえ。幼いころは、「研究者というのはアインシュタインとかニュートンとか、天才がやるものだ」と考えていました。ただ、生物は好きでした。理学部や農学部へ進むことも考えていたのですが、両親を含め周囲から「それで食べていけるのか」と言われまして(笑)。
岸本 医者になれと。どこもみな同じですね(笑)。医学部では、どうして生殖細胞の分野を目指すようになったんですか?
斎藤 はじめは神経系の研究をしたいと考えていたのです。医学部5年生のとき、後に恩師となった月田承一郎先生の講演を聴いて、「細胞の美しい構造には美しい機能がある」といった哲学をもっておられることに衝撃と感銘を受けまして。形態学的な分子生物学を研究すると、発想が広がるのではと思いました。
でも、細胞の構造生物学の分野には、月田先生や細胞間接着分子カドヘリンの発見者である竹市雅俊先生など、すでに著名な先生方がおられるわけで、「自分もこの分野で活躍できるのだろうか」と思い始めました。
大学院生になり月田研究室所属となり、「解明の進んでいない、細胞内の面白い構造はないかな」などと思いつつ、発生生物学の教科書を読んでいたところ、「生殖質」の説明を見つけました。生殖質は特徴的な形態をしていて、生殖質をもった細胞だけが生殖細胞として、次の世代をつくるとあります。「こんなのがあるんや」と驚きながら、生殖質に存在するような分子を解析していけば、生命を継承することの本質がわかるのではないかと思ったのがきっかけです。
岸本 それで生殖細胞のご研究を。生命にとって最も大切といってよい“血のつながり”をつくる細胞だからおもしろいですね。ただ、当時は、基礎研究があまりされていなかったとか……。
斎藤 ええ。なにを原点として、生殖細胞という全能性をもった細胞ができるのか。そうした視点の研究はほとんどなかったですね。
始原生殖細胞に必須の転写制御因子を同定
岸本 生殖細胞の大元となる細胞が、始原生殖細胞だと聞きます。斎藤先生は、始原生殖細胞がどのように精子や卵子といった生殖細胞になっていくのかにご関心をもったわけですね。
斎藤 ええ。胚の後方でつくられた始原生殖細胞が1個ずつ移動して精巣や卵巣に入っていくといったことは報告されていたのですが、分子生物学的にどういうメカニズムで生殖細胞としての特性を獲得して、その後さらに精子や卵子に分化していくのかについては、あまりわかっていなかったのです。
岸本 その研究をしようと、イギリスへ。
斎藤 はい、そうです。始原生殖細胞では発現するけれど、隣の細胞では発現しない遺伝子を同定しようとしました。そこで、大学院生時代に文献紹介ゼミで感銘を受けた論文の中で、ノーベル賞受賞者のリチャード・アクセル先生が、特定の細胞のみで特異的に出現する遺伝子をスクリーニングする独自の方法論を提唱されていたのを思い出しまして、「これを生殖細胞に応用すればうまくいくのでは」と考えたのです。幸運にも始原生殖細胞に特異的なマーカーをまず見つけることができました。
見つけたマーカーのうち、Stellaと名づけた核と細胞質を行ったり来たりする分子をマーカーにして、さらにスクリーニングをすると、Blimp1という転写制御因子が見つかりました。岸本先生もご存知のとおり、Blimp1はリンパ球の一種であるB細胞が形質細胞に分化する際に必須となる遺伝子です。これが始原生殖細胞の形成に関わる因子として現れるとはと驚きました。
Blimp1には、B細胞のプログラムの多くをシャットダウンして、主に免疫グロブリンを産出させる働きがあるとわかっていました。同様に、Blimp1は、生殖細胞においても体細胞に分化するプログラムをシャットダウンしているのではないかと考えて実験を進めたのです。その通りだということがわかり、これが一つのブレークスルーとなりました。
2003年に日本へ帰国してから、Blimp1と似た因子を探そうとスクリーニングしたところ、Prdm14という遺伝子も見つかりました。こちらも生殖細胞の形成に重要な役割をもつ転写制御因子であるとわかりました。
ES細胞を元に始原生殖細胞様細胞をつくる
岸本 その後はどう研究を進められましたか?
斎藤 転写制御因子がわかってくると、今度はそれらの因子がどうやって胚の特定の場所で誘導されるのかが疑問になりました。丹念に調べていくと、胚体外胚葉(エピブラスト)という細胞層が鍵を握っているとわかってきました。
マウスでは、発生6日目前後の段階で、胚体外胚葉は、周囲の内胚葉や胚体外外胚葉から送られるパターン形成に関するシグナルのため、生殖細胞の他に、神経や腸などの様々な細胞へと分化していくのです。そこでパターン形成に関わるシグナルを除いた上で、BMP4などの限られたサイトカインで培養すると、胚体外胚葉のほとんどすべてが始原生殖細胞に分化していくことがわかりました。「よし、胚体外胚葉をつくれば、始原生殖細胞をつくることができる」と強く思いまして。これが帰国後、理化学研究所で行った研究の主な成果でした。
岸本 その後、母校の京都大学へ戻られました。始原生殖細胞の数はわずかしかないので、多くの始原生殖細胞をつくるため、ES細胞を使うようにしたと聞きます。
斎藤 ええ、京大でいままで主にしてきた研究は、始原生殖細胞様細胞をES細胞からつくる手法の確立です。2008年に、オースティン・スミスという著名なES細胞の研究者が、ES細胞が「グランドステート」とよばれるとても均一な状態で培養する方法を報告していました。これまで、ES細胞から目的の細胞をつくるには、血清入りの培地とフィーダー細胞を加える必要があり、一定方向に細胞分化を誘導するのが難しかったのですが、この新手法を使えば目的の細胞をホモジニアスにつくることができます。
そこでこの方法で培養したES細胞を出発点に用いて、まず胚体外胚葉様細胞を誘導し、それから理研時代と同様の方法で、始原生殖細胞様細胞をつくりました。それを生体の精巣に移植すると精子になりました。卵巣に対しては少しだけ細工をしてから始原生殖細胞様細胞を移植すると、やはり卵子になりました。

斎藤通紀 氏
京都大学大学院医学研究科 教授
1970年、兵庫県生まれ。95年京都大学医学部卒業。99年京都大学大学院医学研究科博士課程修了(医学博士)、英国Gurdon Institute留学。2003年理化学研究所多細胞システム形成研究センター(理研CDB)チームリーダー。09年京都大学大学院医学研究科教授。11年科学技術振興機構(JST)創造科学技術推進事業(ERATO)研究総括を兼任。12年京都大学iPS細胞研究所特任教授を兼任。13年京都大学物質-細胞統合システム拠点連携主任研究者を兼任。13年iPS細胞研究所研究員を兼任。専門分野は細胞生物学、発生生物学。生殖細胞の発生機構を研究し、始原生殖細胞に必須な転写因子Blimp1とPrdm14を同定。ES細胞やiPS細胞から、胚体外胚葉様細胞さらに、始原生殖細胞様細胞を誘導することに成功するなど、生殖細胞の研究をリードしている。13年に「生殖細胞の発生機構の解明とその試験管内再構成」の業績により大阪科学賞を受賞するなど、受賞歴も多数。タガメ探しを趣味としている。
生殖の過程は環を描くように進む
岸本 始原生殖細胞は、どんな細胞にもなっていくのですから、いわばゲノムがすべて“裸”になっている状態なんですか?
斎藤 そうです。じつはそこがとても大事なところなのです。学生の頃、私は転写因子について研究をしていました。転写因子が発現することで細胞の運命が決まるわけですが、発現するまでのコンテクストが重要になります。たとえば、細胞と転写因子の組み合わせがむちゃくちゃであれば、うまくB細胞ができたり神経細胞ができたりはしませんよね。当時、まだ「エピジェネティクス」という言葉は使われていませんでしたが、生殖細胞の中でゲノム上の修飾ががらりと変わるということが、すこしずつ言われだしていた時代でした。
つまり、生殖細胞には、ゲノムをいったん“裸”にして、それからつくり直すような、ユニークな能力があるのではないかと言われていたのです。
岸本 ということは、始原生殖細胞の段階では、やはりゲノムはすべて“裸”なんですか?
斎藤 最近わかってきたのは、その度合がとても強いということです。始原生殖細胞が形成されるときには、エピゲノムのリプログラミングが起きていることがわかりました。たとえば、卵子や精子に分化するより前の段階では、ゲノムのメチル化がゼロに近くなります。
岸本 そうすると、始原生殖細胞は、ES細胞やiPS細胞と同じようなものなんですか?
斎藤 それがまた、ちがうのです。ES細胞では、受精卵からお父さんとお母さんのゲノムが来るわけですが、それぞれの遺伝子が両親のどちらから受け継いだものであるかを覚えているゲノムインプリンティングのマークは保たれています。始原生殖細胞のほうは、ゲノムインプリンティングさえも一旦消去されます。“裸”の度合いが高いといいますか。ここが、大きな違いですね。
岸本 けれども、ES細胞を元にして、始原生殖細胞をつくったわけでしょ。ES細胞よりも“原始的”な始原生殖細胞を、ES細胞からつくり出すとは、どういうことなんでしょうか?
斎藤 生殖の過程は環を描くようになっているわけです。ES細胞も胚盤胞の一部の細胞から作製されていて、その胚盤胞が発達して、始原生殖細胞になっているわけで。どこが起点かというのは難しいのです。
ES細胞やiPS細胞と始原生殖細胞がどちらが原始的かというのは、なかなか難しい議論だと思いますね。それでも、ES細胞やiPS細胞は、生殖細胞を含めてすべての細胞に分化しますし、再生医学の発展にも寄与しているので素晴らしい細胞だと思います。
ヒトへの応用も視野 科学の利用のされ方を考える
岸本 始原生殖細胞が精巣に行ったら、そののちに精子になり、卵巣に行ったら、卵子になるわけですね。それぞれ、異なる環境下で、どのようなシグナルが働いているんですか?
斎藤 そこは、現在盛んに研究されつつある大事なテーマになってきます。
精子と卵子それぞれがつくられる際、それらに体細胞が寄り添っていることがわかっています。精子については、精原幹細胞とセルトリ細胞という細胞です。卵子については卵細胞とそれを包み込んでいる顆粒膜細胞という細胞です。これらの常に一緒にいる細胞同士が、複雑なシグナルのやりとりをしていることがわかっています。
岸本 すると、そのシグナルを解明して、始原生殖細胞を作用させたら、精子や卵子を人工的につくることができるようになるんでしょうか?
斎藤 理論的にはそうなると思います。しかし、現状ではまだそれには遠く及ばない状態です。どちらかというと卵子のほうが近いとは思いますが。精子のほうは、いわば雄のゲノムを運ぶためのメッセンジャーのように特異的に分化していますが、卵子のほうは始原生殖細胞のまま大きくなっていくといった感が強いからです。
岸本 もう一つ、お聞きしたいのは、精子と卵子のつくられかたの違いです。始原生殖細胞が精巣に入って精子に、卵巣に入って卵子になるということですが、精子のほうは長らくつくり続けられるのに対して、卵子のほうはある程度つくられる数が決まっていると聞きます。
斎藤 その通りです。精子については、始原生殖細胞が成熟して、精原幹細胞になり、この幹細胞になった段階で増えていきます。一方、卵子については始原生殖細胞が直接、卵細胞形成のために減数分裂を始めますので、その後は決して数は増えないのです。
われわれが考えているのは、始原生殖細胞を、ES細胞のように自由に増やすことができれば、“卵子幹細胞”の役割を担わせられるのではないかということです。
岸本 すると、例えば、始原生殖細胞をES細胞などでたくさんつくって、精子にして、また卵子にして、両方を受精させれば個体ができるわけですか?
斎藤 ええ。マウスではもうすぐ実現できると思います。つくった卵子とつくった精子同士での個体づくりは、卵子が脆弱であるといった課題があるためにまだ成功していませんが、つくった卵子と通常の精子の組み合わせ、またつくった精子と通常の卵子の組み合わせではすでに個体づくりをしています。近いうちには、つくった卵子と精子同士でも実現できると考えています。
岸本 マウスで成功すれば、その次の段階ではサルですよね?
斎藤 そうですね。
岸本 サルの次には、いよいよヒトという対象も視野に入ってきますよね。
斎藤 ええ、産婦人科の先生方からの、強い期待を感じています。
岸本 もし、それが実現したら、人工的に精子と卵子をつくって人工授精させて、ヒトをたくさんつくり出すといった可能性も出てくるわけですか?
斎藤 まあ、すぐには実現しないと思います。マウスとヒトでは、やはり細胞の質や、発生の速度などが大きく異なりますので、マウスで培った技術をヒトに応用するのは、とてもチャレンジングな課題の一つになると思います。
岸本 もし仮に、それが実現したとすると、それは良いことなのか、悪いことなのか……。
斎藤 これに限ったことではありませんが、科学というものは使い方次第ではないかと思います。例えば、ノーベル賞を創設したアルフレッド・ノーベルは、液体の爆薬を固形化したダイナマイトを発明したわけですが、ダイナマイトは、戦争兵器としても使われていますし、山を掘削するのにも使われています。
体外で精子と卵子をつくる技術についても、倫理的な課題がある一方で、精子や卵子の形成異常に伴う、不妊の病気をもっておられる方もいます。それに対してモデルとなるような実験系もないのが現状です。ですので、ヒトの生殖細胞の形成機構を再現するということは、私はとても重要ではないかと思っています。
岸本 1930年代に、オルダス・ハクスリーという小説家が『すばらしい新世界』という小説を書きました。人工子宮で胎児を育てる、培養環境を変えることで人としての特性を決めてしまうといった話もされていて、当時も相当話題になったと聞きます。そうしたことが可能な世界が、良い世界かという点は、難しい問題だと思います。
斎藤 難しいですね。そういう方向を目指して研究をしてきたわけではなく、研究に付随してそういう可能性はつきまといますから。研究成果を発表した者として、責任のようなものがあることも感じます。この問題にはこれからも対峙していきたいと思っています。
基礎医学の研究成果も確実に積み重ねていきたい
岸本 研究分野の裾野は広がってきていますか。
斎藤 そうですね、それは感じます。海外に行って発表をしたり、研究所に招かれて研究者たちとお話をしますが、マウスの系では多くのグループが始原生殖細胞を使い始めています。研究のクオリティは別にしても、ヒトを対象とした研究の競争も激しくなっています。
岸本 世界の研究者が追随してくるようになったわけですね。
斎藤 それは感じますね。
今後、基礎医学的な研究についても、詰めていかなければならないことが数多くあります。そこも確実にやっていきたいですね。築いてきたものは明確になってきている気はしますので、一つひとつの目標に向かって、さらに一個ずつまじめに成果を積み上げていきたいと思っています。
岸本 今日はどうもありがとうございました。
EYES
生命を次世代に引き継ぐ
生殖細胞の形成メカニズムを解明し、試験管内で再現する
生命の根源に迫るとともに、不妊などの治療法開発の知見を得る
基礎と応用、両面の発展に期待
私たちヒトを含む多細胞生物は、親から子へ、子から孫へと、次の世代に連綿と生命のバトンを引き継いでいます。この営みを可能にしているのが、「生殖細胞」という細胞です。細胞は、主に体細胞と生殖細胞に分けることができます。神経、血液、骨、臓器などをつくる体細胞のほうはその世代限りで使命を果たしますが、それに対して精子や卵子などからなる生殖細胞は、果てしなく新しい生命を生み出していく能力をもっています。
ヒトやマウスなどの多細胞生物の個体において、細胞がどのように成長して精子や卵子がつくられていくか、その過程の解明が急速に進んでいます。まず、受精卵が細胞分裂をしていくと、胚盤胞とよばれる構造ができます。さらに、この胚盤胞の中の内部細胞塊という細胞層では、「胚体外胚葉(エピブラスト)」という一層からなる細胞の構造がつくられます。
胚体外胚葉は、体細胞と生殖細胞のすべての大元となる細胞です。胚体外胚葉から最終的に精子や卵子がつくられるまでには、まず「始原生殖細胞」という細胞がつくられます。始原生殖細胞がつくられるタイミングは、精巣や卵巣が形成されるより前の段階であり、つくられる場所も後に精巣や卵巣となる場所とは離れた胚の後方です。また、発生初期段階でつくられる始原生殖細胞の数もマウスで20〜30個ほどと、ごく限られたものです。
この始原生殖細胞が、後につくられた精巣や卵巣へと移動していきます。精巣では、始原生殖細胞から精原細胞がつくられ、その一部が幹細胞の役割を果たします。精母細胞の段階を経て、大量の精子がつくられつづけます。一方、卵巣では、始原生殖細胞から卵原細胞がつくられます。卵原細胞のうち、一次卵母細胞、さらに二次卵母細胞へと成長していった細胞が卵子になります。
生命を次世代へ引き継ぐという、体細胞にはもちえないユニークな能力のしくみを解明するためには、生殖細胞の発生のしくみを解き明かすことが大切になります。
今回の対談に登場する斎藤通紀氏は、「どうして、生殖細胞だけが新しい個体を生み出せるのか」というテーマをもち、生殖細胞が形成されるメカニズムを、主に分子生物学的な観点で研究してきました。
まず、胚体外胚葉の一部が、体細胞でなく生殖細胞になっていく道をたどるのには、Blimp1とPrdm14という2つの遺伝子が重要な鍵を握っていることを突き止めました。Blimp1とPrdm14が発現誘導された胚体外胚葉では、体細胞となるプログラムが抑えられ、始原生殖細胞への分化が始まります。始原生殖細胞がつくられる過程では、潜在的な多能性を維持する遺伝子発現が回復するとともに、すべての遺伝子の使われ方を制御する後天的ゲノム修飾であるエピゲノム情報がリプログラミング(初期化)されることが斎藤氏の研究でわかってきました。
さらに斎藤氏は、では、Blimp1やPrdm14などの遺伝子が、生体内でどのように発現誘導されるのかを解明しようとしました。ここでは、細胞から放出されて様々な働きをする因子であるサイトカインの一種、BMP4とWNT3が、遺伝子Blimp1やPrdm14の発現を誘導することで、胚体外胚葉のすべての細胞を始原生殖細胞にすることが出来ることを突き止めました。こうして遺伝子やサイトカインが特定されたことにより、始原生殖細胞がつくられるための条件が出揃ったことになります。
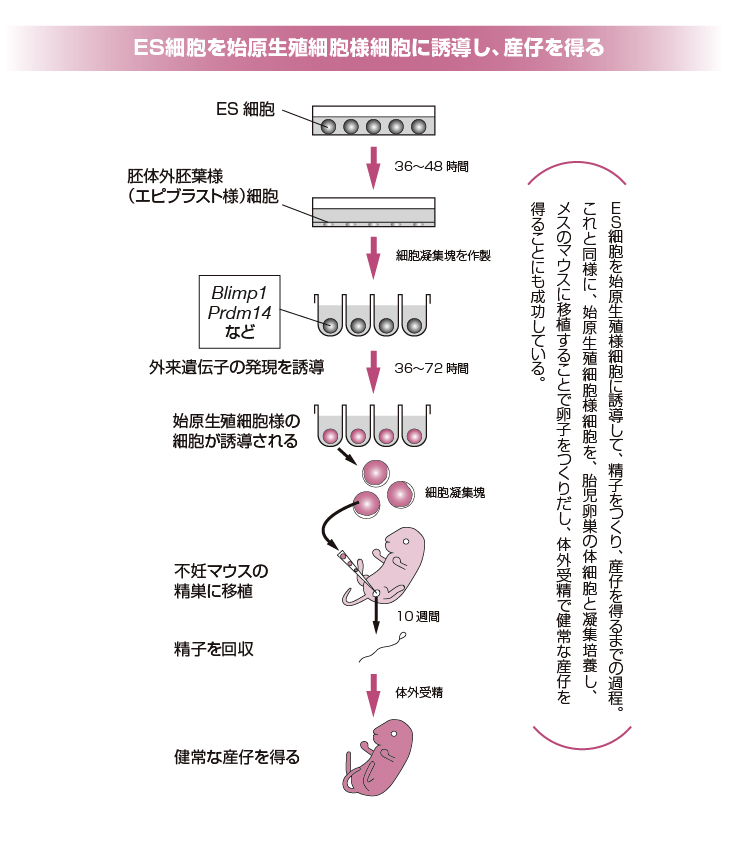
始原生殖細胞の数がとても少ないのは、研究を進める上での制約になります。そこで斎藤氏は、ES細胞やiPS細胞のような増殖能を持つ細胞から始原生殖細胞の形成を導き出す手法も開発しました。胚体外胚葉と同様の細胞(胚体外胚葉様細胞)をつくり、さらにその細胞から、始原生殖細胞と同様の細胞(始原生殖細胞様細胞)をつくり出したのです。マウスの始原生殖細胞様細胞からつくられた精子や卵子からは、健常な産仔がおこなわれることが確かめられています。
生殖細胞の機能や形成のしくみを解明していくことは、生命の根源に関する知見を得ることにつながります。それとともに、不妊、遺伝病、生殖細胞の老化、生殖細胞がんといった、生殖に関わる病気の予防法や治療法を開発するための知見を得ることにもつながりえます。今後、基礎と応用の両面で研究が発展していくことが期待されます。