LF対談
多剤併用療法でHIV感染者の余命は伸び、
世界では新規感染者数も減っています。 No.76(2015.10)

熊本大学大学院生命科学研究部 血液内科・膠原病内科・感染免疫診療部 教授
満屋裕明 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
日本で扱ってきたT細胞株を留学先でも活かして免疫研究
岸本 エイズはかつて「死の病」と言われていましたが、いまは完治しなくとも、死には至らぬ慢性病になったと聞きます。満屋先生は、その状況改善に大きな貢献を果たされました。「名声は遅れてやってくる」という言葉がありますが、近年は慶應医学賞、朝日賞、学士院賞と、数々の賞を受賞されていますね。
満屋 どうもありがとうございます。
岸本 1982年にアメリカに行かれるより前から、僕は満屋先生を知っています。僕の先輩の岸本進先生が熊本大学医学部第二内科の教授だったとき、満屋先生も同じ免疫学の教室に所属されてたんですよね。
満屋 そうです。当時、私は原発性免疫不全症の研究をしていました。いまの研究分野も免疫不全症関連ですから、研究者としては「幸せ者」だと思っています。
岸本 岸本進先生から「満屋君をどこかよい所に留学させたい」と言われて、僕はヒトの免疫研究で第一人者だった米国国立衛生研究所(NIH)・国立がん研究所(NCI)のトム・ウォルドマンに推薦状を書いたのでした。
満屋 その際は本当に有り難うございました。先生からトム・ウォルドマン先生の教室を御紹介して頂かなかったとしたら、私はここにいなかったと思います。先生の推薦状で、いざ渡米することとなりましたら、トム・ウォルドマン先生所属のサミュエル・ブローダーから、「自分のところに来てくれないか」と手紙をもらいました。「呼ばれたからには」と行ってみると、それは小さな研究室でした。ブローダーから「これから研究することをディスカスしよう」と言われましたので、翌日、T細胞株をつくって、成人T細胞白血病(ATL)の原因であるT細胞白血病ウイルス1型(HTLV-1)に感染した細胞と非感染の細胞と比較して抗原特異性や免疫反応の検討をする研究と、もう一つ、HTLV-1に特異的な細胞傷害性T細胞(CTL)をつくる研究を提案しました。すると、あっさり「よし、そうしよう」となりました。
岸本 満屋先生は、熊本大学時代から、T細胞株を作ってこられました。それがつながっているんですね。
満屋 はい。ブローダーの研究室で、私は日本での研究で多用しておりました、破傷風の作る毒素であるテタヌストキソイドを抗原とし、これに特異的に反応するT細胞株を作りました。その実験では、正常なT細胞に抗原刺激をあたえて、最初のヒト病原性レトロウイルスであるT細胞白血病ウイルス(HTLV)に感染させると、HTLVの遺伝子がT細胞の遺伝子に入りやすいこと、そしてHTLV感染で特異的な免疫応答能が減少して、やがて自律増殖を開始することを解明しました。結局、日本でしてきたことがだいぶ役立ったと思っています。
HIV研究に着手
逆転写酵素阻害剤「AZT」を開発
岸本 満屋先生はアメリカ留学時代にHIV関連の研究も始められましたね。ブローダーの研究室に入った1982年、エイズウイルスはもう見つかっていたのですか。
満屋 まだでした。フランスのリュック・モンタニエが「どうもそうではないか」と報告したのが1983年のことです。
岸本 満屋先生がおられたNCIには、自分こそがHIV発見者だと言い張っていたロバート・ギャロがいましたね。
満屋 はい。ギャロは私のいた研究所とは数百メートル離れた棟にいたので、日常的に会うことはありませんでした。ギャロが「自分が見つけた」としてHIVを報告したのが1984年でした。それは後に、ギャロがフランスから入手したウイルスであったことが発覚するわけですが。
岸本 満屋先生は、どうしてエイズの研究をしようとされたんですか。当時は感染の危惧もあり、研究者はみな嫌がっていたでしょう。
満屋 ものすごく嫌がっていましたね。ただ、私はT細胞の株をもっていましたし、レトロウイルスに関する勉強もかなりさせられていましたから。加えて、ブローダーが「エイズのウイルスが手に入るとギャロから聞いた」と言い、「ミツヤにやってもらったらいい」となったのです。
岸本 怖いとは思わなかったですか。
満屋 思いましたね。「これは困ったな」と。しかし、HTLV-1の研究で患者の血液を浴びる経験もしていましたが、自分はHTLV-1に感染していない。エイズ患者の診療に当たっていた医師や看護師が次々とエイズを発症するという事は全く聞いておりませんでしたし、HTLV-1もHIVもレトロウイルスですから、「レトロウイルスにはそう簡単に感染しないだろう」と勝手に推測したのです。いま思うと、HIV感染からエイズ発症までには5年から10年のいわば「潜伏期間」があるので、仮にHIVがより感染しやすいウイルスだったら、いまごろどうなっていたかわかりません。
岸本 それで、ギャロからHIVを提供されて、どのようなことを……。
満屋 逆転写酵素を阻害する薬を作ることに狙いを定めました。すでに作っていたT細胞株を用いて、抗レトロウイルス活性を示す物質を探しました。けれども、そうした物質が見つからず、暗礁に乗り上げました。
そうした時に、ブローダーの研究室に新しく加わったドクターの1人が、NIHのカフェテリアでの昼食で一緒になった研究者に「ミツヤがエイズ治療薬の開発を始めた」と話したようなのです。するとその研究者から、眠り病ともいわれるトリパノソーマ症の治療薬「スラミン」に逆転写酵素阻害効果があるとの話を聞いたのです。この報告を聞いたブローダーがすぐスラミンを入手しました。試してみると、たしかに効果がありました。スラミンの効果についての論文はわずか13日でScience誌に受理されて、結局1984年には10ヶ月の間にHTLV-1の仕事も含めてScience誌に三つ論文を発表することになり、周囲で騒がれたりしました。けれどもスラミンを人体に投与しても副作用だけで効果はないとわかり、エイズ治療薬にはなりませんでした。
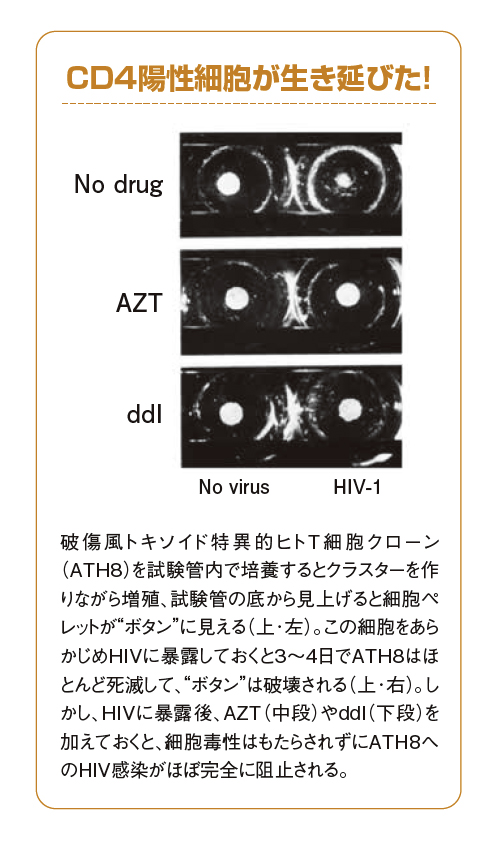
岸本 でも、満屋先生は、T細胞株にHIVを感染させるとT細胞が死ぬというアッセイ系をお作りになっていた。それで、その後に、世界初のエイズ治療薬となるアジドチミジン(AZT)を発見されたんですよね。
満屋 ええ。スラミンを臨床試験で患者に投与しても効かなかったので“次”が必要でした。そこで、いわゆる化合物ライブラリーを提供してもらおうと、ブローダーが様々な企業などに働きかけてくれました。すると、二つの企業が応じてくれたのです。
一社は、いまのグラクソ・スミスクラインの前身にあたるバローズ・ウェルカム。もう一社はブリストル・マイヤーズ・スクイブ(BMS)です。それで、バローズ・ウェルカム提供の候補化合物の一つに「コンパウンドS」という名でAZTがありました。ただし、AZTは他の研究機関ではHIVに対する効果はないという結果しか出ていませんでした。実は、ずっと後になって判明したのですが、彼らは逆転写酵素に対する効果をみたらしく、それもAZTを三リン酸化していなかったからなのです。私のアッセイ系では、ヒトの細胞を用いていました。ヒト細胞内ではAZTが三リン酸化されるので、DNA鎖の停止が効率よく起き、逆転写酵素阻害の効果が得られたのです。
岸本 熊本大学時代から、満屋先生はヒトのT細胞株を使った研究を続けてこられた。それがよかったわけですね。
1987年にAZTは発売されましたね。
満屋 はい。けれども、AZTは記録的に高価な薬になってしまいました。当初、開発はバローズ社と進めていましたが、「死の病気をもたらす生体試料、患者血清なので会社には持ち込めない」などと言われ、すべて私たちNCI側で研究を進めたのです。ところが、バローズ社は特許を秘密裡に申請し、AZTに年間1万ドルになるような当時としては史上最高値が付けられたのです。AZTを必要としても買えない多くの患者が死んで行きました。
岸本 そうでしたか……。
第二、第三の薬「ddI」「ddC」の開発で多剤併用療法が可能に
満屋 「これはもう、第二、第三の新薬を開発する以外に治療薬が安くなることはない」と決心し、生化学の勉強をもう一度しなければと、熊本大学時代に丸暗記していた山村雄一先生の『新医化学』を読みなおしていたのです。それで、AZTと同様、ヒト細胞内で効率よく三リン酸化する化合物を見つければ、それらもDNA鎖の停止が起きてうまくいくかもしれないという発想が生まれました。テクニシャンに「ddI」、「ddC」、「ddT」、「ddG」という一連の化合物を注文してもらい、私のアッセイ系で実験すると、やはりヒトの細胞でこれらも三リン酸化して、HIVの増殖が強力に阻害されるとわかりました。「ddI」「ddC」は第二、第三のエイズ治療薬になりました。
「やはりヒトの細胞を扱っていてよかったな」と思いました。ヒト細胞を扱っていなかったら、ここまで幸運ではなかったと思います。
岸本 それで、ddIとddCも、エイズ治療薬として企業から発売したわけですね。
満屋 そうです。ddIはBMSから、ddCはロッシュからです。一方の、AZTの価格は、少なめの投与に変更されたということもありますが、暴落しました。溜飲が下がりました。
岸本 満屋先生が打ち立てた、AZT、ddI、ddCの3薬で、多剤併用療法が始まったわけですか。
満屋 はい。
岸本 三つの薬は、どれも逆転写酵素阻害剤に分類されていますが、それでも多剤併用療法になるんですか。
満屋 はい。例えば、AZTは増殖中の細胞でチミジンキナーゼによってとても効率よく一リン酸化されて逆転写酵素阻害の効果を発揮しますが、増殖していない細胞ではチミジンキナーゼが少ないため効果があまり得られないのです。しかし、ddIやddCは他の酵素により、増殖していない細胞でも効率よくリン酸化されます。これらの薬を足し合わせると、相乗効果のようなものが臨床でも得られることが後にわかってきました。少なくともAZTとddIの組み合わせでは、単剤での治療よりもかなり良い成績が得られました。

満屋裕明 氏
熊本大学大学院生命科学研究部 血液内科・膠原病内科・感染免疫診療部 教授
1950年、長崎県生まれ。75年熊本大学医学部医学科卒業。82年米国国立癌研究所(NCI:National Cancer Institute)研究員。91年米国国立癌研究所、レトロウイルス感染症部部長。97年熊本大学医学部内科学第二講座教授。同年、日本学術振興会未来開拓学術研究推進事業「HIV-1感染症の病理病態解析とその治療法の開発」リーダー(2002年まで)。2008年熊本大学グローバルCOE「エイズ制圧を目指した国際教育研究拠点」リーダー。現在は、熊本大学大学院での上記職の他、国立国際医療研究センターで理事、臨床研究センター長を、また、NCIでレトロウイルス感染症部部長、獨協大学医学部で特任教授を、熊本大学医学部附属病院では感染免疫診療部部長、治験支援センター長を併任。専門分野は臨床内科学、感染症学(とくにエイズ治療学)など。受賞歴は米国癌研究所発明賞、NIH所長賞、第1回 NIH World AIDS Day Award、紫綬褒章、NCI HIV/AIDS Research Excellence Award、慶應医学賞、高峰記念三共賞、読売国際協力賞、朝日賞、日本学士院賞など多数。
現在も有力なプロテアーゼ阻害剤
「ダルナビル」も開発
岸本 その後、逆転写酵素阻害剤とは別に、プロテアーゼ阻害剤も開発されましたね。こちらはHIV増殖に必要なプロテアーゼの働きを阻害すると……。
満屋 はい。私は、プロテアーゼ阻害剤のうち「ダルナビル」を開発しました。熊本に戻り、1997年頃から、アメリカの有機化学を専攻する研究者との共同研究で、2003年に初めて成果を日本から報告しました。2007年には日本でもエイズ治療薬として使われるようになり、現在も副作用が少なく、HIV耐性の発現を遅延させるということで使われています。
岸本 HIVの変異に対して強いのですね。
満屋 HIVの薬剤耐性変異の獲得に抵抗します。
岸本 それはどうしてでしょう。
満屋 既存のプロテアーゼ阻害剤は、標的となるアミノ酸の側鎖に結合しますが、ダルナビルは主鎖と結合します。HIVにとっては、側鎖にプロテアーゼ阻害剤が結合していれば、アミノ酸をすこし変えるだけで結合力を失わせられる、つまり抗ウイルス薬の結合から「逃げる」事ができるので、耐性獲得が起こるのですが、プロテアーゼの活性部分のアミノ酸の主鎖に結合されると主鎖の立体構造はアミノ酸変異が起こってもあまり変わらないため、耐性を獲得しづらいわけです。
ダルナビルにはもう一つ特徴があります。プロテアーゼは、2個のサブユニットが二量体化してタンパク分解酵素としての活性を獲得するのですが、ダルナビルはタンパク間相互作用であるこの二量体化を阻害します。これでプロテアーゼはいわば「ハサミ」が作れなくなるので、HIVは機能を持った成熟タンパクをつくれず、感染性を獲得できなくなります。
ダルナビルには、この二つの作用があることが判明したのです。
治療効果は世界では顕著一方の日本国内では……
岸本 逆転写酵素阻害剤が最初に出回ったところに、プロテアーゼ阻害剤も加わり、3剤や4剤を併用したエイズ治療法が確立されたんですね。そのあたりから、「エイズは死なない病」となっていったわけですか。
満屋 はい。今や、例えば20歳でHIVに感染した人がきちんと治療を受ければ余命は40年から50年ほどになります。つまり60歳から70歳ぐらいまで生存できるわけで、非感染者と同等の平均余命が得られるようにまでなりました。
岸本 効果も見えていますか。
満屋 ええ。感染者がきちんとした治療を受ければ、本人が長生きできるとともに、二次感染も殆ど起こらなくなる事が分かっています。アフリカでは多剤併用療法が広まるにつれて、2000年からわずか2年の間で新規感染者数が2分の1にまで減りました。治療する事によって感染者から非感染パートナーへのHIV感染は96%も減少する事が発表されたのは2011年の事で、この報告はScience誌上で2011年のブレークスルーと高く評価されました。
岸本 HIVが感染者の体内から全くなくなるわけではないんですよね。それでも、他人への感染は減るんですか。
満屋 そうなのです。たしかにウイルスを感染者の体内から1個もなくなるようにするのは極めて難しいのですが、きちんとした治療で血中のHIV数を検出限界以下までにすることはできます。HIVに感染した母親が治療を受けますと、その感染母体から生まれる子供にも感染が起こらなくなります。
岸本 なるほど。
満屋 結核対策の基本戦略といっしょで、感染者を見つけて必ず治療することが、蔓延を防ぐことになるわけです。
岸本 日本でのHIV感染者の増減はいかがですか。
満屋 残念ながら、新規感染者数はなかなか減少しません。どのような行為をするとHIVが感染するかといった知識は感染者も感染のリスクのある人達も当然ご存知と思うのですが、まだ啓発が足りていないのか……。
岸本 薬もそんなに高くないのなら、きちんと飲めばいいわけですよね。
満屋 実を言いますと、日本国内では薬代に年間250万円ほどかかり、安いとはいえません。アフリカなど開発途上国に対しては、オバマ大統領がエイズ治療薬の特許を無償で供与する方針を出して、ダルナビルは世界で最初のそうしたジェネリック薬として使われています。無論、欧米や日本では特許は有効で、普通の値段で売られています。薬は一生、飲み続けなければならないので、例えば40年生存すると薬代だけで約1億円になります。いま、日本では新規のHIV感染者と新規のエイズ発症者の総計は毎年併せて1500人前後。この事は私達と次の世代の両肩に毎年1500億円の医療費負担がのしかかって来ていることを示します。限りある医療資源が毎年、新しくそこに注ぎ込まれなければならない状況です。これは大きな問題だと思います。
「やった!」という瞬間があるから研究はやめられない
岸本 最近は、どのような研究をされていますか。
満屋 逆転写酵素阻害剤になりますが、「EFdA」という化合物の開発をヤマサ醤油などと続けてきました。3年前、臨床研究への目処が付いたので、この化合物の臨床開発の権利をメルクに供与しました。欧州では、臨床試験の第一相まで進んでおり、極めて良好と聞きます。
岸本 どういった作用があるんですか。
満屋 AZTやddI、ddCと同様、DNA鎖の停止を起こすのですが、それらとは異なる構造をもっています。例えば、AZTの場合、AZT一リン酸化の段階でそれ以降のリン酸化が進みにくく、活性物質であるAZT三リン酸体が増えないという欠点があるのですが、EFdAの場合は活性物質であるEFdA三リン酸体が充分に増えるといったことがあります。AZTなどでは治療をしているうちに標的である逆転写酵素に変異が起きて治療効果が失われることが多いのですが、EFdAでは変異が起きにくく、また変異が起こってもEFdAの抗HIV効果もそれほど失われません。現在は霊長類で長期毒性がないかどうかが確かめられているところです。
岸本 その新薬にかぎらず、毒性をなくすことが課題になるわけですか。
満屋 その通りです。「死なない病気」になると、治療薬の毒性のハードルは高くなります。アメリカの製薬企業の開発担当者はよく「これからのエイズ治療薬に課題は三つある。一に毒性、二に毒性、三に毒性だ」などと言っています。副作用を含めた毒性の課題は極めて大きくなっています。しかし、決して解決不可能な課題ではないと思っています。
岸本 いま、満屋先生は65歳。どこかに「あと15年ぐらいは研究を続けたい」と書かれていましたね。
満屋 岸本先生に負けないように(笑)。
岸本 この前、満屋先生が朝日賞を受賞されたとき、小説家ガルシア・マルケスの「私はなにかを語りたいという幸せな病気にかかっている」という言葉を引用して、「私は病める人に尽くしたいという幸せな病気にかかっている」と挨拶しておられましたね。
満屋 そうでした。私も、ときどき「やった!」という瞬間が来るので、研究はやめられません。だから、本当に「幸せな病気にかかっている」と思っています。
岸本 お話、ありがとうございました。
EYES
HIV増殖の過程を複数のしくみで阻害 多剤併用療法によりエイズは「死の病」から「慢性病」に
逆転写、プロテアーゼ、DNA組込……
HIV増殖の各段階に有効な治療薬が誕生
感染者の余命が劇的に伸びた
エイズ(後天性免疫不全症候群、AIDS:Acquired Immune Deficiency Syndrome)は、エイズウイルスともよばれる「ヒト免疫不全ウイルス(HIV : Human Immunodeficiency Virus)」がヒトの免疫細胞に感染することで生じる病気です。感染したヒトの体では、平均10年という長い潜伏期間の後に、免疫機能に異常をきたし、通常であれば生じることのないような病気が生じて、カポジ肉腫などの悪性腫瘍を発症します。
世界初のエイズの症例は1981年、米国疾病対策予防センターにより報告されました。また、1983年にはフランス・パスツール研究所のリュック・モンタニエらによりHIVの単離が報告されました。
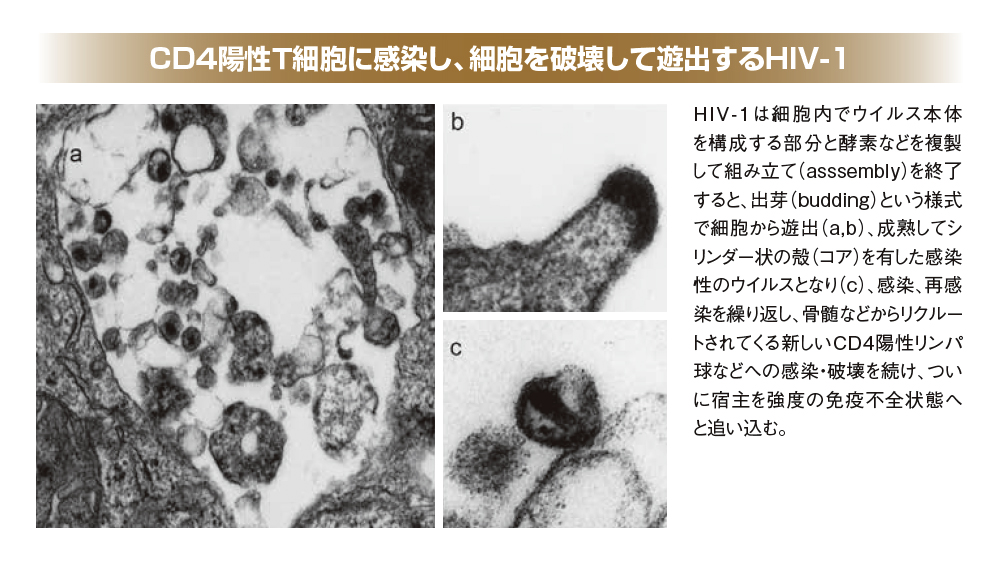
HIVは、ヒトの免疫システムを司るT細胞などの表面に付着、侵入し、細胞内でHIVのDNAを合成します。さらにこの細胞の中にHIVのDNAを組み込み、HIVの組み立てに必要な部品を作り、新たなHIVを組み立てて、それを細胞外に放出することで増殖していきます。1980年代後半頃まで、エイズは「死の病」として恐れられてきました。HIVの増殖を抑えるような有効な治療薬が全くなかったためです。
ところが近年、エイズ治療をめぐる状況は大きく変貌を遂げました。少なくとも費用をかけて治療を受け続ければ、ほぼ確実に病気の進行を抑えることができるようになったのです。「死の病」とされていた時代には、例えば20歳でHIVに感染した人の余命は「1年、長くても数年」とされていました。現在では、その余命は「40年から50年」とされています。
では、どうしてエイズ治療の状況は大きく改善されたのでしょうか。背景には、有効な治療薬が複数種、開発されたことにより「多剤併用療法」が可能になったということがあります。多剤併用療法とは、複数の抗HIV薬を組み合わせて投与し、HIVの増殖を抑える療法です。
まず1987年、世界初となる抗HIV薬として「アジドチミジン」(AZT:Azidothymidine)が、今回のLF対談にご登場いただく満屋裕明氏(熊本大学大学院生命科学研究部教授)により開発されました。AZTは、抗HIV薬の中で「逆転写酵素阻害剤」という種類にあたる薬です。これは、HIVがもっている逆転写酵素という酵素の働きを阻害するしくみをもつ薬。生体での通常のタンパク質合成では“DNAからRNA”が転写されるという過程を踏みますが、これとは逆に“RNAからDNA”が転写されるという過程を踏むことがあり、これを「逆転写」とよびます。HIVは、自らのRNAを遺伝物質としており、ヒトのT細胞などの内部に侵入すると、逆転写により“RNAからDNA”をつくります。そうしたことから、逆転写を起こすRNAウイルスは「レトロウイルス」と総称されます。
HIVは、逆転写を起こす酵素をもつレトロウイルスなのです。一方、ヒトの体は逆転写酵素をもちません。そこで、逆転写酵素の働きを阻害する薬を投与すれば、HIVの増殖過程を食い止められるわけです。
逆転写酵素阻害剤AZTは、HIVが感染した細胞内で、三リン酸化体に代謝されます。これはHIVが逆転写するとき必要な成分とよく似ており、HIVが間違えて取り込んでしまいます。そのため逆転写の過程が阻止されて、結果、HIVの増殖を抑えることになります。
1992年にはさらに、逆転写酵素阻害剤として「ddI」「ddC」という新薬が満屋氏により開発されました。同じ逆転写酵素阻害剤でも、AZTとは異なるしくみで逆転写を阻害するため、これによりエイズ治療の多剤併用療法が幕を開けたことになります。
1990年代後半になると、逆転写酵素阻害剤とは異なる「プロテアーゼ阻害剤」という抗HIV薬も開発されました。プロテアーゼとはタンパクを分解する酵素のこと。HIVに感染した細胞内では、HIVに特有のプロテアーゼが“はさみ”のごとく働いて、HIVの複合タンパクを適宜切断して、機能を持った成熟タンパクに仕上げます。成熟タンパクが出来てはじめてHIVは増殖します。プロテアーゼ阻害剤は、その“はさみ”の刃の部分にはまり込み、HIVのタンパクが切られて成熟化される過程を邪魔するのです。米国では1996年、日本では1997年に「インジナビル」というプロテアーゼ阻害剤が使われ始めました。その後も満屋氏らが開発した「ダルナビル」など、複数のプロテアーゼ阻害剤が開発され、使用されています。
逆転写酵素阻害剤とプロテアーゼ阻害剤という、しくみが大きく異なる抗HIV薬が同時に使われることになり、多剤併用療法の効果は増大しました。1995年から2000年初頭にかけて、世界でのエイズによる死者数は年間約120万人から約40万人へと、急激に減少しました。さらに、2000年代後半には、逆転写で生成されたDNAを宿主細胞(ここではヒト細胞)のDNAに組み込む過程を阻害する、「インテグラーゼ阻害剤」という抗HIV薬も実用化されています。
それぞれの薬は、HIVを生体内から根絶するものではありません。HIV感染者がエイズの症状を生じさせないためには、その人に最適な抗HIV薬の組み合わせで、毎日服用することが必要です。逆にそれを実行すれば、エイズを「死の病」と悲観する必要はなくなったのです。