LF対談
幅が広くて、かつ奥が深い。
免疫学はこれからも重要な分野で あり続けると思います。 No.77(2016.2)

東京大学 名誉教授・東京大学生産技術研究所 特任教授
谷口維紹 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
朝永振一郎先生の姿に感動して
岸本 谷口先生とは、大阪大学細胞工学センター時代にご一緒させていただきました。『LFニュース』では、岡田善雄前理事長を偲んでの追悼座談会(第54号掲載)にもご参加いただきました。
谷口 よろしくお願いします。
岸本 谷口先生は和歌山の「田舎」ご出身というお話でしたね。
谷口 はい。山の中で育ちました。耐久高等学校という歴史の古い学校に通いまして。田舎の高校なのでのんびりしており、その先の進路はあまり考えていなかったんですが、高校3年のとき朝永振一郎先生がノーベル物理学賞を受賞されましてね。お姿を新聞などで見て、「学者って素晴らしいな」と感動したんです。それで、朝永先生が在籍していた東京教育大学(現・筑波大学)理学部を受験したんです。大学では朝永先生の物理学の講義も聴かせていただき感動しました。
岸本 そうでしたか。その後は、イタリアのナポリ大学の海洋研究所に留学されましたね。当時、留学といえばもっぱらアメリカだったのに、どうしてイタリアへ……。
谷口 ナポリ海洋研究所に派遣されていた助手の先生が私に目をかけてくれたんです。そこは白血球の食作用の研究でノーベル賞を受賞したイリヤ・メチニコフもかつて活躍していた有名な研究所。私は、大学に憧れて入ったものの、古い体質などにちょっと落胆していたところがあって。助手の方から「もう1回、人生をリセットしたらどうか」と言われ、その気になって実験助手としてナポリに行ったんです。
岸本 そうでしたか。ナポリでは、どんな研究を。
谷口 いろいろでしたが、例えば、RNAポリメラーゼの精製をやりました。遺伝子の発現調節など、分子生物学の研究にはすでに興味ありましたね。それで、所属先のマッシモ・リボナッティ先生が、スイスのチューリッヒ大学のチャールズ・ワイスマン先生と親友だったんです。ワイスマン先生に私のことを紹介していただき、途中から大学院に入って学位を取りました。
岸本 チューリッヒ大学では谷口先生はどのような研究を。最初からインターフェロン(IFN)関連ですか。
谷口 最初はちがったんです。バクテリアに感染して増殖するウイルスをバクテリオファージといいますが、そのバクテリオファージの遺伝子配列に部位特異的変異を導入して形質変化を調べる研究でした。1978年に学位を得ましたが、学位論文もそれがテーマでした。これはちょっと自慢なんですが、私の学位論文の表紙の体裁は、アインシュタインの学位論文の表紙と同じなんですよ。
岸本 へぇ、アインシュタインもチューリッヒ大学の出身でしたか。
谷口 ええ。あとレントゲンもそうです。そうした人物と同じ体裁の論文を作ったことが、私の密かな誇りなんです(笑)。
インターフェロン-βの遺伝子クローニングに成功
岸本 IFNにはどう着手なさったんですか。
谷口 こう言ってはなんですが、IFNの研究は、私の中では“おまけ”みたいなものだったんです。
岸本 ほぉ…。
谷口 学位論文ができあがる頃、ワイスマン先生が「バイオジェン」創業者の一人になりまして。「バイオジェンとして、IFNの研究をやりたい。帰国前にその手伝いをしてくれないか」とおっしゃったんです。それで、IFNの専門家だったエール大学のピーター・レンゲル先生に来てもらい、セミナーをしてもらいました。「ウイルス感染でIFNが出る。自然免疫においてIFNは重要だ」といった話をされていました。この話に興味をもったんですね。そこから、IFNに関心を抱くようになりました。
岸本 谷口先生がIFNの研究を始めたときはどんな状況でしたか。
谷口 ウイルス増殖が抑制される現象は知られていましたが、その実態やむろんIFNが誘導される仕組みは全くわかっていませんでした。それで、遺伝子を分離すればこれらの課題に取り組めると夢見たんです。
チューリッヒから日本での所属先だった癌研究所に帰ってくる頃、癌研究所からも「IFNはがんに効くと言われている。ぜひ研究を」と励まされ、研究を進めました。
岸本 ワイスマン先生はIFNの研究を続けており、長田重一先生(現・大阪大学免疫学フロンティア研究センター教授)もワイスマン先生の研究室で研究に加わったんですよね。ワイスマン先生たちとは、いわば競争関係になったんですか。
谷口 いえ、競争は避けたいと思いましたね。ワイスマン先生のほうは、後にIFN-αと呼ばれる白血球インターフェロンの研究をしていたので、私のほうは後にIFN-βとよばれる線維芽細胞インターフェロンに取り組むことにしたんです。
岸本 二つは異なるものとわかっていたんですか。
谷口 遺伝子構造まではわかっていませんでしたが、タンパク質がちがうらしいということはだいたいわかっていたんです。ぜひIFN-βの研究をやりたいと思って、東レの基礎研究所にいらした小林茂保先生にも相談したら、「おもしろい。細胞を供与してあげる」と言っていただきまして。
岸本 1979年にヒトIFN-β遺伝子のクローニングに成功したんですね。
谷口 はい。ある程度、遺伝子構造もわかったので、日本学士院の紀要に論文発表したんです。癌研究所のP3施設を使わせてもらい、日本で初めてヒト遺伝子のクローニングをさせてもらいました。
岸本 長田先生たちの発表が翌年の1980年になったんですよね。長田先生とお話したとき、「数か月の差だったけれど、年を跨いで1年の差みたいになった」と(笑)。
谷口 いまとなっては笑い話みたいなものですね。当時、長田先生とは「お互いうまくいってよかったね」と話し合っていました。それで、チューリッヒへ行って遺伝子を比べてみると、アミノ酸配列が166個である点など、似ていたんです。いま振り返ると、これがサイトカインファミリーの最初の例だったんだと思います。
岸本 ワイスマン先生たちといっしょに『ネイチャー』に論文を出されたんですね。
谷口 ええ。「レター」として投稿したら、「アーティクル」として掲載してくれて。大変ユニークなケースで思い出深いです。
インターロイキン-2の遺伝子クローニングにも成功
岸本 1983年には、インターロイキン2(IL-2)の遺伝子もクローニングされましたね。
谷口 はい。IFNの研究の決着がある程度ついた頃、ILが白血球間の情報伝達物質であるということで注目を浴びていまして。癌研究所にいたとき、味の素から共同研究をやらないかと提案を受けたんです。免疫の話に興味をもつようになっていたので、研究することになったんです。
岸本 当時、主役と注目されていたIL-2の遺伝子クローニングも谷口先生が先駆けて成功なさって。世界的にも「またタニグチがやったで」って雰囲気でした(笑)。
谷口 その年は国際免疫学会が京都で開催された年で、大勢の人が聴きに来てくれてありがたかったです。でも、IL-2を発見したのは私ではなく、それを発見した人がすごく立派だと思います。その後で、遺伝子を通して新しいコンセプトを生み出したかどうかっていうことが非常に大切で、畠山昌則さん(現・東京大学大学院医学系研究科教授)などは、IL-2の受容体をクローニングし、シグナル伝達を担うドメインがあることを発見しました。こうした業績はとても大切です。

谷口維紹氏
東京大学 名誉教授・東京大学生産技術研究所 特任教授
1948年、和歌山県生まれ。71年東京教育大学理学部卒業。72年ナポリ大学理学部ナポリ海洋研究所奨励研究員。78年チューリッヒ大学大学院博士課程終了後、(財)癌研究会癌研究所に入所。80年主任研究員、83年生化学部部長。84年大阪大学細胞工学センター教授。95年東京大学医学部教授、97年同大学院医学系研究科教授、2007年同研究科附属疾患生命工学センター長、12年同大学生産技術研究所特任教授。内閣府総合科学技術会議専門委員などを歴任。専門分野は免疫学。世界で初めてインターフェロン-β(IF-β)、またインターロイキン-2(IL-2)の遺伝子クローニングに成功。生体防御のメカニズムや細胞のがん化の解明に貢献する。受賞は野口英世記念医学賞、朝日賞、ロベルトコッホ賞、慶應医学賞、日本学士院賞、ペツコラー・米国癌学会癌研究賞、内藤記念科学振興賞ほか多数。文化功労者。米国科学アカデミー外国人会員。和歌山県有田川町名誉町民。趣味はクラシック音楽鑑賞、野球観戦(熱烈なタイガースファン)。
がん治療の免疫療法にも興味
岸本 谷口先生には、私どもの誘いで大阪大学の細胞工学センターに来ていただきました。当時は主にインターフェロン調節因子(IRF:Interferon Regulatory Factors)の研究をされていたんでしたね。
谷口 はい。1988年当時、細胞工学センターの大学院生だった宮本昌明さん(現・神戸大学大学院理学研究科准教授)が、IRF-1を見つけました。同じく原田久士さん(現・バージニア・コモンウェルス大学マッセイがんセンター)がIRF-2を見つけました。ファミリーだとわかったんです。その後、いろんな人たちの研究で、IRF-3以降があることもわかってきました。
岸本 いまIRFは1から9まで発見されていますが、生物学的にどれが最も重要な働きをしているんでしょう。
谷口 あえて言えば、3ですかね。Toll様受容体の下流で、ウイルス感染によって働きます。コンディショナル・ノックアウト・マウスの系を解析したところ、T細胞にも関連していそうだとわかってきましたし。
岸本 その後、僕は1991年になって阪大の医学部に移ったし、谷口先生は1995年に東京大学医学部に行かれた。
谷口 岸本先生にも「また東と西とで競争や」なんて言われましたよね(笑)。
誘ってくださった東大医学部の方々には熱意が感じられたし、私自身も医学部はそれまで身を置いたことがなく「どんな研究と教育ができるんだろう」とチャレンジ精神に火が付いたんですね。
岸本 そうでしたか。東大医学部では、どんな研究をされてきたんですか。
谷口 細胞工学センター時代から引き続き、IRFの研究を進めました。私たちだけの研究成果ではありませんが、ウイルス感染すると受容体経路の過程でIRFが活性化されて、IFNの転写がオンになるといった機序などもわかってきました。
岸本 後進の指導にも力をお入れになった。
谷口 ええ。ただ、「私の研究はこれだから、お前はこれをしろ」という感じでなく、その人のモチベーションを高めることが教員としての大切な役割とは思ったですね。例えば、後任となった高柳広さん(現・東京大学大学院医学系研究科教授)には、骨の研究をしてきたので、「骨と免疫の関係について研究したらどう。IFNとの関わりはおもしろいよ」とだけ言いました。
「自分は研究を徹底的にやる」とか、「自分は若い人を育てる」とか、科学での楽しみ方は人それぞれあると思うんです。それでいいんじゃないかと思っています。
岸本 うん。それで東大医学部は2012年に定年になられて……。
谷口 はい。いまは駒場の東大生産技術研究所で、炎症・免疫制御学社会連携研究部門の特任教授を務めています。
岸本 どんなことをされてるんですか。
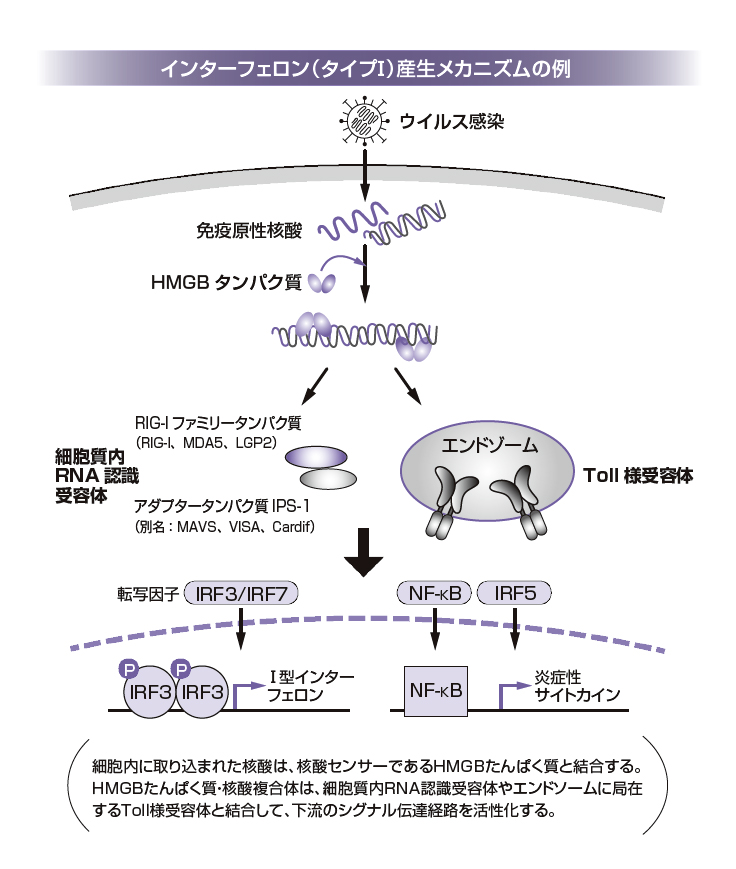
谷口 自己の細胞が出す分子がどのように免疫を活性化するかに大きな興味があって、その研究です。本来、免疫とは自己を認識して発達するものです。例えば、T細胞は胸腺の中で自己分子を認識して成熟し、外に出てきて、病原体などの非自己分子に強く反応するわけです。この関連で最近はHMG(High-Mobility Group)というタンパク質ファミリーに着目しています。細胞は死ぬと免疫を活性化しますが、その際、HMGB1(High-Mobility Group Box1)というタンパク質が細胞外に放出されます。これが敗血症などの病態を促進することに関係していたり、他の多くの病態に関係していたりすることがわかってきました。
岸本 免疫というのは、単に感染症を防御するといったことだけでなく、がんの増殖を抑えるといった役目でも中心的な存在だと思うんです。本庶佑先生(現・京都大学客員教授)が研究されてきた、T細胞活性化のブレーキをかけるPD-1(Programmed cell Death-1)遺伝子とかを含め、免疫はこれからも大事な分野だと思えますね。
谷口 そうですね。最近、話題になっている免疫チェックポイント療法も、免疫細胞にかけられたブレーキを外すものですし、免疫調整によるがん治療法の一つですね。
それと、個人的にはCAR-T(Chimeric antigen receptor T-cell : キメラ抗原受容体発現T細胞)療法も興味深いですね。この療法でT細胞が活性化すると、IFN-βがたくさん作られるそうです。一方で、IRF-7の経路をブロックすると、がんに効かなくなると言います。
岸本 先生の場合は効くほうとしてのインターフェロンへの興味ですね。僕の場合は、副作用としてショックが起こることがあり、IL-6が1000倍ほど出ると聞きます。それを抑える方法として、アクテムラとのコンビネーション療法が使われると。そういうことから、興味を持っています。
谷口 ああ、そうですか。昔はインターフェロンを投与すればがんが治るという単純な考え方でした。もちろん、それで治療できた人もいます。でも、実際はT細胞がローカルにインターフェロンを出すことががん抑制に効いているんじゃないかとも思っていて、そんな可能性もディスカッションしています。
免疫学は、これからも重要な分野であり続けると思います。幅が広くて、かつ奥が深い学問だな、と。
自分と違う価値観をもつ人と接してほしい
岸本 谷口先生は研究をしてきてよかったことはなんだと思いますか。
谷口 そうですね、一つは世界中に話し合える友人ができたこと。もう一つは、自分を追い越してくれる後輩がたくさん出てきたことですね。
岸本 谷口先生の人間関係が世界中に広がっているのに感心しますが、英語が上手で、海外の研究生活も長かったから……。
谷口 いえいえ、おそらくは田舎村の出身だったからですよ。村ではみんなが家族みたいな付き合いをしてましたから、誰とでも割合と気楽に入っていける点はあったのかなと思います。
岸本 いろんな人とのつながりは後々まで財産になりますね。いまは、日本の研究環境がよくなったからか、海外に行かない研究者も多くなったと聞きます。これは後に響いてくると思うんです。
谷口 そんな感じはしますね。自分と違う価値観をもつ人と接することで、自分を高めたり、いままでにない自分を見いだせたりできるという視点を、もうすこし大切に思ってもらえたらと思いますね。
岸本 うん。僕らの若い頃は、日本にいたのでは、1か月もしないと論文雑誌が届かないような時代だったから、外国に行かなければならなかった。当時に比べたら研究環境はよくなった気がするけれど、そういうことではないわけですね。
谷口 そうですね。われわれが細胞工学センター時代に楽しんでいたサイエンスと、いまのサイエンスを比べると、いまのほうが膨大化が進むとともに細分化もされてきたと思います。競争が激化し、科学が膨大化し、研究費を獲得するために細切れでもいいから論文を書いて予算を獲得しなければならない。
アメリカのハロルド・ヴァーマスとか有名な科学者たちが2014年、『PNAS』(全米科学アカデミー紀要)に、このままだとアメリカの医療・生命科学分野の研究はシステム的欠陥に行き着くという主旨の論文を出しましたが、日本でも似たようなことが言えると思うんですね。若い人たちに「夢をもって研究しろ」と言うのが難しい時代になりつつあるんじゃないかという気がします。
岸本 うん、それは研究費の配分のしかたとか、国の施策なんかにも関わってきますね。
谷口 ええ、そう思います。それで、ドイツのマックス・プランク協会と東京大学が設立した統合炎症学研究センターのセンター長をしている関係で、2015年の3月にアンゲラ・メルケル首相にお会いする機会があったのですが、「海外で勉強してきた経験から見て、日本の学問の強さと弱さはなんですか」って訊かれました。
岸本 なんと答えられたんですか。
谷口 強さがあるとしたら、日本の大学には人文・社会科学から自然科学まで広く学術と呼ばれて支援されてきたこと。一方、弱みのほうは、政府が予算の傾斜配分を強めていることとか、短期的な実利優先型になっているといったことですね。
岸本 うん、そうですね。
谷口 政治家しかリーダーシップをとれないところはありますが、一方で科学者だからこそ提起できる問題もあるわけです。科学者が積極的に、政治家や官僚の人たちに働きかけて新たな学問を作っていくといったしくみも大切で、それが国際平和にも貢献するのではないかといったこともメルケル首相に申しあげました。帰りの飛行機の中で「科学者との対談が有意義で楽しかった」と言われた、と後で大使館から聞かされましたので嬉しかったです。日本の学問も、科学者同士で「これではいかん」と言っているのでなく、社会の理解のようなものがもうすこしなければならないような気はしています。
岸本 今日はありがとうございました。
EYES
免疫システムで作用するサイトカインの代表的存在、 インターフェロンとインターロイキン
遺伝子のクローニングと機能の解明で免疫学と免疫療法が前進
私たちヒトなどの生体は、自己と非自己を識別して、非自己を排除しようとする免疫システムをもっています。そして、この免疫システムに関与する特定のタンパク質は、「サイトカイン」と総称されています。サイトカインはリンパ球(白血球の一種)などの細胞から放出され、おもに細胞間の情報伝達役を担うなどして、免疫細胞の活性化や機能抑制などに働いています。
現在サイトカインに分類されているタンパク質は数百種類にもなりますが、この多様さはおもに1950年代以降、研究者たちが生体内の物質やそのしくみを次々と発見してきた結果といえます。そして、そんなサイトカインの中でも代表的存在と位置づけられているのが、今回のEYESと対談の記事で登場する「インターフェロン(IF:Interferon)」や「インターロイキン(IL:Interleukin)」です。それぞれについて説明します。
まず、インターフェロンは、ウイルスなどに感染した細胞でつくられるサイトカインです。ウイルスの増殖を抑制するほか、抗腫瘍作用や獲得免疫の制御などの働きも示します。「インターフェロン」は「干渉する」を意味する英語“Interfere”にちなんでおり、1957年に英国のアリック・アイザックスとジーン・リンデマンが命名しました。ただし、この物質を発見したのは日本の長野泰一氏と小島保彦氏で、1954年のことです。両者は「ウイルス抑制因子」と呼んでいました。
インターフェロンについては当初、ウイルスの増殖を抑えるなどの役割が知られるだけでしたが、1970年代後半、インターフェロンの遺伝子が相次いでクローニング(単離および増幅)され、分子構造が明らかになってきました。今回の対談で登場していただく谷口維紹氏は1979年、線維芽細胞で産生されるインターフェロンの遺伝子をクローニングすることに成功しました。翌年の1980年には、谷口氏がチューリッヒ大学留学時代に師事していたチャールズ・ワイスマンと、彼の下で研究していた長田重一氏(現・大阪大学免疫学フロンティア研究センター教授)が、白血球で生産されるインターフェロンの遺伝子をクローニングしました。谷口氏と長田氏がそれぞれ同定したインターフェロンは、現在それぞれインターフェロン-β、インターフェロン-αと呼ばれています。これら研究成果は、インターフェロンの分子構造の解明だけでなく、謎の部分が多かったサイトカインの単一分子としての性質の解明にもつながるものとなりました。現在では、ヒトにおけるインターフェロンはαやβを含む多種からなるタイプI、γからなるタイプⅡ、λからなるタイプⅢに分類されています。
インターフェロン生産のしくみをめぐってはその後、1988年に谷口氏らのチームが、インターフェロン-βの遺伝子の発現調節領域に結合する転写因子を発見しました。これは、インターフェロン調節因子(IRF:Inteferon Regulatory Factor)と呼ばれ、現在ヒトではIRF-1からIRF-9までの9種類が存在することがわかっています。
次に、インターロイキンは、免疫システムで重要な役割を果たすT細胞やマクロファージの増殖や活性化、B細胞の分化といった様々な作用を示すサイトカインです。「インターロイキン」という言葉は、白血球同士での相互作用に働くという意味から、「間」を意味する接頭辞“inter-”と「白血球」を意味する“leukocyte”にちなんで命名されたとされています。
1979年に、スイスのエルマツィンゲンで開催された第2回国際リンフォカイン・ワークショップで研究者たちはインターロイキンの命名法を整理し、タンパク質として同定された順に1から番号を付けて呼ぶようになりました。現在、30種類以上のインターロイキンが知られています。このうち1983年には、後にインターロイキンとして初めて、インターロイキン-2と呼ばれる物質の遺伝子を谷口氏らの研究チームが分離することに成功しました。これを機に分子的なしくみの解明が進みました。現在、インターロイキン-2は、T細胞で産生され、T細胞の増殖と分化を促進することがわかっています。また、1986年には当財団の岸本忠三理事長が、炎症の促進に関わるインターロイキン-6の遺伝子を分離しています。
インターフェロンやインターロイキンをはじめとするサイトカインの研究は、免疫学やその応用としての医療を大きく発展させています。