LF対談
「どうして構造はそうなっているんだ」を
究めるのが自分の科学者としての使命なのだと思っています。 No.80(2017.2)

東京大学 分子細胞生物学研究所 教授
豊島近 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
タンパク質の結晶構造解析を確立するため米国そして英国へ
岸本 豊島先生は30年近く、カルシウムポンプ(Ca2+ポンプ)のご研究を続けてこられました。ご研究につながる第一歩はどんなものでしたか。
豊島 大学の物理学科3年生の時に夏休み学生実験というのがあって、江橋節郎先生の研究室に行き、英国留学から帰ってきた若林健之先生(現・帝京大学理工学部教授)にお会いしました。
そこで、電子顕微鏡で筋肉フィラメントの構造やそのカルシウムによる制御などが目で見えると。「これはすごいな」と思って、大学院に進みました。
岸本 その後、電子顕微鏡で膜タンパク質を見るため留学されたんですよね。
豊島 はい。スタンフォード大学のナイジェル・アンウィンの研究室に行きました。そのころ「氷包埋法」がまっとうに出来るのは、世界で1、2か所でした。試料を氷に埋めて染色せずに観察する技術です。
岸本 京都大学の藤吉好則先生(現・名古屋大学細胞生理学研究センター長)なども研究で使っていますよね。
豊島 そうです。まさにその技術の走りでした。そこでアセチルコリン受容体のチューブ状の結晶構造を解析する手法の開発を始めたんです。
岸本 その後、アメリカからイギリスのケンブリッジに移られたんですよね。
豊島 はい。ジェームズ・ワトソンやフランシス・クリックもいたMRC分子生物学研究所に行きました。せっかく開発できたチューブ状結晶構造の解析技術を他のタンパク質でも確かめたいといった思いがありました。
そんなとき、隣の研究室にいた米国人ポスドクのデビッド・ストークス(現・ニューヨーク大学教授)がCa2+ポンプのチューブ状結晶をもっていて、「よし、これを解析してみよう」となりました。それがCa2+ポンプの研究を始めたきっかけです。
脂質を含んだCa2+ポンプ 世界初の3次元結晶化
岸本 留学時期は1980年代後半あたりですよね。研究の状況はどうでしたか。
豊島 当時は膜タンパク質を結晶化するときは脂質は不均一だから除かなければならないというのが常識だったんです。高名なノーベル賞受賞者がそう主張していて。ところが、脂質を除いてしまうとCa2+ポンプの活性は無くなってしまいますから、そんなことできないのは明らかでした。
岸本 イオンポンプは脂質のなかに浮いているようなものなんでしょう。
豊島 そうなんです。結局、2000年に、脂質があってもX線結晶解析は可能であることを示せたのですが、脂質が存在する状況で膜タンパク質を3次元結晶化できたのは世界初でした。電子顕微鏡レベルの目茶目茶薄い3次元結晶を巨大化し、SPring-8の強力なX線で解析に成功したのです。成果は「ネイチャー」の表紙にもなり、「SPring-8から大きな成果」という見出しもついて、ちょっと驚きました。
岸本 豊島先生は2016年にスウェーデン王立科学アカデミーから「アミノフ賞」が贈られたのですよね。
豊島 まさにその受賞理由の1つが「リン脂質を利用した膜タンパク質の結晶化技術の開発」だったんです。
岸本 そもそもの話、どうして脂質が付いているタンパク質を結晶化できるんですか。
豊島 水の実効濃度を下げて、タンパク質が並ばないといられないという状況をつくってやるという基本は同じです。ですが、脂質は二重膜を作るわけですから、タンパク質の並び方には大きな制限がつきます。だから難しいんですね。タンパク質の並び方の自由度を下げるという意味ではプラスに働くはずなんですけど。

豊島近 氏
東京大学分子細胞生物学研究所 教授
1954年秋田県生まれ。78年東京大学理学部卒、83年同大学院理学系研究科物理学専攻博士課程終了。84年同大学理学部物理学教室助手、86年米国スタンフォード大学細胞生物学教室博士研究員、88年英国MRC分子生物学研究所研究員、89年理化学研究所・国際フロンティア研究員、90年東京工業大学理学部助教授を経て、94年より東京大学分子細胞生物学研究所教授。同研究所附属高難度蛋白質立体構造解析センター長。専門分野は構造生物学。2000年にイオンポンプタンパク質のX線結晶構造解析に世界で初めて成功。その後、カルシウムポンプとナトリウムポンプの反応中間体を次々と結晶化し、能動輸送機構の原子構造に基づく理解を可能にした。受賞は朝日賞、山崎貞一賞、紫綬褒章、上原賞、Gregori Aminoff賞、武田医学賞ほか。米国科学アカデミー外国人会員。
イオンポンプのしくみは「ポンプ」そのもの
岸本 Ca2+ポンプは実際どのような構造をしていて、どう働くのですか。イオンチャネルとのちがいは。
豊島 イオンチャネルは膜を貫通する“穴”なのですが、イオンポンプはまさにミクロの“ポンプ”なんです。イオンポンプには細胞質側と小胞体内腔側にそれぞれゲートがあって、細胞質側のゲートが閉まってから内腔側のゲートが開くことで、Ca2+を濃度勾配に関係なく細胞質側から内腔側へと輸送できるんです。その後、内腔側のゲートが閉まってから細胞質側のゲートが開いて、元の状態に戻ります。
岸本 ほぉ。細胞質側のゲートと内腔側のゲートが順に開いて、Ca2+が輸送されるという過程を、もうすこし詳しく説明していただくとどうなりますか。
豊島 ちょっと難しくなりますが、まず、細胞質の方から2個のCa2+がやって来てポンプタンパク質に結合します。これにより「細胞質側のゲートを閉めろ」というシグナルが送られます。それで、ATPの3つ目のリン酸がタンパク質に渡されます。その結果、Aドメイン(領域)という部分が傾きM1というヘリックス(らせん構造)が引っぱり上げられて、丸太でつっかえ棒されるみたいにゲートが閉められるのです。
岸本 内腔側のゲートのほうは……。
豊島 ポンプとして機能するための最小限の動きというのは、M4という2個目のCa2+を結合したヘリックスが内腔側に押し下げられ、Ca2+を押し出すことです。それが「ミクロのポンプ」と言ったことの意味なんですが、ここの機構は複雑です。先ほど、ATPの結合でAドメインが傾いてといいましたが、傾く結果、このドメインを回転させようという力が働くんですね。それでAドメインは実に110°も水平に回転します。その回転で、M4ヘリックスが組みこまれているPドメインが押し下げられ、M4ヘリックスも押し下げられ、というふうになります。信じられないくらい大きな構造変化です。内腔側には、細胞質側にあったつっかえ棒のようなものはありません。
岸本 とても複雑ですね。それと、そのように構造が変わっていくということは当然エネルギーが必要になりますね。エネルギーはどこからあたえられるのですか。
豊島 基本的に、ポンプを動かしているのは熱エネルギーです。
岸本 ATPがポンプを動かすエネルギーをあたえているのではないのですか。
豊島 そのように思われるのは当然だと思います。でもATPのエネルギーは単に“辻褄合わせ”をしているだけのようなのです。
岸本 辻褄合わせっていうのは……。
豊島 たとえば、細胞外のCa2+濃度は細胞内の1万倍にもなりますが、その差はATPの加水分解によって放出されるエネルギーがないと生じえないということです。イオンポンプという機械を動かすのは熱エネルギーだけれど、イオンの濃度差を保つためにはATPのエネルギーが必要なのです。
Ca2+ポンプとNa+/K+ポンプは似て非なるもの
岸本 豊島先生はCa2+ポンプのほか、ナトリウム-カリウムポンプ(Na+/K+ポンプ)の構造解析もしてこられました。この2つはかなりちがうのですか。
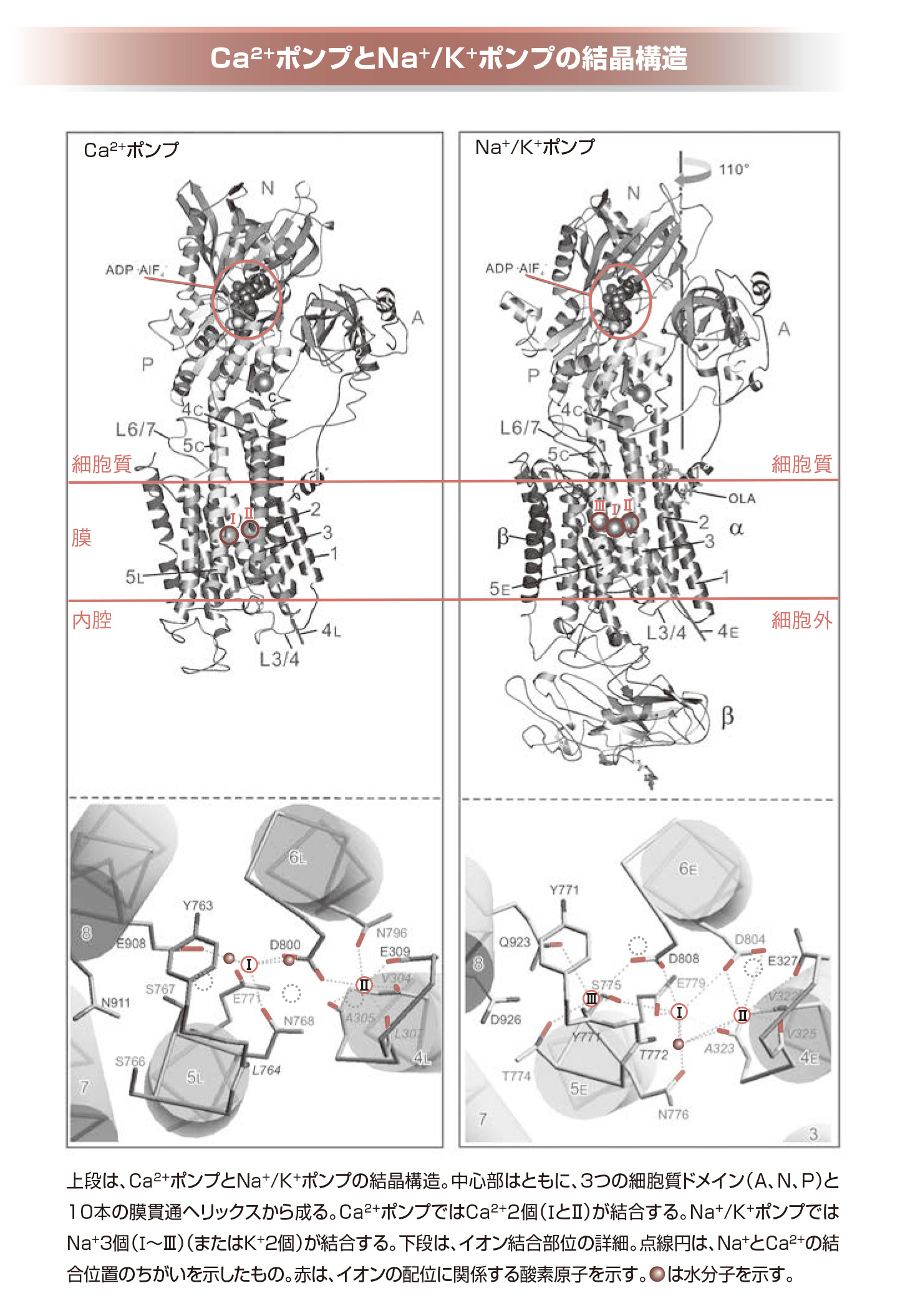
豊島 一見そっくりですよね(後述EYESの図版を参照)。でも、Ca2+ポンプでは2個のCa2+が結合するのに対して、Na+/K+ポンプでは3個のNa+がイオンタンパク質に結合するわけです。構造が解けるまではCa2+ポンプとNa+/K+ポンプのアミノ酸配列は似ているので、Ca2+もNa+も2個目まではほぼ同じように結合するのだろうとみんなが思っていました。きっとNa+の3個目のサイトだけが特別なのだろう、と。ところが、Ca2+ポンプとNa+/K+ポンプでは、まるでちがっていました。
岸本 どういうことですか。
豊島 Ca2+ポンプとNa+/K+ポンプとでは、それぞれのイオン、つまりCa2+またNa+の結合位置が大きくちがっていたんです。Ca2+ポンプについては、結合する2個のCa2+の位置は、M4、M5、M6と呼ぶ3つのヘリックスの真ん中あたりになります。ところが、Na+/K+ポンプでは、3個のNa+は、M5ヘリックス側に大きく寄っていて、しかも非常に近接して置かれていました。それには当然意味があるわけです。
大きさ、並び方、傾き イオン選択性の要素は多様
岸本 Na+/K+ポンプというのは、Na+もK+もどちらも扱うわけですか。
豊島 はい、そうです。
岸本 だとすると、Na+/K+ポンプでは、なにをもってして、Na+を扱うときとK+を扱うときに分けられるのですか。つまり選択性はどうやって生まれるのかと。
豊島 Na+/K+ポンプは本質的にNa+のポンプで、Na+を運ぶ方向には厳密にNa+だけを運びますが、逆方向にはK+だけでなくNa+や他の1価の陽イオンも運びます。Na+とK+の半径はほんの少し(0.3Å)しかちがわないのですが。
岸本 すると、イオンポンプによるイオンの選択性は、イオンの大きさのちがいによって生じるわけですか。
豊島 大きさは当然、選択性の要素になります。ですが、熱エネルギーでタンパク質は大きく揺らいでいるのでその差を見分けるのは難しいはずなんです。まずは揺らぎを減らす工夫が必要で、Na+の結合サイトがM5側に大きく寄っていたのはそのためです。でも、もっと大事そうなのは電気的な力です。3個のNa+がすごく近接して配置されていると言いました。その距離は、小さいNa+には良いけど、大きいK+には短すぎるのですね。つまり、個々のイオンの大きさを測るのは難しいけれど、2個、3個並べればうまく測れるというわけです。ですから、3個のNa+を運ぶのは効率のためだけではないんですね。でも、選択性を決める要素はそれだけではないんです。
岸本 まだほかにも要素がある、と。
豊島 そうなんです。3つあるNa+のうちの最初のもの(Ⅲ)は、M5ヘリックスの真ん中辺の、ヘリックスがほどけているところに結合するんです。そこは、K+が結合できなくもなさそうなのですが、正しい大きさのイオン、つまりNa+が結合しないと、M5ヘリックスの傾き具合がまずくて、2番目、3番目のNa+結合サイトが正しく形成されない。でもそれだけではなくて、3つある細胞質ドメインが正しい配置にならないのでリン酸化反応がすすまない、という仕掛けになっていたのです。何重もの仕掛けがあることがわかって感動しました。
岸本 選択性の要素はさまざまなのですね。
心筋Ca2+ポンプの制御機構 医療分野にも貢献したい
岸本 医療との関連では、どんな研究が進んでいるのですか。
豊島 重要な研究のひとつは、心筋のCa2+ポンプにおけるフォスフォランバンの機能解明です。フォスフォランバンはCa2+ポンプの作用を制御するタンパク質で、普段はポンプの作用をある程度だけ抑えるといった働きをしています。けれども、フォスフォランバンはリン酸化するとCa2+ポンプから外れ、その結果、心筋のCa2+ポンプはフル回転するようになります。つまり、フォスフォランバンのやっていることは、Ca2+ポンプがフル活動しなければならないときのために“ため”をつくっているようなものです。フォスフォランバンが発現しすぎて、Ca2+ポンプによるCa2+の出し入れがうまくいかなくなることが心不全になると起きると言われています。ですのでフォスフォランバンを結合できなくさせれば心筋でのCa2+の出し入れは正常になるわけです。
「じゃあ、どうやってフォスフォランバンはCa2+ポンプに結合しているんだ」というのが次に取り組むべき課題です。
岸本 豊島先生は基本的な原理を解明しつづけてきたから、応用的な研究についてはどう考えているのかなと思っていたんです。
豊島 基礎的な研究だけでいいとは思わないですね。もちろん、基礎は基礎で「自分がやらなかったらだれがやるんだ」と感じます。でも、やっぱり役に立つこともやりたいと思いますね。
構造の意味を考える研究
岸本 Ca2+ポンプやNa+/K+ポンプについての研究は豊島先生が独走状態ですか。
豊島 たしかに2004年ごろまでは独走していました。でも、いまはデンマークの研究グループと熾烈な競争を続けています。Na+/K+ポンプの研究のほうも同じような状況です。
岸本 先生のお話を聞いていると、しくみがみんなわかったような気になりますが、まだわからないことがあって競争が続いているわけですか。
豊島 ええ、そうです。ただし、デンマークの研究グループと私たちのグループでは、研究への心構えのようなものがかなりちがいます。たとえば論文の書き方でも、彼らは「こういう構造を解析できました」と書いて終わりです。私は本当のサイエンスはそこから先だと思うんですよね。「得られた構造にどういう意味があるのか」を考えないといけない。
岸本 それは、よく先生が、構造が見えても「わかった」とは言えないとおっしゃることですかね。
豊島 そのとおりです。彼らは「進化の過程によって、こういう構造になった」で済まそうとします。私は「どういう進化の圧力があったから、その構造になったのか」まで考えて解明していきたいと思うんです。
岸本 頭を使うということですか。
豊島 ええ、「どうして構造はこうなっているんだろう」と考え続けることです。たとえば、 Ca2+ポンプでは、2個目のCa2+の結合なしにはリン酸化は起こらないのですが、ではそのシグナルとは、つまりリン酸化反応の活性化シグナルとはなんだろうと何年も考えてきました。その答えがようやく見えてきたように思うんです。
岸本 何年も、ですか。どんなことを考えて、どんな答えが見えてきたんですか。
豊島 Ca2+ポンプはどうしてNa+を結合できないのだろう、と。2個目のCa2+をNa+に置き換えたら何が起こるのだろうと考えました。実験的に置き換えるのは無理ですが、量子化学計算で理論的に予想することはできます。それで実際に計算してみたら、予想に反して大きく壊れるわけではなくて、M4ヘリックスの傾きが変わったのです。驚いたことに、それはNa+/K+ポンプでまさに起こっていたことなんです。
では、どうしてそうなるのか。Ca2+を結合するために、Ca2+ポンプでは実に7個の酸素原子がCa2+を取り巻いています。この酸素原子は負の電荷を持っていますから、その間の反発があるわけで、Ca2+が結合してそれを中和するから構造が保てるわけです。Na+だと大きさはCa2+と一緒ですが、1価ですから反発の方が大きいんですね。D800のカルボキシル基の酸素とA305のカルボニル基の酸素の間の反発でM4が傾くんですね。
それでは、Na+もなかったらどうなるか。反発が大きすぎて、M4はCa2+を結合したときの位置には来れないはずなんです。そうすると、M4ヘリックスは細胞質ドメインの1つPドメインに組み込まれていますから、先ほどのNa+/K+ポンプの時と同じで、3つの細胞質ドメインは正しい配置をとれない。だからリン酸化反応は進まない、というわけです。なんだそんなこと当たり前じゃないか、という気になりますが。
岸本 先生がされているような、本質を究めていく研究が継続的に続けられるということが大事だと思います。
豊島 私も本当にそう思います。たった2つのタンパク質ですが、そこで見えてくるのは結局、タンパク質はこうやって動いているんだという共通原理です。それは構造に書いてあるはずなんです。自分の関心は、やはり「どうして構造はそうなっているんだ」にあります。それを究めるのが科学者としての自分の使命だと思っています。
岸本 今日はありがとうございました。
(2017年2月発行のLF News No.80に掲載)
EYES
濃度勾配に逆らうようにして運ばれていくイオン
その担い手「イオンポンプ」のしくみを詳細に解明
結晶構造解析技術を確立し、原子レベルの反応を3次元的に捉える
細胞の内側にも外側にも各種のイオンがあります。では、その濃度はというと、細胞の内外で大きくちがっています。たとえば、カルシウムイオン(Ca2+)では、細胞外の濃度は細胞内の1万倍ほど、またナトリウムイオン(Na+)ではおなじく30倍ほど高く、逆にカリウムイオン(K+)では細胞内が細胞外より20倍ほど高くなっています。こうしたイオンの濃度のちがいは、生体のエネルギー源として利用されたり、またイオンの流入が神経伝達に利用されるなどしています。つまり、細胞内外でイオン濃度にちがいがあることは、生物が生きる上でのとても大切な基盤といえるのです。
通常、イオンは濃度の高いほうから低いほうに流入します。この一方向のみでは濃度のちがいはなくなってしまうはず。そうならず、細胞の内外で各種イオンの濃度差がおおむね一定に保たれるのはどうしてでしょう。そこには、イオンが濃度の低いほうから高いほうへと濃度勾配に逆らうように運ばれるしくみがあるのです。
このしくみの担い手が、生体膜にある「イオンポンプ」とよばれるタンパク質群です。一般的に「ポンプ」とは水などを汲み上げて運ぶ機械を指しますが、イオンポンプはイオンを汲み上げて運ぶタンパク質でできた微小な機械といえます。
たとえば、Ca2+を濃度の低い細胞内(細胞質側)から濃度の高い細胞外(小胞体内腔側)へと汲み出すタンパク質群は「カルシウムポンプ(Ca2+ポンプ)」あるいは「Ca2+-ATPase(ATP水解酵素)」とよばれます。また、Na+やK+を汲み出すタンパク質群は「ナトリウム-カリウムポンプ(Na+/K+ポンプ)」あるいは「Na+/K+-ATPase」とよばれます。
Ca2+ポンプとNa+/K+ポンプには共通して、イオンが結合したあとに、アデノシン三リン酸(ATP)によりポンプタンパク質がリン酸化され、それがさらに分解されるというプロセスがあります。この一連のプロセスを通じて、イオンは濃度勾配に関係なくいつも一定の方向に運ばれます。
このような複雑なイオンポンプのしくみを詳細に解明しようと挑んできたのが、前述の対談に登場していただいた豊島近氏です。豊島氏は1980年代後半の留学時代、電子顕微鏡を用いてアセチルコリン受容体タンパク質のチューブ状結晶構造を3次元的に解析する技術を確立しました。
さらに、開発したチューブ状結晶構造解析技術の確認のため、新たな対象としたのがCa2+ポンプでした。電子顕微鏡での解析技術などを高める一方で、圧倒的に情報量の多いX線結晶解析に適した結晶化法の開発にも取り組みました。そして2000年、兵庫県にある大型放射光施設「SPring-8」にて、Ca2+ポンプの構造を原子レベルで明らかにしたのです。豊島氏はその後もCa2+ポンプ、さらにNa+/K+ポンプの反応サイクルの中間段階の各構造を相次いで決定し(LF News No.80表紙や上図の構造モデルはその一例)、これらイオンポンプの反応サイクルの全体像を示しました。
30年以上にわたり一貫してこれら2つのタンパク質の構造解析に取り組んだ豊島氏の貢献により、濃度勾配に逆らうようにしてイオンを運ぶ生体内ポンプのしくみが、原子構造に基づいて詳細に理解されるようになりました。また、イオンポンプは生命機能の維持に重要な役割をもっていることから、しくみの詳細な解明が医療応用につながるものと期待されており、豊島氏自身、医療応用を視野に入れた研究にも取り組んでいます。