LF対談
がんの分類は、臓器ごとから、
原因となる遺伝子ごとへと、移りつつあると思います No.81(2017.6)

東京大学大学院医学系研究科細胞情報学分野 教授
国立がん研究センター研究所 所長
間野博行 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
固形がんで初めて本質的な原因となる融合遺伝子を発見
岸本 間野先生のご研究について、なによりまずお話したいのは、白血病など血液のがんでしか起こらないと考えられていた染色体転座が、肺がんなどの固形がんでも起こることを発見されたということです。
発見に至る経緯はどんなものでしたか。
間野 最初のきっかけは、慢性骨髄性白血病の分子標的治療薬「グリベック®」の登場でした。私も血液内科医でしたので、この薬の登場で白血病治療が大きく変わったと驚いていました。
それで、「グリベック®に続け」といわんばかりに、分子標的治療薬の臨床試験が次々と行われたのですが、患者さんの予後を改善できず、ことごとく失敗したんですね。
なぜグリベック®だけ成功したのか。それは、この薬が標的としているBCR-ABLという融合遺伝子が、そのがんを起こしている本質的な原因だからです。それが無いとがんは生きていけないからです。「第2のグリベック®」を実現するには、このような本質的な原因遺伝子を見つけることが大事だと考えたんです。それを見つけるための方法として、レトロウイルスのcDNA発現ライブラリーシステムをつくりました。
岸本 間野先生が開発されたcDNAライブラリーシステムというのは、がんで発現しているがんの原因遺伝子をすべて拾い出すという発想によるものですね。
間野 はい。機能アッセイといいますが、がん組織から、がんを起こす能力をもつ遺伝子を直接採ってくるという発想です。ヒトがたくさん亡くなる肺がんをやろうと考え、大学院生に実験してもらったところ、不思議というか幸運にも、ALKが融合した遺伝子が見つかって。信じがたい気持ちでした。
岸本 染色体の転座が固形がんでも起こるというのは、画期的な発見だったと思います。
間野 ありがとうございます。血液内科医として、リンパ腫ではALKが転座することは知っていました。EML4-ALKを見つけたときは、「もし、肺がんでも転座するのなら、その患者さんたちの生活を変えられるような発見だろう」と思いました。その後、検証を重ねて、実際にALKの転座が肺がんで起きているとわかり、「よし行こう」となったんです。
岸本 その結果、がん治療の分子標的薬としてALK阻害剤ができたわけですね。薬が上市するまでの経緯はどうでしたか。
間野 ALK阻害剤の「クリゾチニブ」は、もともと、消化器がんの治療に向けてMETというチロシンキナーゼの阻害剤として開発されていたんです。
その臨床試験が行われていたころ、私どもが、肺がんの原因となるEML4-ALKを発見したと発表しました。そこで、クリゾチニブがALKのキナーゼ活性も阻害することを知っていたファイザーが肺がん患者に対して臨床試験を行いました。そうしたら、ものすごく効いたんです。以降、この薬はALK阻害剤と認識されるようになり、肺がんの分子標的治療薬の臨床試験が加速しました。
岸本 それが米国のFDA(Food and Drug Administration、食品医薬品局)で承認されたのですよね。けれども、日本では承認は遅れてしまった。
間野 はい。ALK阻害剤として肺がん治療の臨床試験がはじまったのは、米国のボストン、韓国のソウル、オーストラリアのメルボルン。日本は対象から外れていました。どうしても日本人の肺がんの患者を救いたいという一心で、EML4-ALKの有無を診断するボランティア事業を始めました。1000人ぐらいの患者さんのうち、40例ぐらいが陽性と診断され、ソウルの臨床試験に参加されました。そして奏効率100%で、みなさん帰国されました。半分ほどは若い方でした。
岸本 有名な話ですね。日本で見つけたのに、日本人の患者がソウルへ行って治療してもらったというのが。
間野 残念なんですが、当時は何とか救いたいという一心でした。
医者であることを最大限に活かせる研究がある
岸本 間野先生のご研究の歩みについてお聞きすると、まず東京大学で血液内科医になられましたね。
間野 はい。
岸本 その後、研究のほうにお力を入れられるようになったのだと思います。僕も最初は臨床医でしたが「同時に臨床と研究はできない」と、研究のほうに進みました。間野先生はどうでしたか。
間野 やっぱり、研究をしたいという気持ちは強かったんですね。
東大の血液内科医になってから、3年後の1989年にセントジュード小児研究病院生化学部門に留学しました。帰国してから、研究をやりたいと望んでいたところ、自治医科大学で研究をするポジションを探していただき、そこに移りました。
岸本 そうでしたか。間野先生はよく「よい研究をするには、よい医者でなければならない」と言っておられますね。僕もそれは思っていて、患者にちゃんと向き合っていたら「これはなんでだろうか」といった疑問や気付きが生じて、研究の糸口が生まれたような気がしているんです。
間野 そうですね。やっぱり、医者がおこなう研究には、医者しかできない強みがあると思うんですよね。「どうしてこの病気は若い人に多いのだろう」とか、そうした視点を研究に活かすことができます。それに「患者さんの病気を治したい」という気持ちも、強く続く研究のモチベーションになると思います。それらを最大限に活かせたほうがよいのだろうとは思いますね。
岸本 そもそも、なぜ間野先生は医者になろうとされたのですか。
間野 幼いころ、私は病気がちだったんですね。なので体のしくみについては子どものころから興味がありました。一方、ラジオとかアマチュア無線とかにも興味がありました。大学を選ぶときは、数学者になるか医者になるかが選択肢でした。やっぱり人を救えるような道がいいだろうと思い、医者の道を選んだんです。
岸本 血液内科がおもしろいな、と。
間野 そうです。病気のしくみを明らかにしたいという研究意欲のようなものはずっとあったので、臨床も研究もおもしろく取り組める科を選びたいと……。自分のなかでは、「神経内科か血液内科がおもしろいんじゃないか」と思っていました。神経内科のほうは遺伝病の原因遺伝子が同定され始めたころでしたし、血液内科のほうはサイトカインのシグナル伝達がわかりはじめていたころでしたから。最終的には、血液内科のほうがおもしろいと思ったんです。

間野博行 氏
東京大学大学院医学系研究科細胞情報学分野 教授
国立がん研究センター研究所 所長
1959年岡山県生まれ。84年東京大学医学部卒業、86年東京大学医学部第三内科に入局。89年米国セントジュード小児研究病院生化学部門に留学。92年東京大学医学部第三内科助手。94年より自治医科大学へ。分子生物学講座講師。2001年、同大学ゲノム機能研究部教授。13年東京大学大学院医学研究科へ、現在に至る。また、2016年より国立がん研究センター研究所所長にも就任、現在に至る。専門分野は、分子腫瘍学、がんゲノミクス、ゲノム医学。2007年に肺腺がんの細胞から肺がんの原因となるEML4-ALK融合遺伝子を発見、世界的に注目されるとともに、がん治療における分子標的治療の道を大きく切り拓く。受賞は、日本医師会医学賞、高松宮妃癌研究基金学術賞、武田医学賞、上原賞、持田記念学術賞、高峰記念第一三共賞、慶應医学賞、ベルツ賞。紫綬褒章受章。
人工知能を使ったゲノム医療で最適な治療法を見出す
岸本 自治医科大学に移られて、EML4-ALK融合遺伝子を発見され、以降、血液の癌や肺がんだけでなく、ほかの固形がんでも融合遺伝子が存在することが、間野先生の研究などによりわかってきたと聞きます。
間野 ええ。ALKはEML4と融合すると肺がんをつくるのですが、ALKがNPMという遺伝子と融合すると悪性リンパ腫をつくるし、VCLという遺伝子と融合すると腎髄質がんをつくるといったことがわかっています。がんについては遺伝子を調べないと最適な治療法を選べないというふうになってきているので、やはりEML4-ALK融合遺伝子の発見は、がんのゲノム医療が進むきっかけになったとは思うんですよね。
岸本 それでいまは東京大学で研究するとともに、2016年からは国立がん研究センター研究所の所長も務められていらっしゃいます。どんなことを目指しているんですか。
間野 ゲノム医療に向けた研究が世界で進んでいくなかで、日本があまりに立ち遅れているので、それをどうにかしなければと思っています。
岸本 日本は遅れていますか。
間野 圧倒的に遅れていますね。なんとかしなければと何年か前から言っていました。今回、がん研究センターにお声がけをいただいて、私の師の高久史麿先生からも「がんのゲノムの医療をやりなさい。そのためにがん研究センターに行きなさい」と言っていただき、研究所の所長を務めることになりました。
岸本 間野先生は、ゲノム医療では「人工知能の活用が必要」とおっしゃっていますね。人工知能を活用するというのは、どういうことでしょうか。
間野 ゲノム医療における人工知能の役割はいくつかありますが、すぐにでも必要なのは最適な薬または治療法を選ぶことです。
岸本 最近、人工知能を使って白血病のタイプを決定して治療に役立ったと話題になっていましたが、そういったものですか。
間野 そうですね。その事例では「IBM Watson」という人工知能が使われていましたが、ゲノム情報のデータベースを使うという意味では同様です。そうしたものを日本でがんのゲノム医療向けにつくる必要があると考えています。
岸本 がん研究センターでは、人工知能を使って統合的にがん医療をおこなうシステムのプロジェクトを始めたそうですね。
間野 はい。がんのゲノムでは変異がものすごく多いので、大きな知識データベースを活用するために人工知能を使い、対象のがんに対してどの薬が適応するのかを判断するといったシステムです。
EGFRというタンパク質の遺伝子の一部が変異すると、がん細胞の増殖のスイッチがオンの状態になりますが、その変異としてはエクソン19内欠失やL858R変異といったものが知られていました。ところが、調べていくと、EGFRの変異だけでも、最近では700種類以上のアミノ酸置換が見つかったんですね。そのうちどの変異がEGFR阻害剤の治療適応かといったことは、大きな知識データベースをもたないとわからないわけです。
一方で、PubMedなどの文献情報には膨大な文献データがあるので、だれかが「これは活性型の変異です」などと報告しているかもしれません。そこで人工知能によってそうした膨大な文献情報を自然言語処理し、最適な治療法を判断するといったシステムを日本でつくりたいと考えています。
岸本 もう一つのご所属の東京大学でも、間野先生たちがゲノム医療のプロジェクトを立ち上げたと。
間野 はい。東大のプロジェクトで「ターゲット遺伝子パネル解析システム」を開発しています。これは、一度のゲノム解析で発がんに関連する遺伝子を選び出し、それら遺伝子の異常を判別するシステムです。
岸本 各患者の変異の情報をすべて調べて、データを蓄積していくことが、ゲノム医療につながっていくわけですね。
間野 そうです。薬剤での治療が可能な病気については、変異情報をもとに最適な薬を使うようにします。一方、ターゲット遺伝子パネル解析で発がん原因となる遺伝子変異が見つからない患者さんには、全ゲノム解析や全トランスクリプトーム解析に移行することになると思います。
どちらにしても、それぞれの患者さんの遺伝子変異をパネル解析システムで調べて、そのデータベースをもっておけば、たとえ診断した時点では最適な薬剤がなくても、たとえば2年後には臨床試験が始まっている分子標的治療薬があるかもしれない。そんなシステムができればいいなと思っています。
今後、ターゲット遺伝子パネル解析システムが保険適用されることを見据えながら、知識データベースを参照することで治療選択に役立てられるようなインフラをつくっていきたいと考えています。
原因となる遺伝子ごとにがんが分類される時代へ
岸本 ゲノム医療のお話もしていただきましたが、それも含めた今後のがん治療やその研究についてお聞きしたいと思います。
間野 そうですね。いまもまだ、がん治療で分子標的治療薬が有効である患者さんは2、3割ほどでしかありません。大多数の人はいまも従来の抗がん剤などを使った化学療法をおこなわないといけない。やはり新しい治療法を開発していくことは大きな社会的使命だと思います。
岸本 最近のがん治療の大きな潮流をどう見ていますか。
間野 これまでのがんの分類は「どの臓器にできたがんか」や「どういう病類型をしているのか、例えば腺がんなのか扁平上皮がんなのかなど」で判断されるものでした。
一方で、お話したように、様々な臓器においてALKとほかの遺伝子が融合して、がんがつくられることがわかりました。同様に、他にもがんの本質的な原因となる遺伝子が解明されつつあります。ですので、今後は「ALKによって起こるがん」や「ABLによって起こるがん」といったように、原因となる遺伝子ごとにがんが分類される時代に入りつつあるのではと思っています。
ただし、グリベック®やALK阻害剤などの分子標的薬だけで、がんを全滅させるのはむずかしいだろうとも考えています。恐らくがんはどんながん種でも均質な細胞クローンの集合体ではありませんから、そのなかには増殖せず寝ているがんの幹細胞といえるような細胞もあり、ALK依存的には増殖しないので殺せないんですよね。ですので、その細胞の増殖状態に関わらないような治療方法とALK阻害剤のような分子標的薬を組み合わせることで、はじめてがんの根治を目指せるんじゃないかと考えています。
岸本 臓器や組織などを見る病理的診断をもとにしたがん治療から、ゲノム解析によるがん治療へと移っていくとすると、病理診断を行なう病理医の存在はどうなっていきますかね。
間野 病理医には、きっと「真実を見る」能力があると思っています。彼らがつくった診断基準が、ゲノムのプロファイルと完全に一致していたという事例はありますし、素晴らしいと思います。だから、例えば特定の病理系だけに絞ってがんを解析するという手法は有効な作戦だと思っています。
岸本 がんの免疫療法についてはいかがですか。抗PD-1抗体などの免疫チェックポイント阻害剤も使われ、話題になっていますが。
間野 抗PD-1抗体や抗CTLA-4抗体といった免疫チェックポイント阻害剤も素晴らしい薬剤です。これからのがん治療のなかで、中心的な柱のひとつになるのはまちがいないと思います。とくに、ほかの抗がん剤による治療とはちがう効き方をして、長期の治療効果も期待できるというのはとても魅力的です。
岸本 がんの新たなマーカーを探索する研究もすると言っておられますね。そういうことも大事なわけですね。
間野 非常に大事ですね。遺伝子変異の総数が多いがんに対しては、免疫チェックポイント阻害剤が効きやすいことがわかってきましたが、それでも奏効率はまだ7割程度です。患者さんに適切な治療法をちゃんと選べていないんですよね。さきほど申しあげたゲノム医療のシステムのなかには、ぜひがんの免疫療法に関するバイオマーカー探索の機能も入れなくてはならないと思っています。
岸本 将来、さまざまな研究が進み、ゲノム医療や人工知能も組み合わさり、「このがんにはこの治療法を」と判断できるようになれば、大部分のがんは治るでしょうか。
間野 そうなってほしいと思っています。
岸本 そういう方向に進んでいる、と。
間野 私が医者になったときとくらべて、はるかにその状況に近づいたと感じています。いま原因がわからずに効果的な薬が選べない7割の人に対して、がんの原因を見つけることが、今後のがん治療を進歩させるのに重要になると思っています。
現時点ではまだないような発想に基づいた研究も、かならず重要になってくると思います。そうした研究を担う若い人たちにも期待をしているところです。
岸本 お忙しいところ、今日はありがとうございました。
EYES
がんの本質的な原因となる融合遺伝子を発見
奏効率7割という画期的な肺がん治療薬が実現
膨大なデータから最適な治療法を見出す
がん治療は「ゲノム医療」の段階へ
細胞の増殖のアクセルが踏まれたままの状態にする遺伝子は「がん遺伝子」とよばれます。正常な細胞の増殖を司る遺伝子が突然変異により活性化され、がん遺伝子となって細胞をがん化させます。近年、がん遺伝子のなかでも、遺伝子異常の一種として、複数の遺伝子が連結されて生じる「融合遺伝子」をめぐる研究が進んでいます。そして、それを標的とした治療薬が、非常に高いがん治療の奏効率をもって、がん患者の命を救っています。
融合遺伝子は、染色体の一部が切断されて、おなじ染色体のほかの部分、あるいはほかの染色体に融合する「転座」という現象などによって生じます。融合遺伝子ががんの原因となる例としては、第22番染色体のBCR遺伝子に、第9番染色体のABL1遺伝子が転座してBCR-ABL1融合遺伝子がつくられ、これがもととなり血液がんの一種である慢性骨髄性白血病が起きることが知られていました。
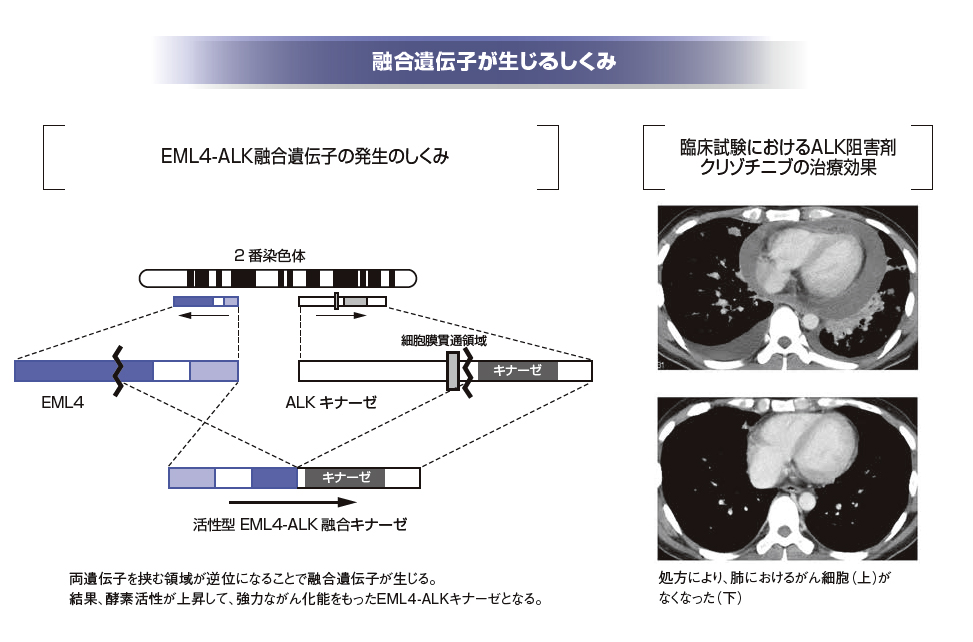
一方、先進国でもっとも死亡者数の多い固形腫瘍である肺がんの一部についても、がん化の原因となる融合遺伝子が世界で初めて発見されました。今回の対談記事に登場していただく間野博行氏は2007年、肺がんの一部では、2番染色体内で転座が生じ、微小管に会合するタンパク質をつくるEML4という遺伝子と、リン酸化酵素をつくるALKという遺伝子がつながった「EML4-ALK融合遺伝子」が生じていることを発見し『Nature』に発表しました。この成果を導いた手法は「cDNA発現スクリーニングシステム」を利用するもの。これは、個別患者のがん組織のmRNAから合成したcDNA(相補的DNA)を対象に質の高いcDNAライブラリーをつくり、細胞のがん化能を指標にがんの本質的な原因遺伝子を高感度に探索するシステムです。
ALKがEML4に融合した結果、がんが生じるのであれば、ALKのキナーゼ活性を阻害するような酵素阻害剤をつくることで細胞のがん化を抑制できるはずです。間野氏の研究成果を受け、製薬企業はその開発に取り組み、最初のALK阻害剤「クリゾチニブ」が2011年には米国で承認され、発売開始となりました(日本での承認は2012年)。ALK阻害剤のように、特定の分子を標的として、その機能を制御する治療薬を「分子標的薬」といいます。
ALK阻害剤の承認は、間野氏の研究成果からわずか4年という迅速さでした。これは目覚ましい治療効果が臨床試験で確かめられたためです。第1相と第2相の臨床試験では奏効率が7割にもなりました。従来の抗がん剤による肺がん治療の奏効率が2割前後であることからすると、ALK阻害剤の特効性がわかります。クリゾチニブの臨床試験では第3相は不要と判断され、スピード承認となったのです。その後、ALK阻害剤の第2世代も次々と開発・販売され、クリゾチニブに耐性をもった変異型ALKにも有効に作用しています。
間野氏の発見を機に、がんの直接的な原因となる融合遺伝子についての研究も進みました。リンパ腫の一部ではALKが5番染色体にあるNPMという遺伝子と融合していることや、腎髄質がんではALKがVCLという遺伝子と融合していることなどが報告されています。これらの成果は、がんを遺伝子で分類・診断する時代の幕開けを意味します。
さらに、各患者のゲノム解析結果を薬剤選択に役立てる「ゲノム医療」を、がん治療において確立するための取り組みが始まっています。患者のDNA配列を次世代シークエンサーにより解析することで、がんのゲノムデータを蓄積していきます。また、蓄積された膨大なゲノムデータや、過去のさまざまながん治療にかかわる研究成果の情報などをもとに、人工知能を用いて個々のがんに対する最適な治療法を見出そうとする研究も進んでいます。