LF対談
脳内における眠気の実体は、
驚くべきことに、まだなにもわかっていないんです No.82(2017.10)

文部科学省 世界トップレベル研究拠点プログラム
国際統合睡眠医科学研究機構 機構長・教授
柳沢正史 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
血管収縮作用をもつペプチド「エンドセリン」を発見
岸本 柳沢先生は、睡眠の研究を始めるずっと前の1987年に、血管収縮作用をもつエンドセリンというペプチドを発見されましたね。これは、どんな方法によってですか。松尾壽之先生(現・国立循環器病研究センター名誉所長)や寒川賢治先生(同研究所長)がいろいろなペプチドホルモンを発見されたときは、抽出物を熱処理などして、タンパク質分解酵素を壊してからペプチドを得ていましたが。
柳沢 エンドセリンについては、血管内皮細胞の培養上清から取ったんです。無血清培地なので、非常にクリーンなところから始められて、精製するのは比較的簡単だったんです。
岸本 エンドセリンを研究されていた時代は、筑波大学の医学部で眞崎知生先生(現・京都大学名誉教授)の研究室に所属していましたね。博士号もエンドセリンの研究でお取りになって。その後、アメリカに渡ってからも、しばらくはこの研究を続けられたんですね。
柳沢 はい、そうです。
岸本 でも「博士号を取った研究室の仕事をそのまま続けているようでは」とよく言いますよね。先生も、エンドセリンの後はオレキシンの研究に移られたわけで……。
柳沢 そうですね。エンドセリンについては、1995年ごろから多くの企業が拮抗薬を発表しはじめて、もうすぐ薬になるだろうという雰囲気がありました。「基礎研究では、最もおもしろい部分は終わったのかな」と感じました。それに研究者の数も増えましたが、私は“混んでいる”のも嫌いなもので、新しいことを始めようと考えるようになったんです。
最初に探し当てたリガンドがオレキシンだった
岸本 それで、柳沢先生はオレキシンを発見されました。どのような経緯でしたか。
柳沢 1995年から96年ごろ、EST(Expressed Sequence Tag:発現遺伝子配列断片)解析プロジェクトなどが盛んに行われているなかで、相手となるリガンドが不明なGタンパク質共役受容体が、次々と同定されつつあったんですね。そこに目を付けました。テキサス大学の私の研究室の隣に、デイビッド・マンゲルスドルフという男がいて、いつも「核内オーファン受容体がね」と口にしていたんです。
岸本 つまり、リガンドが同定されていない受容体のことですね。
柳沢 はい。「マサシもやらないか。おもしろいよ」と言うので、Gタンパク質共役受容体のことをすこし調べてみると、彼の研究している核内受容体とは異なり、嗅覚などの感覚関連の受容体を除いても400種類ほどあると知ったんです。
岸本 そんなにあるんですか。
柳沢 ええ。その半分ぐらいで、まだリガンドが見つかっていませんでした。「まずはリガンドを見つけることを目指そう。リガンドの機能解析は後でやればいい」と考えて、リガンドの探索を始めました。
それで、最初に見つかったのが、オレキシンだったんです。
岸本 そうだったんですか。オレキシンはどのように得られたんですか。
柳沢 ウシの視床下部とラットの全脳から抽出液をとり、液体クロマトグラフィーにかけて、という従来からの方法でした。
岸本 それで、見つけたオレキシンが、特定のGタンパク質共役受容体に結合することを突き止めたんですね。
柳沢 ええ、そうです。
夜間のマウスの行動変化からオレキシンと睡眠の関連性を解明
岸本 さっき「とりあえずは見つけることを目指して、機能解析は後で」と言っておられましたね。すると、その次はオレキシンの機能解析をされたんですね。
柳沢 そうです。
岸本 まずは、分泌される場所から機能を推測するといったアプローチでしょうかね。オレキシンを、ウシの視床下部などから抽出したと言っておられましたが……。
柳沢 ええ。基本的にはオレキシンは脳にしかないとわかりました。脳の中でも、産生ニューロンは外側視床下部という場所にしかないとわかったんです。
教科書を見ると「外側視床下部は食欲に関する部位」とあります。実際、マウスにオレキシンを脳室内投与してみたところ、摂食量が増えました。同時に、そのマウスを絶食させて空腹状態にすると、オレキシンmRNAの量も増えました。これらの結果から「オレキシンは食欲の因子かもしれない」と考えました。
岸本 そうしたことがあって、オレキシンは食欲にかかわるペプチドだと考えて、研究を進められたんですね、最初は。
柳沢 はい。それで、次の段階として当然ながらオレキシンのノックアウトマウスをつくりました。「普通に過ごさせていれば痩せてくるだろうし、高脂肪食をあたえても太らないだろう」と期待していました。
岸本 結果はどうなりましたか。
柳沢 オレキシンノックアウトマウスはむしろ太っていったんです。期待を裏切られました。「これは困った」と思いました。
それで、当時はというと、マウスが夜行性動物であるにもかかわらず、夜の行動を観察することはほとんどされていなかったんです。昼にマウスの実験をして、昼に観察をするだけ。でも、マウスの食事量を昼と夜で分けると、夜が9割と圧倒的なんです。だから、夜におけるマウスの摂食行動を見なければなりません。
そこで、赤外線カメラを入手しました。私は「赤外線カメラは高価だろう」と思っていたところが、ソニーが赤外線を使って暗闇でも撮れる民生用ビデオカメラを1台5万円くらいで売っていたんです。「こんなに安いのか」と購入して、夜間撮影を始めました。担当してくれたポスドクはアメリカ人の小児科医でしたが、“もの言わぬ赤ちゃん”ならぬ“もの言わぬマウス”の観察にも長けていました。
岸本 小児科医だから(笑)。
柳沢 そんな中である日、彼が学生とともに「なんか変なことが起きている。ちょっと見てくれ」と言ってきたんです。
岸本 マウスがバタッといくやつですか。
柳沢 そうです。はじめ私が見たときは、そんな明瞭にはマウスは倒れ込みませんでしたが、よく見ると、動きがやはり変でした。
そこから先は、もう鑑別診断でしたね。てんかんの可能性も除外できず、とにかく脳波は調べなければなりません。当時、マウスの脳波を測定できる研究室は、世界でも数か所しかなかったんです。でもラッキーなことに、テキサス大学にはマウスで睡眠を研究しているクリス・シントンという英国人の生理学者がいて、彼にマウスの脳波測定法を教わることができました。
岸本 オレキシンノックアウトマウスの脳波を調べて、どんなことがわかりましたか。
柳沢 覚醒中にレム睡眠が入り込むという、通常ではありえないことが起きているとわかりました。これは、とりもなおさずナルコレプシーとおなじ症状です。
もし、マウスが倒れ込む原因がてんかんだったら、てんかんは研究され尽くしているから論文を1報ぐらい書いてさっさと手を引こうと思っていました。ところが、蓋を開けてみると睡眠に関わることだったんです。オレキシンが欠乏することで、ナルコレプシーが起きるとわかってきました。
岸本 すると、次は論文づくりですかね。
柳沢 ええ。その論文については、じつは裏話があって。スタンフォード大学のエマニュエル・ミニョーという睡眠学者も昔から遺伝型ナルコレプシーのイヌの家系を研究していたんです。ミニョーは研究をどこまで進めているのだろうか、と。1999年のアメリカ睡眠学会に、マウスの脳波測定法を教えてくれたクリス・シントンが参加するというので、彼にミニョーの研究の進捗具合について探りを入れて来てくれと頼みました。学会で彼はミニョーを見つけると、私どものオレキシンノックアウトマウスの脳波データを見せて、さらに「僕のコラボレーターがこんなマウスをもっているんだが、どう思う」と聞いちゃったんです。
ミニョーは「これはナルコレプシーだ」とわかっただけでなく、「そのコラボレーターとは、オレキシンを発見したヤナギサワだ」と気づいたみたいです。すぐに彼の研究室のポスドクだった角谷寛さん(現・滋賀医科大学特任教授)に電話をして「いますぐオレキシンの受容体をシーケンシングしてくれ」と言ったらしいんです。やろうと思えば3日で答えが出ます。それで、彼らに、オレキシン受容体の遺伝子こそが、ナルコレプシーの遺伝をもたらすものだと知られてしまったんです。
岸本 そんなことがあったんですか。
柳沢 そういったことが起きているとはつゆ知らず、私たちは証拠をきちんと整えて論文にしようと、じっくり取り組んでいる最中でした。すると突然、『セル』の編集長だったベンジャミン・ルインから電話がかかってきました。
岸本 ルインですか。私も彼が編集長のころ、よく論文を投稿してましたよ。
柳沢 私も前年にオレキシン発見の論文を『セル』で発表していたので、ルインは私のことを知っていて「おまえが発見したペプチドが、ナルコレプシーと関係しているっていう論文が送られてきたんだが、おまえのところはこの研究をやっていないのか。やっていないならレフェリーになってくれ」と言うんです。私は「うちもやってる!」と言って電話を切り、スクランブル体制で論文をつくって投稿したんです。
岸本 ミニョーとおなじタイミングで掲載されたんですか。
柳沢 2週間あとでした。いま考えると、最初からミニョーとはコラボレーションすべきだったのかもしれません。

柳沢正史 氏
文部科学省 世界トップレベル研究拠点プログラム
国際統合睡眠医科学研究機構 機構長・教授
1960年東京生まれ。筑波大学大学院博士課程修了。大学院在学中だった87年に血管制御因子「エンドセリン」を発見。また、98年に睡眠・覚醒を制御する「オレキシン」を発見。91年テキサス大学サウスウェスタン医学センター准教授兼ハワード・ヒューズ医学研究所准研究員、96年同教授兼研究員。2001年科学技術振興機構の戦略的創造研究推進事業「ERATO」・柳沢オーファン受容体プロジェクト統括責任者。 10年に最先端研究開発支援プログラム(FIRST)に採択されたことを受け、筑波大学に研究室を開設。12年には世界トップレベル研究拠点プログラム(WPI)に採択され、国際統合睡眠医科学研究機構(IIIS)を設立、機構長に就任。米国科学アカデミー正会員。16年紫綬褒章
オレキシン受容体拮抗剤が不眠症の治療薬に
岸本 オレキシンをノックアウトしたマウスは、バタッと倒れ込んだ後に、どうしてまた起きて動き出すんですか。オレキシンは全く無いままなのに……。
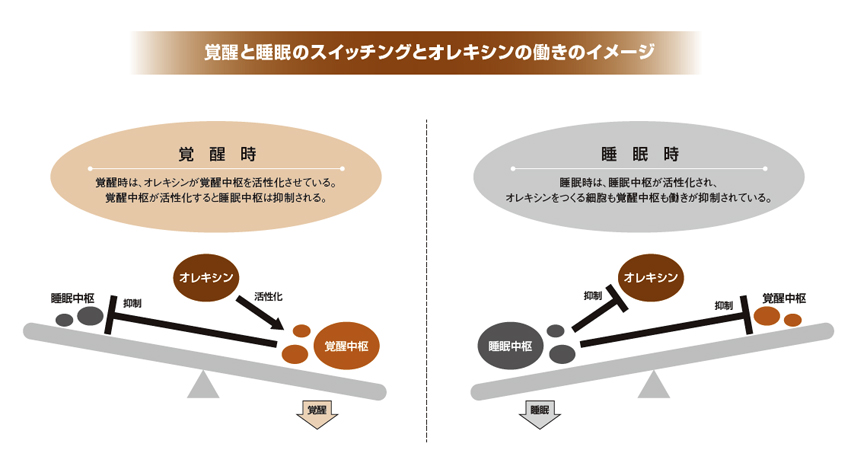
柳沢 そのスイッチがどう入っているのかは、いまだに明確には解明されていないんです。でも解釈は可能です。脳のなかに、覚醒と睡眠を切り替えるスイッチ役の神経細胞群が何ヶ所かにあり、それらが抑制しあうように神経回路を形成していて、シーソーのように睡眠か覚醒かのどちらかに傾くようになっているということだと思います。そのなかで、オレキシンは覚醒側に傾かせる機能をもちますが、それだけでなく、より大切なことに、シーソーの動きを安定化させる機能ももっているのだと解釈しています。
だから、オレキシンがなくなると、既存の覚醒と睡眠の切り替えスイッチが不安定になり、突然に眠ってしまうということになるのだと思います。ナルコレプシーの本態とは、睡眠と覚醒のスイッチングの不安定化なんです。
岸本 オレキシンは、ただ単に起こすだけのものではないということですね。
柳沢 はい。そういうことです。
岸本 オレキシンは覚醒と睡眠の切り替えを安定化させるとなると、そのしくみを利用した薬はどのようなものになりますか。
柳沢 オレキシン受容体の拮抗剤が不眠症の治療薬となっています。2014年から2015年にかけて日本とアメリカで相次いで承認されました。
岸本 そうなんですか。
柳沢 ええ。だけど、私はずっと「オレキシンからは、よい薬は生まれないだろう」と思っていたんです。
岸本 それは、どうして……。
柳沢 ナルコレプシーになってしまうと思ったからです。ナルコレプシーは単に眠くなるだけでなく、レム睡眠に特有な脱力発作などの困った症状も現れるので、「オレキシン受容体拮抗剤は、よい薬にはならないと思いますよ」と言ってきたんです。
ところが、アメリカのメルクやスイスのアクテリオン(現・ジョンソン&ジョンソン)が実験動物に拮抗剤を投与したところ、ナルコレプシーの症状が出ないらしいとわかってきたんです。メルクが大規模な治験を行い、承認に至りました。
岸本 だとすると、オレキシンが無い場合はナルコレプシーが起きるけれど、オレキシン受容体拮抗剤でオレキシンの働きを止めた場合は、かならずしもナルコレプシーは起きないということでしょうか。
柳沢 ええ。私の弟弟子にあたる名古屋大学の山中章弘さんがマウスで実験したところ、オレキシンを分泌する細胞の数が減っていくと眠気の症状は出てくるけれど、通常の約5%まで減らないとナルコレプシーの症状が起きないとわかりました。いま出ている拮抗剤は、眠気は誘発しても、ナルコレプシーの症状は出ない程度に効いているということなんだと思います。
スイッチが押されるしくみの謎に
フォワード・ジェネティクスで挑む
岸本 柳沢先生は何年、アメリカにおられたんですか。
柳沢 1991年から、24年いました。2010年からはアメリカと日本を行き来していましたが。
岸本 日本に戻られてきたのは、どういうきっかけで……。
柳沢 2009年のある日、ダラスにいたら、当時の筑波大学学長の山田信博先生から夜中に電話がかかってきました。「政府のFIRST(最先端研究開発支援)というプログラムが発表されたので、ぜひ筑波大学を研究拠点にして応募してくれないか」とおっしゃったのです。当時の私はアメリカにいてハッピーだったので、日本で腰を据えて研究する理由などなく「すみません、無理です」と返事しました。でも、ご熱心なことに、その後も夜な夜な電話がかかってきて、申請書類まで送られてきて、「研究内容の部分だけ埋めてください。事務手続きの部分は埋めておいたので」と。まぁ、倍率は高いようだし、受かるまいと思って、「応募だけはします」と伝えました。すると、本当に採択されてしまいました。 2009年の12月にFIRSTの研究室を開設し、実質的には2010年から始動しました。
岸本 FIRSTでどんな研究をされましたか。
柳沢 睡眠量が増えたり減ったりするような睡眠異常のあるマウスの家系を見つけてきて、そこから原因にあたる遺伝子変異を見つけることにしました。家系さえ見つかれば、原因遺伝子は短い期間で突き止められるだろうと。
岸本 「フォワード・ジェネティクス」という手法ですね。
柳沢 そうです。でも、突然変異の入ったマウスを数十や数百匹の規模で見ていても、睡眠異常の家系は出てこないので、数千匹のマウスをスクリーニングしました。毎週60から70匹の脳波を測定して、睡眠や覚醒の状態を調べて。それが大変でしたね。
岸本 その後、世界トップレベル研究拠点プログラム(WPI)にも採択されましたね。
柳沢 はい。結局FIRSTから足かけ6年、2016年の末にようやく1本目の論文を、WPIを受けて設立した国際統合睡眠医科学研究機構から出すことができました。
岸本 睡眠や覚醒に関わる新たな遺伝子が見つかってきたわけですね。
柳沢 ええ。オレキシンを発見して20年が経って、覚醒と睡眠を切り替えるスイッチの役割も理解できてきました。けれども、そのスイッチが「どんな指でどう押されるのか」については、白紙といってよいくらい未解明のままで来たんです。もちろん、眠気が起きればスイッチが睡眠側に押されるわけですが、では、脳内における眠気の実体はというと、驚くべきことに、まだなにもわかっていないんです。それが物質なのか、活動電位のパターンなのか、シナプス可塑性に関わるものなのかさえも……。
この部分を解明しないかぎり、睡眠学の課題は解決されません。まともな仮説を立てるとっかかりがない。だから、フォワード・ジェネティクスで探索研究をしたんです。
岸本 今後もご研究が進むことを祈っています。ありがとうございました。
EYES
眠気のしくみという“暗闇”に光が差す 覚醒・睡眠スイッチ、
そしてスイッチを押すしくみの解明へ
フォワード・ジェネティクスの手法で
睡眠異常の遺伝子変異を複数発見
私たちヒトを含む、脳を持つあらゆる動物が眠ります。睡眠中は無防備になるため敵に襲われるリスクが高い状態になります。それにもかかわらず、なぜ動物は眠るのでしょうか。その理由はわかっていません。
睡眠は人の生活に直結するものですから、現象としての解明は進んできました。睡眠を誘発する眠気については、眠らない時間が蓄積すると眠気が増していくという恒常性による制御と、夜が訪れると眠気が増すという体内時計による制御のふたつがおもに関与していることがわかっています。
しかしながら、眠気が生じている動物の脳では、どのような変化が起きているのかといった機構の解明は進んでいませんでした。睡眠が脳の一部でなく個体レベルでしか観察できない現象である点や、計測が困難である点などが理由にあります。
いま、“暗闇”ともいえる眠気のしくみに、光が当たり始めました。今回の対談で登場する柳沢正史氏、それに氏が拠点長をつとめる筑波大学国際統合睡眠医科学研究機構(IIIS : International Institute for Integrative Sleep Medicine)が、眠気の謎の解明に向けて研究を前進させています。
柳沢氏は、睡眠学の研究を開始する前、筑波大学大学院在学中だった1987年に、血管収縮作用をもつペプチド「エンドセリン」を発見するなど、早くも優れた研究成果を出していました。そして、米国で研究していた1996年、共同研究者の櫻井武氏(現・筑波大学 国際統合睡眠医科学研究機構 教授)と「オレキシン」というペプチドを発見しました。当初、食欲を制御するペプチドと捉えてオレキシンを研究していたところ、オレキシンをつくれなくさせたマウスが動きを突然やめて倒れ込む姿をビデオ撮影することができました。これを機に、柳沢氏らはオレキシンが睡眠にも関わる物質であると考え、研究を進めました。結果、オレキシンは覚醒を維持する働きがあるだけでなく、覚醒か睡眠かを決めるスイッチ役を果たすこと(図参照)、また、オレキシンが欠乏すると激しい眠気を催して眠ってしまう「ナルコレプシー」という睡眠障害の原因であることなどを発見しました。
2010年に、内閣府・最先端研究開発支援プログラム(FIRST)に採択されたことを受け、柳沢氏は筑波大学に研究室を開設。2012年には文部科学省世界トップレベル研究拠点プログラム(WPI)にも採択され、国際統合睡眠医科学研究機構(IIIS)を設立し、睡眠の制御の中心を担うような遺伝子の同定に取り組んでいます。
その手法が「フォワード・ジェネティクス」(順遺伝学)です。生物の形質に着目し、個体の表現型から、原因となる元の遺伝子や遺伝子変異を特定しようとする手法であり、特定の遺伝子を変異させて生体への影響を解析するリバース・ジェネティクス(逆遺伝学)に対してこう呼ばれます。具体的な手順は、エチルニトロソウレア(ENU)という遺伝子変異原性物質を用いてマウスにランダムな突然変異を誘発し、得られたマウスの脳波や筋電図を解析して睡眠異常を検出し、その睡眠異常マウスの家系から睡眠異常に関わる遺伝子変異を同定するというものです。IIISは2016年11月、覚醒時間が大幅に減少するSleepy変異家系からはSik3という遺伝子を、また、レム睡眠が著しく減少するDreamless変異家系からNalcnという遺伝子を同定したことを発表。研究成果は『Nature』に掲載されました。これらを含め、睡眠異常に関わる複数の遺伝子変異の同定に成功しています。
今後も、未知なる遺伝子変異が解明されていけば、睡眠・覚醒のスイッチを傾かせる要因など、睡眠をめぐる重要なメカニズムが明らかになっていくと期待されます。