LF対談
がんが中期まで進むと、TGF-βによる がんの進行促進作用は強くなります No.84(2018.6)

東京大学大学院 医学系研究科 分子病理学教授
宮園浩平 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
来日していた研究者の人柄に感激し、
スウェーデンで計8年間の留学を果たす
岸本 宮園先生と初めてお会いしたのは、スウェーデンだったんですよね。先生はウプサラ大学のカール・ヘルディン先生と日本で出会い、彼のお人柄に感激してウプサラ大学に留学されたわけですが、現地ではよくお会いしました。
そもそも、宮園先生のヘルディン先生との出会いはどんなものだったんですか。
宮園 1984年にヘルディンさんが来日していたとき、東京大学でセミナーが開かれることになりまして、私も参加しました。大々的な告知はされていなかったので、聴衆は私を含め5人ぐらいのセミナーでした。
とにかく、ヘルディンさんの正直で、まじめで、気さくなところにものすごく感激したんです。もう、その場で「スウェーデンで勉強させてもらいたい」と伝えて。なにもわからずあわてて渡航したものだから、お金も足りなくなり最初は10か月しかいられなかったんですが、その後また行って2年ほどいまして、さらに日本に戻ってから「研究室をもたせてやるから来い」と言っていただき、また5年ほどいまして。合わせて8年、スウェーデンにいたことになりますね。
岸本 ウプサラ大学は、首都のストックホルムから電車とかで1時間くらいのところにあって、昔から有名な研究者がたくさんいたんですよね。
宮園 はい。植物学のカール・フォン・リンネや、「摂氏」で知られるアンデルス・セルシウス、それに長さの単位にもなっているアンデルス・オングストロームなどですね。
岸本 向こうでの研究の進め方や体制は、日本でのものとずいぶんちがっていたとか……。
宮園 ええ。僕は夜中まで研究してもなかなか論文を出せずにいたのに、向こうの人たちはいわゆる「九時五時」にもかかわらず論文をたくさん出していて、「なぜそんなことが可能なんだろう」と本当に不思議に思ったんですね。わかったのは、いろいろなプロトコルがしっかりできていて、仕事を分担して本当に効率よくやっていたんです。男女平等だし、ワークシェアリングも徹底していました。
TGF-βやそのファミリーの受容体クローニング・同定に次々と成功
岸本 スウェーデンにいつ行っても「宮園さん、おるなぁ」と思ってよく会わせてもらっていましたけれど、スウェーデンと日本を行き帰りしていたんですね。でも、そうしているうちにだんだん、偉くなられていって(笑)。いまだれもが知っている先生の研究テーマとなったTGF-β(トランスフォーミング増殖因子-β)も、おもにスウェーデンにいた時期に研究を進めてこられたんですよね。
宮園 はい。当時ヘルディンさんはPDGF(血小板由来増殖因子)の研究で世界的に知られていて、PDGFの細胞増殖を促進する作用について研究をされていたのですが、その頃、TGF-βをめぐっては、細胞増殖を抑制する作用の重要さも言われるようになっていました。ヘルディンさんが「促進」についての研究をされていたので、僕は「抑制」のほうを中心に研究させてもらうことになったんです。それが1986年のことでした。
岸本 TGF-βの研究を始めて30年以上になるんですね。僕はよく「継続が創造を生む」と言っていて、自分もIL6(インターロイキン6)をずっと研究してきたけれど、先生もTGF-βの研究を長く続けて「TGF-βといえば宮園先生」と思われるようになりましたもんね。
宮園 ありがとうございます。
岸本 どんなところから着手されたんですか。
宮園 まずTGF-βが「潜在型」として作られることに注目して研究を始めました。潜在型TGF-βは活性をもたないのですが、それがどんな構造を持っていてどのように活性化するのかについて研究しました。そのしくみの解明は結構うまく行きました。
岸本 どんなしくみだったんですか。
宮園 TGF-βを「刀」に喩えると、通常その刀は「鞘」に収まったような状態になっていたんです。では、鞘はなにかというと、TGF-βのN末端側のLAP(Latency-Associated Peptide)という部分です。それにLTBP (Latent TGF-β Binding Protein)という大きなタンパク質が結合して複合体を作っていました。潜在型のTGF-βが活性化するのは「刀が鞘から抜かれる」ように、TGF-βがLAPから放出されることが必要でした。
それで、この研究が一段落ついた頃に、岸本先生が私どものところに来られて、「あんたら、レセプター(受容体)はなかなか取れませんなぁ。がんばってレセプターを取らなあかんで」と言われたんですよ。
岸本 そうでしたかな……(笑)。
宮園 はい。岸本先生からの叱咤激励もあって、1990年の終わり頃からTGF-βの受容体の研究をするようになったんです。
岸本 宮園先生もレセプターのクローニングに成功されたんですよね。先生をはじめ研究者たちは、どうやってクローニングしていったんでしょう。TGF-βの受容体にはⅠ型とⅡ型があると聞きますが、まず、どちらが先に見つかったんですか。
宮園 まず、Ⅱ型の受容体がエクスプレッションクローニング法でボストンのMITのグループによってとられました。
岸本 そのTGF-βのⅡ型の受容体は、多くの細胞増殖因子の受容体に見られるチロシンキナーゼ型ではなくて、セリン・スレオニンキナーゼ型だったんですよね。
宮園 そうです。当時、岸本先生は「チロシンキナーゼやったらおもしろないな」とよく言われていましたが(笑)。だから、違うものだったら面白いだろうなと。実際、セリン・スレオニンキナーゼ型だったので「これは、ちがう世界が開けてくるかな」と。
岸本 それで、I型の受容体については、宮園先生たちが最初にとられたんですよね……。
宮園 はい。当時、私たちはⅡ型の受容体に類似したものをとりあえずPCRでクローニングしていこうとして、結果、6つの候補が取れたので調べていました。すると、たまたまそのうちの1つが、TGF-βのI型の受容体であることがわかったんです。さらに、残りの候補の受容体も、TGF-βファミリーに属するアクチビンや骨形成因子(BMP:Bone Morphogenetic Protein)などのI型受容体であることが明らかとなりました。また、BMPのⅡ型受容体もクローニングすることができました。
TGF-βが受容体と結合したその先
Smadの解明にも貢献
岸本 TGF-βがⅡ型受容体に結合すると、Ⅰ型受容体が活性化する。すると、シグナル伝達の経路の先の段階へと進んで、今度はSmadというタンパク質の活性化などにつながっていくんですよね。
宮園 はい、そうです。
岸本 Smadの研究が進んだ頃の宮園先生のご活躍ぶりも、すごかったですよね。
宮園 ありがとうございます。ただ、Smadを単離・同定したのは私たちでなく、ショウジョウバエや線虫の研究をしていた人たちでした。私が日本に帰ってきた1995年のことですね。
Smadの研究についてはちょっと遅れをとってしまったので、「なんとかしないと」と思っていたところ、岸本先生たちが、SSI(Stat-induced Stat-Inhibitor)というのを発見されて『ネイチャー』に報告されたのを拝見したんです。1997年のことでしたかね。この論文を見て、「Statにより誘導されてStatでシグナル伝達を抑制するしくみがあるんだ」と思いまして。それで、私たちも「Smadにより誘導されてSmadでシグナル伝達を抑制するしくみ」を見つけることができて、約半年遅れで、そのSmadについて『ネイチャー』に報告することができたんです。
岸本 そんなことがあったんですね。いま、Smadは8種類あると聞きますが、宮園先生が見つけたそのSmadは何番目になるんですか。
宮園 Smad6ですね。一方、私が昔いたスウェーデンのグループは同じ頃にSmad7を見つけました。この2つのSmadは、シグナル伝達を抑制する働きなどの点で似ていることがわかりました。さらに東大分生研(現・定量生命科学研)のグループはショウジョウバエのSmad6の相同分子を発見されたので、いっしょに投稿し、1997年10月に同じタイミングで論文掲載となったんです。
岸本 それ以外のそれぞれのSmadには、どんな特徴があるんですか。
宮園 Smad2、3がTGF-βで活性化されるもので、1、5、8がBMPで活性化されるものだとわかっています。Smad4については、膵臓がん発症時に異常が見られる遺伝子から見つかったものです。
岸本そうした各種のSmadが複合体を作って、核へと移って、遺伝子の発現に作用するわけですよね……。そうした経路は、僕らが研究してきたStatとよく似ているなぁと思いますね。
宮園 私も本当にそう思います。

宮園浩平 氏
東京大学大学院 医学系研究科 分子病理学教授
1956年、佐賀県生まれ。81年東京大学医学部卒業、83年第3内科入局。血液内科学を専門として臨床に従事。85年より、Carl-Henrik Heldin氏に師事し、スウェーデン・ウプサラ大学ルードヴィヒ癌研究所で、のべ8年間の研究生活ののち、95年より癌研究会癌研究所生化学部部長。2000年より、東京大学大学院医学系研究科教授、11年より同研究科長・医学部長、現在に至る。専門分野は分子病理学、分子腫瘍学。がんの抑制と進展の両方に関与するタンパク質TGF-βや、TGF-βに類似した構造をもつ骨形成因子などを含む「TGF-βファミリー」の因子のシグナル伝達機構の研究などを行う。18年より日本学士院会員。受賞はベルツ賞、高松宮妃癌研究学術賞、井上学術賞、日本医師会医学賞、武田医学賞、紫綬褒章、藤原賞、日本学士院賞など。他に、ウプサラ大学Honorary Doctor of Medicine。12年よりAmerican Association for the Advancement of Science (AAAS) Fellow。
細胞増殖を抑制するし、がんの進行を促進もする……
TGF-βのもつ二面性の解明に挑む
岸本 宮園先生が長く携わってこられたTGF-βやSmadのことについてお話をうかがってきましたが、根本的な疑問もあります。それは「どうしてTGF-βが、細胞増殖を抑制させもするし、がんの進行を促進させもするのか」です。はじめは線維芽細胞の増殖を促進させるということでTGF-βが見つかったけれど、その後は細胞増殖を抑制することもあるとわかってきた。この疑問については解明されているんでしょうか。
宮園 たしかに、おっしゃった疑問については、わかりにくいところだと思います。いま私が考えているのは、大まかに言うと「TGF-βは、がんの初期には、がんの増殖を抑える働きをしているが、中期ぐらいになると、がんを進行させるはたらきが強くなる」ということです。
がんの進行では多くの場合、ご存知のように「上皮間葉転換」という現象が伴うことがわかっています。これは、上皮細胞が間葉系細胞に分化することを指し、これにより間葉系細胞がどんどん浸潤していき、がんが進行するというものですね。
じつは、がん進行につながる上皮間葉転換を、ある状況においてTGF-βが強く引き起こすということがわかったんです。
岸本 それは、どんな……。
宮園 例えば、膵臓がんですと、初期にrasというがん遺伝子の点突然変異がよく起こり、rasが活性化されますよね。そうすると、TGF-βが上皮間葉細胞転換を強く起こすようになるんです。つまり、だんだんとTGF-βのがん細胞増殖抑制作用が隠れていき、逆にTGF-βのがん進行促進作用のほうが強くなっていくというわけです。
岸本 けれども、TGF-βが受容体と結びついて、Smadを活性化させるといったシグナル情報伝達の経路は変わらないんですよね。
宮園 ええ。Smadが活性化されることは変わりません。
岸本 そうであれば、どうしてTGF-βが、よい働きをしたり、悪い働きをしたりするのか……。
宮園 それは、がん遺伝子などの信号が横から入ってくると、悪いことを始めるといったことなんだと思っています。いわば、善いことをしていた人も、脇に“悪い人”が現れると影響されて悪いことをしてしまうようなものと言えばいいでしょうか。
がんの進行では上皮間葉転換が伴うと言いましたが、SnailやSlugといった転写因子の発現上昇が上皮間葉転換には重要とされています。がん遺伝子rasの信号が脇から入ってくると、Smadが影響を受けてSnailやSlugの発現を促すようになるといったことがわかってきたんですね。
TGF-βの知見を臨床応用に、研究は続く
岸本 宮園先生は、スウェーデンから帰ってきてからは、癌研究会癌研究所の生化学部長をつとめ、そして東京大学に移られて、いまは医学部長をなさっていますね。研究との両立はできていますか。
宮園 なかなか難しいところもありますが、土曜・日曜や朝晩はなるべく研究のことを考える時間に充てさせてもらっています。なるべく時間をつくって、研究も行おうとしています。
岸本 医学部長の仕事で忙しくて、TGF-βのことを忘れかけたりは……。
宮園 じつは、数年前にカリフォルニア大学のリック・デリンク教授とともに編集した本が『The Biology of the TGF-Beta Family』という書名で改訂されて、2人で全章を3回ほど通して読んだんです。それで再度、しっかりと勉強することができました。
岸本 そうですか。僕も、大阪大学の総長をしていたから、そうした役職を務め終えたら、また研究者に戻れるということを身をもって実感します。日経新聞の「私の履歴書」で「総長を辞めたらまた研究者」といった記述があって、「研究やらないわけにはいかん」とも思って研究を続けているんですけれどね。
宮園 私も研究は続けていきます。
岸本 TGF-βの研究成果を病気の治療に活かすような研究については、いかがですか。
宮園 いろいろな企業が挑んでいるところですが、副作用があるようですね。ただし、がんの治療については、TGF-β阻害剤と免疫チェックポイント療法を併用すると高い効果が得られるのではないかということで、特異的にTGF-β阻害活性が患部で作用する薬剤の研究がさかんに進められているところです。私はちょっと出遅れてしまっていますが。
岸本 僕が研究してきたIL6は、いろんな作用があるのに、運もよくて、関節リウマチなどの治療薬になったものだけれど……。
宮園 本当にそうですね。IL6阻害剤には重い副作用がないということで、私もびっくりしました。
岸本 TGF-βについては、レセプターもシグナル伝達経路も解明されているのに、なかなか臨床応用につながらない。まだ研究すべきことがたくさんあるわけですね。
宮園 はい、そう思います。TGF-βのレセプターやシグナル自体でなく、そのターゲットとなる遺伝子かなにかで、うまく応用につなげられないかと思っています。免疫との関係などがわかってくればおもしろいかもしれないな、と。
岸本 TGF-βと病気の関係性については見つかってきているんですか。
宮園 直近では今年2月、『ネイチャー・ジェネティクス』に、TGF-βの遺伝子に異常があると、免疫抑制作用がうまく働かず、出生後に重篤な炎症性腸疾患が起こるというような論文が出ました。
それと、私たちは潜在型TGF-βの複合体に含まれるタンパク質LTBPを見つけたのですが、そのタンパク質が、結合組織が脆弱なために全身障害が生じる「マルファン症候群」という遺伝性疾患の原因遺伝子ととてもよく似ていたんです。この病気で動脈瘤ができるのは、TGF-βの作用を制御できないためだとわかってきました。TGF-βのシグナルを制御することで、マルファン症候群や動脈瘤の治療に応用できないかという研究もされています。
岸本 東大医学部には、研究志向の若い人はたくさんいますか。
宮園 清水孝雄先生が前任で医学部長をされていた時代から、「MD研究者育成プログラム」というのを組んでいまして、研究者をめざす学生たちに、さまざまな研究室での経験をさせて、英語の卒業論文を書かせるといったことをしています。学年で10人ぐらい参加していますが、中には論文が神経系の雑誌の表紙を飾ったような、優秀な学生もいますね。
岸本 先生の教室にも、若い人はいますか。
宮園 あと4年したら定年となるので、昔のように多くの若い人は来なくなりましたが、いまいる研究室のメンバーで楽しんでいます。
岸本 これからも、医学部長として、そして研究者として、ご活躍なさることを祈っています。ありがとうございました。
EYES
細胞の形質転換、増殖抑制、浸潤・転移促進……
さまざまな作用をもたらすTGF-β
情報伝達のしくみを解明
がん治療などの臨床応用を視野に
私たちヒトを含む生物は、さまざまな環境に適応するため、体内に「情報伝達」のしくみをもっています。生体内では、いくつもの種類のタンパク質などが連鎖的に作用することによって、必要な情報伝達が行われています。
たとえば、細胞膜の表面にある受容体というタンパク質に特定の分子が結合すると、情報伝達のためのスイッチが「オン」になります。すると、それを受けて、ほかのタンパク質が活性化したり、タンパク質を構成する分子がほかの分子と結合したりします。こうした作用をいくつも経て、最終的には、特定の遺伝子の発現が調節されるなどして、情報伝達が完了します。
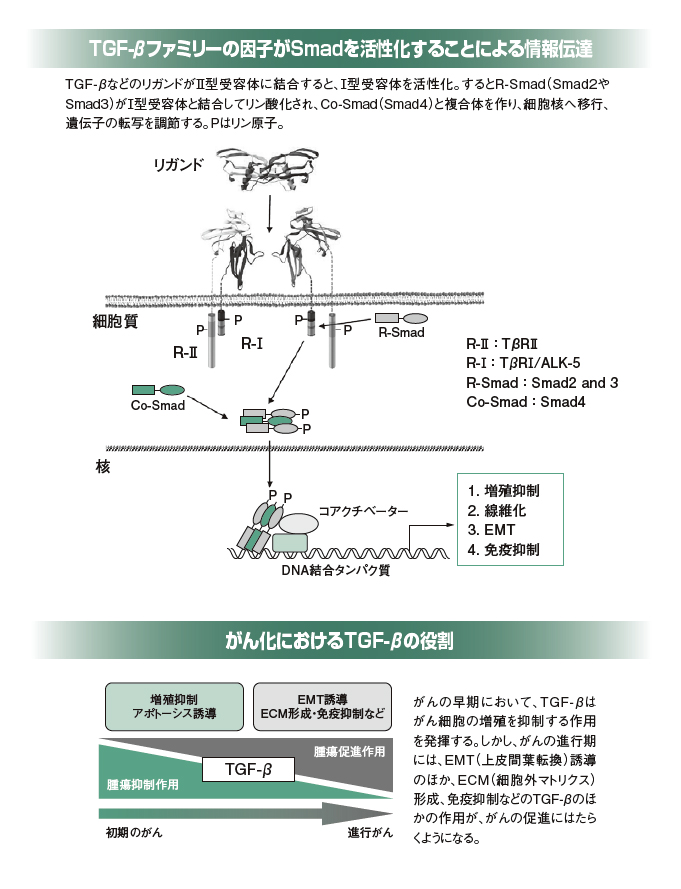
生体内での情報伝達の担い手の一つに「TGF-β」(Transforming Growth Factor-β)というサイトカインのタンパク質があります。TGF-βが、Ⅱ型とⅠ型という2種類の受容体と結びつくと、Ⅱ型受容体がⅠ型受容体をリン酸化し、さらにこのリン酸化されたI型受容体が、「Smad」とよばれる別のタンパク質をリン酸化します。Smadには8種類がありますが、Smad2または3が、Smad4と三量体を形成すると、それが核内に移動して転写因子と結合し、特定の遺伝子の発現を調節するのです。
TGF-βは1980年代、細胞の形質転換を促進する因子として発見されました。“Transforming Growth Factor”の名が付くのはそのためです。しかし、1985年になると、TGF-βが上皮細胞などの細胞の増殖を抑制する因子でもあることが明らかになりました。さらにそれだけではなく、1990年代には、進行したがんでTGF-βががん細胞の浸潤・転移を促進する因子として働くことも明らかになっているのです。
さまざまな作用をもつTGF-βに対して、構造やしくみの解明などの研究で貢献してきたのが、今回の対談に登場する宮園浩平氏です。
宮園氏は、1985年からのスウェーデン留学時代にTGF-βの研究に着手。まず、1988年に「潜在型」とよばれるTGF-βの複合体の構造を解明しました。その後はTGF-βのⅠ型受容体の遺伝子ファミリーや、「TGF-βファミリー」とよばれる分子群に属する骨形成タンパク質(BMP:Bone Morphogenetic Protein)のⅡ型受容体を発見しました。さらに、上述のSmadについても、シグナルを伝える「R-Smad」、そのR-Smadと複合体を作る「Co-Smad」、これらのシグナル伝達をするSmadに抑制的に作用する「I-Smad」の3つのタイプに分類することを提唱。自らもI-Smadの一つであるSmad6を発見しています。
また、宮園氏はTGF-βががん細胞を浸潤・転移させるしくみの解明にも挑みました。その結果、TGF-βが上皮細胞に作用して、上皮細胞のがん化の発端となる「上皮間葉転換」という現象が重要であることなどを解明したのです。
いま、多くの研究者や企業が、TGF-βのしくみを創薬をはじめとする病気の治療に応用するための研究を進めています。宮園氏はひきつづきTGF-βの多彩な作用の解明に向けての研究を進めており、臨床応用に結びつく研究成果にも期待が集まっています。