LF対談
Musashiから再生医療、
創薬まで つながっていると思っています No.86(2019.2)

慶應義塾大学 医学部生理学教室 教授
岡野栄之 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
Musashiの発見からヒトの神経再生能力の発見へ
岸本 先生には、2002年5月の『LFニュース』第36号で、当時の理事長だった故・岡田善雄先生と対談をしていただいたことがあります。
岡野 そうでした。もう15年以上も前になるのですね。今回、岸本先生にもお声がけいただき光栄です。
岸本 岡野先生は1985年からの約7年間と、1997年からの4年間、大阪大学で研究されていました。僕が阪大の総長をつとめていたときは、先生が阪大からべつのところへ移りそうなご様子で、「また東大に行くとなったらどないしよう」などと思っていましたが、慶應の塚田裕三先生の教室へ移られるとのこと。「そうか、岡野さん、出身校に戻るんやな。名門やしそれはしょうがないな」と見送った覚えがあります(笑)。
岡野先生といえば、Musashiの発見がまっさきに思い浮かびます。どういう経緯で見つけられたんですか。
岡野 私が、はじめに大阪大学にいたとき、御子柴克彦先生のもとでおこなっていた研究が原点にあります。マウスを使って神経系の研究をしていましたが、より強力な遺伝学的手法で新しい歴史を見つけていきたいと考えていました。当時はマウスの遺伝子をノックアウトする方法がまだまだ難しく、新たな遺伝子を見つけていくにはショウジョウバエか線虫しかないと思っていました。脳があるということでショウジョウバエで神経系に重要な役割を果たしている遺伝子をクローニングしようと思い、留学先のジョンズ・ホプキンス大学で、ショウジョウバエの遺伝学的手法を学んで、神経系に異常を示す変異体を取りました。それがRNA結合タンパク質をコードしている遺伝子、musashiの変異体で、遺伝子産物までたどり着いたのが1991年のことでした。
岸本 そうでしたか。「Musashi」という呼び名は、宮本武蔵にちなんだものと聞きますが、どういった意味を込めて……。
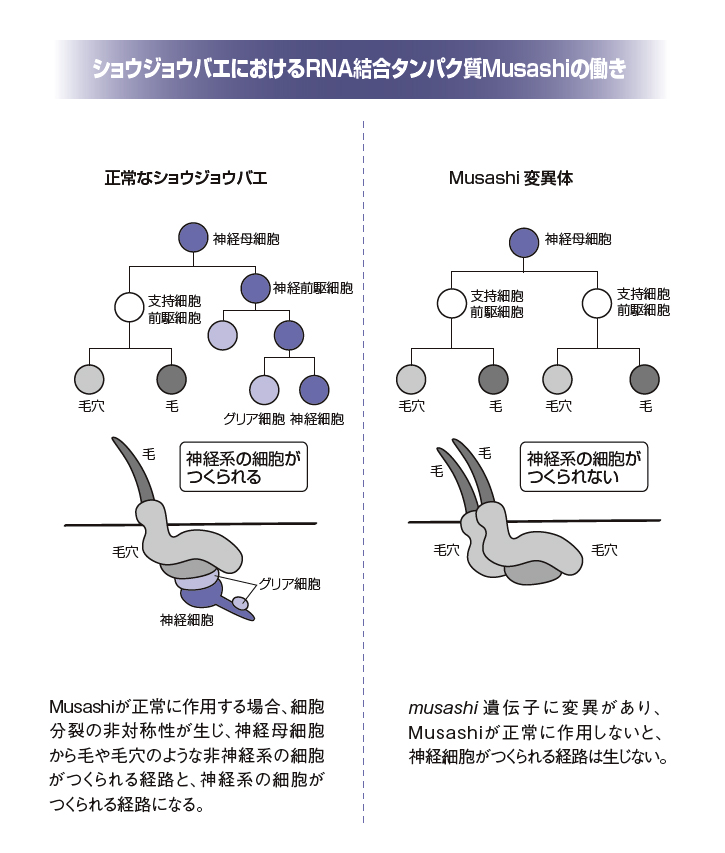
岡野 「毛が2本になる」ということから「二刀流」だ、ということで「Musashi」と名付けました。本来、ショウジョウバエの感覚受容器では1つの毛穴から1本の毛が生えますが、musashi遺伝子に変異があると、毛がもう1本生えてくるなどします。神経細胞やグリア細胞に分化していくはずの細胞がそうならず、分化転換して毛になるからです。それで毛が2本で二刀流ということで、「Musashi」だ、と。
岸本 なるほど。そうすると、変異体でない正常のMusashiは、神経に分化していく前駆細胞に発現しているわけですか。
岡野 ええ、そうです。ふだんMusashiは、神経系になる細胞において、tramtrackという神経系細胞の分化を抑制する転写抑制因子のmRNAと結合し、その翻訳を抑制しています。ですのでMusashiが正常に働けば、その転写抑制因子が発現してこなくなり、その細胞は神経系の細胞になっていきます。ところが変異体では、Musashiが正常に働かないため、転写抑制因子tramtrackが異所性に発現し、本来なら神経系の細胞になっていくはずの細胞の分化が阻害され、毛になってしまいます。
結局これは、musashi遺伝子にコードされたRNA結合タンパク質が、翻訳調節を介することで、非対称性分裂を制御しているということになります。この結果を『ネイチャー』で発表したところ、興味深く思ってもらえて、いろんな教科書に載るようになりました。
岸本 Musashiを発現する幹細胞は、ショウジョウバエだけでなく、他の生物にも存在するんですね。マウスとか、ヒトとかでも……。
岡野 そうなんです。MusashiとそっくりのRNA結合タンパク質が哺乳類にもあって、やはり神経の幹細胞で発現していることがわかりました。まず、マウスの成体脳にMusashiを発現する幹細胞があることを1997年に発表し、ついで1998年にヒトの大人の脳でも同様であることを見出だせました。
岸本 Musashiが神経幹細胞で発現するということは、逆にいうとMusashiの存在が神経幹細胞の存在を示すマーカーにもなりうる、というわけですかね。
岡野 そうです。ですから、これまで再生能力がないと思われていたヒトの脳にもじつは幹細胞があるのだという発見になりました。さらに「ということは、その眠っている幹細胞を神経の再生に利用できるかもしれない」と考えまして。ヒトの大人の脳にもMusashiが発現することを発表してからは、基礎的な研究だけでなく応用面もやっていこうと考えるようになりました。
脊髄損傷の再生医療臨床研究が間近に
岸本 そこから岡野先生は、神経細胞を再生させて脊髄損傷などの患者さんを治療する研究も進めていったわけですね。
岡野 はい。インターロイキン6を発見された岸本先生が、さらに薬の開発につながる研究もされているお姿を見ていて、「自分たちがしてきた基礎研究を人の役に立つようにするのも大事なことだ」と思いました。
岸本 そうでしたか。その後、ES細胞や、新たにつくられたiPS細胞をもとに神経幹細胞をつくり、それを患者さんに入れて、脊髄損傷などの病気を治そうとされてきたわけですね。治療に向けた研究の進み具合はいかがですか。
岡野 じつは、ちょうど今週(2018年11月下旬)、iPS細胞を使った脊髄損傷の患者さんへの初の臨床研究が、慶應義塾内の特定認定再生医療等委員会から承認を受けたところです。2019年には、厚生労働省の厚生科学審議会での承認を経て、患者さんに実際に投与される段階に進んでいくと思います。
岸本 そうですか。どんな臨床研究をされる予定ですか。
岡野 その臨床研究は、損傷して2〜4週間の亜急性期の患者さんを対象とするものです。iPS細胞から誘導した神経幹細胞を、脊髄の損傷した部位に移植します。
岸本 そうしたら、神経がつながっていくわけですか。どのようなメカニズムで……。
岡野 ええ。脊髄損傷ですと、胸の高さあたりの脊髄で、脳からの神経線維が途切れているのですが、そこに神経幹細胞を移植すると、神経細胞になりまして、そこのニューロンネットワークに組み込まれてシナプスがつくられ、上から来たシグナルが移植した細胞を介して、また下のほうへとリレーしていくようになるのです。
あと、もうひとつとして、神経系の細胞のうち、グリア細胞の一種であるオリゴデンドロサイトというミエリンを軸索にまく細胞がありますが、それが死ぬことにより、髄鞘が正常に形成されなくなり、神経線維が無髄化してしまうことがあります。そうすると電気の伝達速度が極めて遅くなり、運動障害をきたしてしまいます。そこで神経幹細胞を移植することで、オリゴデンドロサイトを補い再髄鞘化させるわけです。
岸本 そのメカニズムは、岡野先生が御子柴先生のもとで研究されていたような……。
岡野 はい。学位論文のテーマにしていた内容です。自分がかねてからおこなってきた研究が再生医療にも役立ったということで、自分なりに感動しているところです。
岸本 脊髄を損傷してから長く時間が経過した患者さんへの治療の見通しはいかがですか。
岡野 じつはその研究の成果も、ちょうど今日の未明に発表できたのですが、慢性期の患者さんに対する治療への手がかりもついてきました。こちらの研究はまだ動物実験レベルですが、iPS細胞からつくった神経幹細胞からさまざまな神経分化が誘導されるよう、移植前にNotchシグナルという情報伝達系を阻害する低分子化合物で処理してから移植すると、ホストの脊髄の中で移植細胞の神経細胞の成熟度が増して、慢性期の脊髄損傷でも運動機能の回復が得られました。今後の脊髄損傷治療のプロトコルに入れて、進めていきたいと思っているところです。
岸本 すると、慢性期の脊髄損傷でも回復の可能性が見えてきたわけですね。ただしお話を聞いていると、急性期より慢性期のほうが治療はむずかしそうですが、それはどうして……。
岡野 慢性期ですと、損傷した脊髄のなかに瘢痕組織が多くできてしまい、かさぶたのように固くなって神経の軸索が伸びていくのをじゃまするのです。けれども、移植する神経幹細胞の神経細胞としての成熟度を上げてやると、瘢痕組織を乗り越えて軸索を伸ばしていくことがわかってきました。
岸本 脊髄損傷については、車いすでの生活を余儀なくされている人が、だんだん減っていくわけですかね。
岡野 重症の患者さんに対する治療の難度は高いものがあります。でも、そうした方への治療法も開発していきたいと思っています。最近はリハビリテーション用のロボット技術が発展しているので、それらの方法も組みあわせて、集学的併用療法を開発していけば、これまで治療法がなかった患者さんに対する治療でも見通しがついてきたと思っています。

岡野栄之 氏
慶應義塾大学 医学部生理学教室 教授
1959年、東京都生まれ。83年慶應義塾大学医学部卒業。慶應義塾大学医学部生理学教室助手。85年大阪大学蛋白質研究所助手。89年米国ジョンス・ホプキンス大学医学部生物化学教室研究員。92年東京大学医科学研究所化学研究部助手。94年筑波大学基礎医学系分子神経生物学教授。97年大阪大学医学部神経機能解剖学研究部教授(99年より大学院医学系研究科教授)。2001年慶應義塾大学医学部生理学教室教授。主な研究領域は、分子神経生物学、発生生物学、再生医学。慶應義塾大学では大学院医学研究科委員長(2度)、医学部長を歴任。21世紀COEプログラム「幹細胞医学と免疫学の基礎-臨床一体型拠点」拠点リーダー、内閣府FIRSTプログラム「心を生み出す神経基盤の遺伝学的解析の戦略的展開」中心研究者もつとめる。RNA結合タンパク質Musashiの研究で世界的に有名。神経系疾患に対する再生医療の研究も進める。東京テクノフォーラムゴールドメダル、文部科学大臣表彰、井上学術賞、紫綬褒章、ベルツ賞など多数。
パーキンソン病、ALS…… iPS創薬の研究も進める
岸本 岡野先生の研究グループはとても大規模で、さまざまな研究をされていますね。応用面では脊髄損傷のほかに、パーキンソン病などに対してもアプローチされていると聞きます。
岡野 はい。パーキンソン病については、患者さんからiPS細胞をつくって、病気の進行を遅らせるような薬を開発しようとしています。
岸本 それはうまくいきそうですか。
岡野 いまちょうど製薬企業と共同研究をしていて、患者さん由来のiPS細胞を利用した系を使って、既存薬のライブラリーから創薬の標的となりそうな重要分子を見つけられたところです。パーキンソン病の患者さん由来の神経細胞ではT型カルシウムチャネルの機能が高まっているのですが、その機能を阻害する化合物を細胞にあたえることで、細胞死を抑えられることがわかってきました。
岸本 ほかの病気に対してはいかがですか。
岡野 神経系の難病に筋萎縮性側索硬化症(ALS:Amyotrophic Lateral Sclerosis)がありますが、この病気に対する研究もかなり進みました。ALS患者さんの体細胞からiPS細胞をつくります。そのiPS細胞から誘導された神経細胞が変性していく系を試験管内でつくりました。その神経細胞を観察すると、RNA結合タンパク質の局在異常、ストレス顆粒の形成、軸索の短縮化、細胞死などのさまざまな異常が見られました。それらを抑制する薬を既存薬ライブラリーから探索したところ、神経疾患の治療薬として使われているロピニロール塩酸塩が、ALSのそうした表現型を抑えることがわかりました。こちらは慶應大学病院神経内科での治験開始となります。
岸本 創薬の研究に関連して、ベンチャーも起業されたと聞きます。
岡野 はい。再生医療については製薬会社からの支援も多くいただいていますが、iPS細胞を利用した創薬については大学発ベンチャーで資金を得て研究を進めることを基本としています。
岸本 どこかの企業が面白いと思ったら、全部資金を注ぎこむということにはならないのですか。
岡野 再生医療と違って、iPS細胞創薬のほうは、まだ駆け出しの段階ですしね。いまお話したALSの治療薬開発などでは企業主導でなく、医師主導で治験を進めています。治験の第1相を始める段階ぐらいまでは、AMED(日本医療研究開発機構)からの資金が頼りになりますが、第2相や第3相までAMEDが資金を出していては国の財政が破綻してしまいます。
ですので、大学発ベンチャーをつくって、資金を調達し、新薬が承認されるまでがんばろうということでやっているわけです。それに国内外のさまざまな難病関連の財団にも興味をもっていただき、研究費を補助していただいています。
アクセルを踏んで加速して研究を続けていく
岸本 岡野先生は、もともと慶應大学に入られたわけですが、どうして東大でなく慶應へと進んだのですか。
岡野 中学までは公立学校に通っていましたが、高校受験で慶應義塾志木高校ともうひとつの高校と両方に受かったんですね。それで、自分なりに高校受験の勉強をしてきて消耗もしていて、「大学でも受験勉強となるときついなぁ」と思って、悩んだ末に慶應付属の高校に進むことにしたのです。
岸本 付属高校ですから、自然に試験なしで慶應大学に入れるわけですね。
岡野 はい。でも、高校時代うっかりしたことがありまして。大学では理論物理学を学びたいと考えていましたが、当時は理学系の学部が慶應大学になかったのです。いまは理工学部がありますが、当時は工学部で。そのことに気づいて愕然としたのは高校3年のときでした(笑)。
それで、いろいろな学部の説明会にいくなかで、医学部でも基礎的な研究ができることを知ったのです。好きだった物理学者のエルヴィン・シュレディンガーは物理学者でありながら『生命とは何か』という本も出していましたし、生命科学的な学びもおもしろいだろうと思って、医学部に行くことにしました。1977年に入学して、1983年に医学部を卒業しました。
岸本 僕と20年ちがう(笑)。実際、医学部生になって、生命科学への興味はいかがでしたか。
岡野 渡辺格先生の授業を受けたり、日本分子生物学会が開催したAMBO (Asia Molecular Biology Organization)シンポジウムに参加したりして、「分子生物学っておもしろいな」と思いましたね。
ただし、当時はなかでも免疫やがんの分野の研究が強くて、それらの分野に自分がいまから入って追いかけるのはきついのではとも思っていました。けれども神経の分野についてはまだ分子生物学の研究がほぼおこなわれていないことに気づきました。それで、御子柴先生に「岡野くん、やりなよ」と言われて、当時、慶應大学にいらっしゃった塚田先生と御子柴先生のもとで研究をすることになったわけです。
岸本 そうした経緯があったんですね。
それで最近では、岡野先生は慶應で医学部長をされていたんですよね。
岡野 ええ。2017年の9月まで、2年半つとめました。
岸本 僕も阪大で医学部長をしていた時期がありますが、慶應で医学部長をされてみてどうでしたか。
岡野 忙しくはありました。でも、岸本先生が医学部長だったときの凛々しいお姿を覚えていて、医学部長はアドミニストレーション能力ももちろん求められるけれど、先頭に立って研究をするのも大事だと思って、両方やってきました。
岸本 両立されたのですね。いまは、もう研究に専念されているのですか。
岡野 大学院の医学系研究科委員長をしています。大学院だけを見ているので、時間的にはだいぶ研究に専念できるようになりましたね。
岸本 学部長としても、研究科委員長としても有能だったんでしょう。それに最近では、塾長の選挙にも出ていましたね。
岡野 あれは一応そうなりましたけれどもね。医学部が100周年を迎え、そのような機運が盛り上がっていたのかもしれません。
岸本 いままで医学部から塾長は出ていないのですか。
岡野 はい、残念ながらその通りです。慶應では、文学、経済学、法学、商学あたりが歴史的にも強いです。大阪大学のように、医学部が大学をリードしていくというのが慶應でもできたらと一瞬、思ったことはありますけれどね(笑)。
岸本 最後になりますが、岡野先生のメジャーな成果は、Musashiの基礎的研究から始まって、応用的研究で再生医療の臨床研究も始まろうとしています。創薬も実現するとよろしいですね。
岡野 ありがとうございます。ALSの発症機構でもRNA結合タンパク質の異常があるとお話しましたが、私の研究はRNA結合タンパク質をキーワードに、Musashiから、神経系の再生医療、iPS細胞創薬までがつながっていると思っています。ここまで20年かかりましたが、基礎研究の成果を糧に、臨床研究や治験を始められるところまできました。アクセルを踏んで加速して、いろいろな形で研究を続けていければと思っています。
岸本 今日はお忙しいところ、どうもありがとうございました。
EYES
RNA結合タンパク質Musashiの発見・解明を起点に、
神経系疾患の治療への道が開いた
再生医療は臨床研究、創薬は治験の段階へ
RNA結合タンパク質は、細胞内に存在する1本鎖、あるいは2本鎖RNAと結合するタンパク質の総称で、機能的に関連性のあるRNA群の細胞内挙動を制御していると考えられています。
RNA結合タンパク質のひとつに「Musashi」とよばれるタンパク質ファミリーがあります。Musashiは、Tramtrack という転写抑制因子のmRNAの3’側の非翻訳領域に結合します。すると、このmRNAの翻訳が抑制されます。その結果、生じるのが「細胞分裂の非対称性」。つまり、細胞が分裂して自分とおなじ細胞を2個つくるのではなく、自分とおなじ細胞1個と別の細胞1個をつくるようになるのです。このようにRNA結合タンパク質Musashiは、標的のRNAと結合して、細胞の非対称性分裂をもたらすのです。
脳ではMusashiを多く発現している細胞が、神経細胞に分化できる神経幹細胞ということになります。ショウジョウバエの神経幹細胞(神経母細胞)では、Musashiが作用することで、1個の細胞が分裂してできた2個の細胞のうち、1個は毛へ、もう1個は神経細胞へと分化するという非対称性の経路をたどります。Musashiが作用することで、神経細胞がつくられる経路が保たれるわけです。
このRNA結合タンパク質Musashiを発見したのが、今回の対談で登場する岡野栄之氏です。岡野氏はまず1991年、ショウジョウバエからmusashi遺伝子を発見しました(詳細は対談で)。その後、Musashiを指標にしてマウスの脳やヒト成人脳といった哺乳類にも神経幹細胞が存在することを明らかにしています。
この「ヒトの大人の脳に神経幹細胞が存在する」という事実は、医療分野で大きな意味をもつようになりました。従来の定説では「神経系は成長発達が終われば再生しない」とされ、神経の損傷を回復するような治療は見込めないと考えられてきました。そうしたなかで、脳に内在性の神経幹細胞が存在し神経細胞やグリア細胞がつくられる、つまり、ヒトの神経系は再生しうることが示されたわけです。定説は覆り「損傷した神経系を再生することができる」と考えられるようになりました。いまではMusashiは、神経幹細胞のマーカー分子としても知られるようになりました。
岡野氏のこれら一連の研究成果により、神経系の再生医療の道が大きく開かれました。岡野氏自身は以降、神経系疾患の再生医療を実現させるための研究にも取り組んでいます。折しも、神経幹細胞を試験管内でつくりだせるES細胞やiPS細胞が樹立されました。神経幹細胞を試験管内でつくり、患者の体内に移植するという再生医療の道筋が立ちました。下肢の麻痺などを伴う脊髄損傷の患者に対する臨床研究が、岡野氏のチームによって、今年2019年に始まろうとしています。
一方で、RNA結合タンパク質の解明は、神経系疾患の治療に向けた創薬の研究にも役立てられています。たとえば、筋肉が徐々に萎縮していく筋萎縮性側索硬化症(ALS)では、細胞内でのRNA結合タンパク質の局在異常が見つかっており、これが疾患の原因の一つと考えられています。岡野氏はこれまで培ってきたRNA結合タンパク質の知見や、iPS細胞の技術を駆使して、患者由来の神経系細胞に対して治療効果のある化合物を探し、創薬につなげようともしています。2017年12月には、ALS治療薬候補ロピニロール塩酸塩の治験開始が慶應義塾大学により発表されました。