LF対談
師を目指すなかれ、師の目指しているものを目指せ。真髄をついた研究こそが重要。 No.96(2022.6)

大阪大学大学院医学系研究科呼吸器・免疫内科学教授
大阪大学医学系研究科長、医学部長、総長参与
熊ノ郷淳 氏
大阪大学大学院医学系研究科免疫制御学教授
大阪大学免疫学フロンティア研究センター拠点長
竹田潔 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
「どうして」と病因を突き詰める
探究型の講義の鮮烈な印象
岸本 「LF対談」では、これまでノーベル生理学・医学賞受賞者レベルの研究者の方々と数多くお会いさせていただいてきました。大村智先生(北里大学特別栄誉教授)から始まり、山中伸弥先生(京都大学iPS細胞研究財団理事長)、本庶佑先生(京都大学特別教授)、大隈良典先生(東京工業大学栄誉教授)などのみなさんです。
ただし、受賞をされたから対談をお願いするのではなく、どなたも対談後に映えある賞を受賞なさっています。対談を企画するに当たり誇らしいことです。
今後に向けての期待も込めて、今回は僕が大阪大学の医学部第三内科(現・呼吸器・免疫アレルギー内科)に所属していた1990年代前半に、教室の門を叩いてこられた熊ノ郷淳先生と竹田潔先生のお二人をお呼びした次第です。
そもそもどうして阪大の医学部に入って、僕の教室に入ろうとしたのかからお話してもらえればと思います。
熊ノ郷 私が中学3年の時、父親が脳腫瘍となり大阪大学医学部附属病院に入院しました。そうしたこともあり阪大の医学部に関心と憧れを抱き、入学を志しました。けれども、入学後すべきことが見つからず、モチベーションが上がらないまま過ごしていました。
2年生になったある日、家で新聞の朝刊を見ると、岸本先生がインターロイキン6(IL-6:InterLeukin 6)を発見したというお顔写真付きの記事が目に飛び込んできたのです。「自分がいる阪大では免疫学研究がさかんなんだ」と初めて知りました。受験では物理と化学を選択していたので、免疫はもとより生物学の知識をほとんどもっていませんでしたが、「こんな発見をした人が大学にいるのだから免疫学の勉強をしよう」と思い立ちました。その後の岸本先生の講義も受け、さらに「免疫学を研究したい」という思いが強くなりました。
そうした中、医学部卒業年の6回生となり、大学院でどの科に進もうか迷っていたところ、岸本先生が阪大内で細胞工学センターから第三内科に移られるとお聞きし、岸本先生の教室の門を叩いた次第です。
竹田 私は、両親がともに微生物研究者で、大阪大学微生物病研究所(微研)に勤務していました。親の影響もあり、医学の基礎研究には小さいときから興味をもっていて、両親の勤める阪大を受験してみようと志し、医学部に入学できました。
ただし、私は1年の浪人を経ていたので、同じ年の熊ノ郷先生は1年先輩で「研究をやらないかん」といつもアドバイスをいただいていました。
岸本 二人とも、医学部生であるとともに、ボート部に入っていたんでしたかね。
二人 そうです。
竹田 それで、学部生時代、岸本先生から臨床の講義を受けました。一般的な臨床の講義は、「この病気の症状はこうで、診断法と治療法はこうで」と、暗記を要するものでしたが、岸本先生の講義はまったくちがいました。たとえば関節リウマチについての講義では、「関節が腫れるのはどうしてかわかるか。免疫が暴走するからや」「じゃあ、どうして免疫が暴走するかわかるか」と、私たち学生に考えさせるものでした。岸本先生の講義はさらに「細胞」そして「分子」と深まり、最終的にIL-6まで辿りついたのでした。病気の根本的な原因を突き止めていく形の講義をされていました。「考えるとはこういうことなんだ」と学びました。先輩の熊ノ郷先生からも強い勧めをいただいて、「岸本先生の第三内科に行くしかない」と決心しました。
岸本 そうでしたか。熊ノ郷先生も竹田先生も、僕が細胞工学センターから第三内科に移ったことに縁があるわけですね。じつは僕も当時、移籍するかどうか相当に迷ったんです。けれども、「優秀な人を育てられるところは、やっぱり人の多く集まってくる内科や」と思って、移籍することにしました。僕にも医学部5年生のとき、九州大学から山村雄一先生が阪大に移ってこられて、「この先生のところに行こう」と第三内科に入る決心をした経験がありましたしね。
お二人とも講義のことを覚えていると話してくれましたが、僕も優秀な人を育てたいという一心でした。前のほうの席で僕の講義を聴いていた人たちが第三内科に入ってきました。熊ノ郷先生と竹田先生もそうでしたね。
熊ノ郷 岸本先生の講義を聴いた経験から、いま教員として「講義をしっかりやらないと」と強く思っています。最近はコロナ禍で、対面講義をしづらい状況にありますが、Zoomミーティングを利用して、夜に学生たちとつないで「免疫夜話」という講話会を開いています。できるだけ学生たちに研究のおもしろさを伝えられればと思っています。
岸本 熊ノ郷先生は、前々から希望する学生たちと「面談」をしてきたと聞きます。
熊ノ郷 はい。2011年に大阪大学免疫学フロンティア研究センター(IFReC)から医学系研究科の呼吸器・免疫アレルギー内科へ移って以来、「100人面談」をしています。1年間で100人ほどの学生に教授室にきてもらい、一対一で話をするというものです。ここ2、3年はコロナ禍で直接面談はむずかしくなりましたが、それでもこれまで800人以上の学生たちと話してきました。
岸本 優秀な学生は入ってきていますか。
熊ノ郷 たくさん入ってきています。学生たちが育っていくような環境をつくるのが自分の大事な使命だと思っています。
免疫不全症からセマフォリンを得る
「神経・免疫・代謝連関」の研究へ
岸本 お二人の研究のことに戻りますが、僕が第三内科の教授になった初年度に熊ノ郷先生が入ってきて、翌年度に竹田先生が入ってきました。専門分野への道を歩きはじめる時期です。僕の師だった山村先生は、「上の言うことなんか気にせず、自分の好きなことをやれ」と言っておられましたが、実際はなかなかそうもいきませんな(笑)。
熊ノ郷先生は大学院時代までは僕の下にいながら、主に細胞生体工学センターに出向いて研究し、大学院修了後は菊谷仁先生(現・大阪大学免疫学フロンティア研究センター教授)の下に行かれましたね。それで、いま熊ノ郷先生の代名詞となっているセマフォリンの研究に取り組まれました。
熊ノ郷 はい。1997年、菊谷先生が大阪大学微生物研究所の教授になられたとき、大学院生として菊谷先生に付いていきました。当時、免疫不全症に関連する現象を探そうと思って実験をしていたところ、セマフォリンを得られたのです。
岸本 あらためて、セマフォリンとはどういったものですか。
熊ノ郷 もともと神経に関わる分子として知られていました。神経の発生過程で、神経の進むべき方向をナビゲートするような、神経ガイダンス因子として同定されていました。
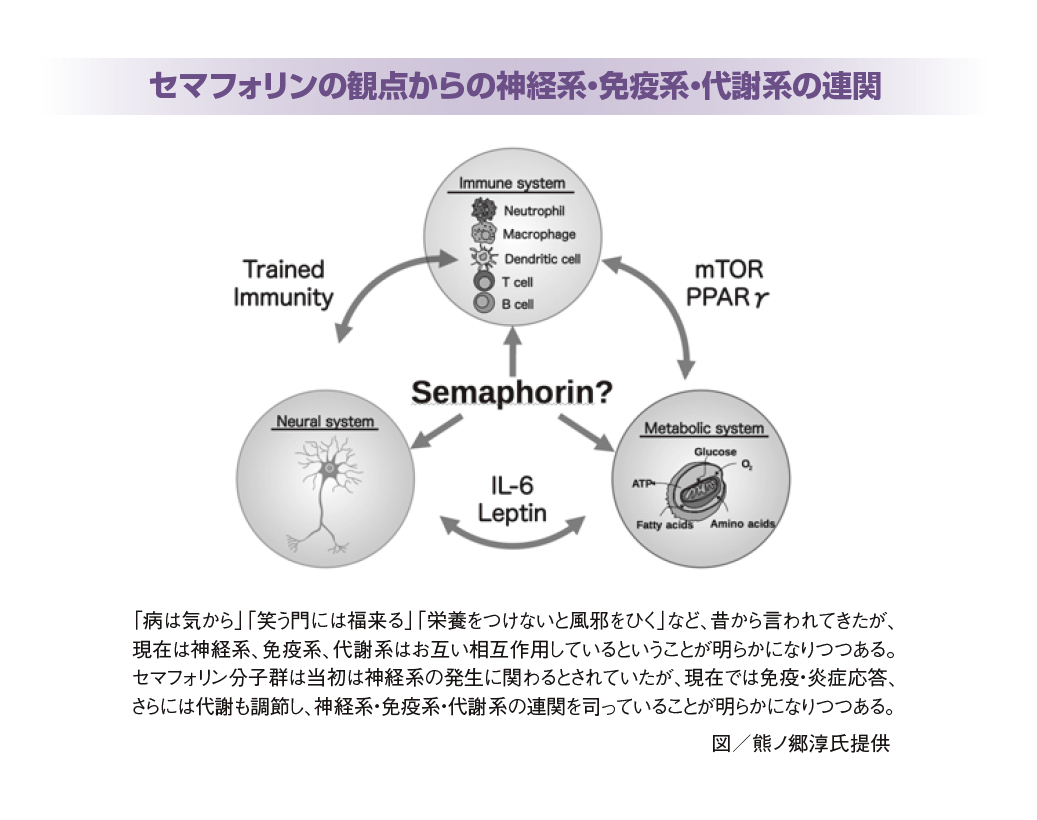
ところが免疫不全症の研究をしていると、セマフォリンを得ることができました。「どうして神経の分子であるセマフォリンが免疫不全症の疾患関連分子として現れるのか」と疑問がわき、神経系と免疫系の相互作用に興味をもつようになりました。さらに、代謝系も神経で調節されていることがわかってきたので、現在は「神経・免疫・代謝連関」を研究テーマにしているところです。
岸本 「免疫」が付いた「免疫セマフォリン」という言葉を聞くけれど、これは熊ノ郷先生が付けたものと聞きます。
それで、もともと菊谷先生は、免疫細胞の一つであるB細胞の活性化に必要なCD40分子の研究をされていましたよね。これと熊ノ郷先生のセマフォリンの研究との関係はどういったものでしたか。
熊ノ郷 研究対象にしていたと言っていた免疫不全症は、抗体のうち免疫グロブリンM(IgM:Immunoglobulin M)の量が相対的に多くなる「高IgM症候群」とよばれるものであり、CD40の信号が行き届かないことで生じるものだったのです。そこで、CD40の刺激で発現量が変化する遺伝子を探そうとして、サブトラクション法という手法で実験に取り組んでいました。そのとき、セマフォリンが得られたのです。セマフォリンには何種類もありますが、そのときのは、Sema4D/CD100とよばれるものです。B細胞の活性化に関わる分子であることがわかり、2000年に一連の研究で初めて論文発表することができました。
ところが、さらに調べていくと、B細胞以外にも、T細胞、樹状細胞、マクロファージ、好中球といった免疫系の細胞それぞれに、対応するセマフォリンが芋づる式に見つかっていったのです。
岸本 構造は似ているからセマフォリンで括れるけれど、それぞれにちがうところがあるわけですか。
熊ノ郷 はい。関わっている免疫反応が、それぞれ異なるのです。
岸本 それらのセマフォリンがないと、生体はどうなりますか。高IgM症候群のほかにも、やっぱりいろいろな病気になるんですか。
熊ノ郷 セマフォリンの種類にもよりますが、免疫反応が落ちたり、炎症やストレスに対応できなくなることがわかってきています。たとえば、抗好中球細胞質抗体(ANCA:Anti-Neutrophil Cytoplasmic Antibody)関連血管炎という免疫疾患がありますが、これは好中球にあるSema4Dというセマフォリンがなくなることで、好中球が「暴走」する結果、生じるものとわかっています。
岸本 そうすると、そのSema4Dがなくならないようにすれば、ANCA関連血管炎を治療することができるわけですか。
熊ノ郷 ええ。Sema4Dは好中球の「暴走」を止めるブレーキ役なので、Sema4Dのブレーキ作用を強めるような抗体が実現すれば治療につながっていきます。
岸本 セマフォリンの研究が病気の診療につながるという事例で、最も有望なのはどんなものですか。
熊ノ郷 これも免疫系の病気ですが、多発性硬化症では、Sema4Aが診断マーカーとして使われていて、すでに「多発性硬化症・視神経脊髄炎診療ガイドライン」にも記載されています。
岸本 治療法についてはどうですか。セマフォリン研究から薬が生まれたといったようなことは……。
熊ノ郷 具体的な臨床試験まではまだ進んでいませんが、経路の全容を解明し、そこから病気を制御する可能性を見出そうとしているところです。たとえば、製薬企業と共同で、セマフォリンの濃度を中和する抗体の開発をしています。そうした成果を一つの「窓」にして、パスウェイ解析などで全容を解明していけば、各種の病気に対して制御すべき経路が見えてくると思います。これにより、汎用的な医療応用につなげられるのではないかと考えながら研究しています。
岸本 現在の呼吸器・免疫内科学教室(旧・第三内科)全体では、なにか興味深いトピックはありますか。
熊ノ郷 臨床の教室ですので、外来と入院の患者さんから血清を提供していただき、研究に活用させていただています。これはすごい症例数となりました。
岸本 そんなに多く集めているのですか。
熊ノ郷 はい、集めています。
岸本 僕も阪大病院で血を採ってもらったことがあるけれど、それもですか。
熊ノ郷 はい、岸本先生のもあります(笑)。それで、血清を用いて、血清に含まれるエクソソームとよばれる小胞の「中身」に着目した研究をしています。エクソソームは、細胞外膜小胞という血清中を流れる「郵便袋」みたいなものであり、このなかに核酸、マイクロRNA、あるいはさまざまなタンパク質などを含みます。その含まれる内容物がなにであるかによって、どんな病気にかかっているかを診断することができます。たとえば、呼吸器系であれば喘息や慢性閉塞性肺疾患(COPD:Chronic Obstructive Pulmonary Disease)、また免疫系であれば全身性エリテマトーデス(SLE:Systemic Lupus Erythematosus)やベーチェット病などのマーカーとなります。
岸本 病気によってエクソソームの中身がちがってくるわけですか。
熊ノ郷 その通りです。ベーチェット病の場合、ミトコンドリアDNAが入っていますが、SLEの場合は2本鎖DNAが入っています。また、喘息だと、好酸球に含まれる化学物質がマーカーになります。従来は血清中ではすぐ分解されてしまいますが、エクソソームの袋に包まれているために分解されず保存されているので、マーカーとして使えるわけです。このマーカーを使った診断法の開発を、装置メーカーと進めているところです。臨床の教室という、患者のみなさんに血清を提供していただける場でなければ、実現できなかったことです。

熊ノ郷淳 氏
大阪大学大学院医学系研究科呼吸器・免疫内科学教授
大阪大学医学系研究科長、医学部長、総長参与
1966年大阪府生まれ。91年大阪大学医学部医学科卒業。同大学医学部付属病院、NTT西日本病院で内科臨床研修。93年大阪大学大学院医学研究科(内科学第三講座)入学。97年同大学微生物病研究所助手。2003年同助教授。06年同教授。07年世界トップレベル研究拠点免疫学フロンティア研究センター(WPI-IFReC)教授。11年大阪大学大学院医学系研究科呼吸器・免疫アレルギー内科教授。15年大阪大学大学院医学系研究科・副研究科長。15年大阪大学副理事(~17年)。18年大阪大学大学院医学系研究科・副研究科長(~21年)。21年より医学系研究科長、医学部長、総長参与。専門は免疫学。日本免疫学会理事、日本内科学会評議員、日本臨床免疫学会理事、日本炎症再生学会理事、日本骨免疫学会理事などをつとめる。専門分野は免疫学。セマフォリンが免疫で重要な役割を果たしていることを解明。受賞は、日本学術振興会賞、日本免疫学会賞、大阪科学賞、文部科学大臣表彰・科学技術賞、大阪大学総長顕彰、持田記念学術賞、米国臨床医学会特別会員選出(Elected membership for American Society of Clinical Investigation)。

竹田潔 氏
大阪大学大学院医学系研究科免疫制御学教授
大阪大学免疫学フロンティア研究センター拠点長
1966年、米国生まれ。92年大阪大学医学部卒業、同大学医学部附属病院内科学第三講座にて研修開始。94年同大学大学院医学研究科(内科学第三講座)入学。98年同研究科修了。97年日本学術振興会奨励研究員。98年兵庫医科大学生化学講座助手。99年大阪大学微生物病研究所助手。2003年九州大学生体防御医学研究所教授。07年から大阪大学大学院医学系研究科教授、同大学免疫学フロンティア研究センター(IFReC)教授。19年から大阪大学免疫学フロンティア研究センター拠点長。日本免疫学会理事、日本生化学会評議員、Federation of Immunological Societies of Asia-Oceania理事・財務担当理事などをつとめる。専門分野は免疫学。タンパク質Lypd8が細菌の鞭毛に結合してその運動性を抑制することを見出すなど、腸管恒常性を維持する分子の発見・同定とその分子機構の解明をおこなう。受賞は、日本免疫学会賞、日本学術振興会賞、大阪科学賞、ベルツ賞、持田記念学術賞。
「大腸の上皮」に着目、腸内細菌と
免疫系を分けるしくみ解明
岸本 竹田先生は腸管免疫の研究を幅広くしていますね。腸管に60兆個もの細菌がいるにもかかわらず、ヒトは病気にならない。むしろ腸内細菌のおかげで健康でいられるともいいます。
第三内科の僕の教室に所属した後、竹田先生は審良静男先生(現・大阪大学免疫学フロンティア研究センター特任教授)の下で研究されました。最初どのようなことから着手したのですか。
竹田 岸本先生に「審良先生のところで勉強してこい」と言っていただいて、細胞工学センターにおられた審良先生の下で研究を始めたわけですが、ちょうど審良先生は岸本先生の発見されたIL-6のシグナルに関する研究をされていた時期でした。私は、そのシグナル候補だったSTAT3遺伝子を欠損させたマウスをつくって、マウスにおいてIL-6のシグナルがどうなるかを調べました。予想通り、STAT3遺伝子の欠損によりIL-6のシグナルはなくなりましたが、さらにいろいろ調べていると興味深いことが見えてきたのです。その中でも予想外だったことに、マウスの自然免疫系の細胞でSTAT3遺伝子を欠損させると、炎症性腸疾患が生じました。
炎症性腸疾患については、それまでの臨床研修で、3人の患者の方を診てきましたが、治療法がなく、絶食点滴を施すことしかできませんでした。そうした苦い経験もあり、炎症性腸疾患に大きな関心をもつようになりました。審良先生の下で自然免疫の研究をしながら、炎症性腸疾患の研究にも着手しはじめたのです。
岸本 審良先生は大阪大学細胞生体工学センターから1996年に兵庫医科大学に移りましたね。竹田先生も迷わず審良先生に付いていったわけですか。
竹田 はい。審良先生の下で研究を進めたいと強く思っていたので、審良先生が兵庫医科大学に移ると聞いたとき、「私も連れていってください」とお願いしました。阪大の大学院生に籍はありましたが、兵庫医科大学で研究させてもらいました。
岸本 長く兵庫医科大学にいたのでしたか。
竹田 3年で審良先生が阪大の微研に戻られたので、私も付いていきました。
岸本 その後、竹田先生は九州大学に移りましたね。
竹田 はい。九州大学から声をかけていただきました。当時、岸本先生は阪大で総長をされており、私はまだ助手の身でありながら総長室に行って、「九州大学からよばれたのですが、行ってもいいですか」と伺うと、岸本先生から「行きなさい! 行きなさい!」と言われ、喜び勇んで九州大学に向かいました。
岸本 それで竹田先生は、炎症性腸疾患を基点として腸管免疫の研究を進め、いまは腸内細菌のこと、腸管免疫細胞のこと、そして腸内細菌と免疫細胞を分け隔てるしくみのことまでを研究していますね。どのように研究を展開していったのですか。
竹田 研究者として独立してからは炎症性腸疾患についての研究を本格的に始めましたが、どうしてこの疾患が起きるのかはあまりよくわかりませんでした。現在もそうです。けれども、「消化管に存在する免疫細胞が腸内細菌を攻撃することで炎症が起きている」という事実はわかりました。そもそも、免疫の側からすれば異物である細菌を攻撃するのは当然のことです。その一方で、「ではどうして健康なヒトでは、腸管の免疫細胞が異物の腸内細菌を認識せず、攻撃もしないのだろうか」と、疑問を抱くようになりました。
この疑問に対する答えとして言われていたのは、「粘液層の存在によって、異物である腸内細菌が腸管組織と直接に接することが避けられているから」というものでした。けれども、炎症性疾患の原因にこの粘液があるわけではありません。それ以外の原因があるにちがいないと考えました。
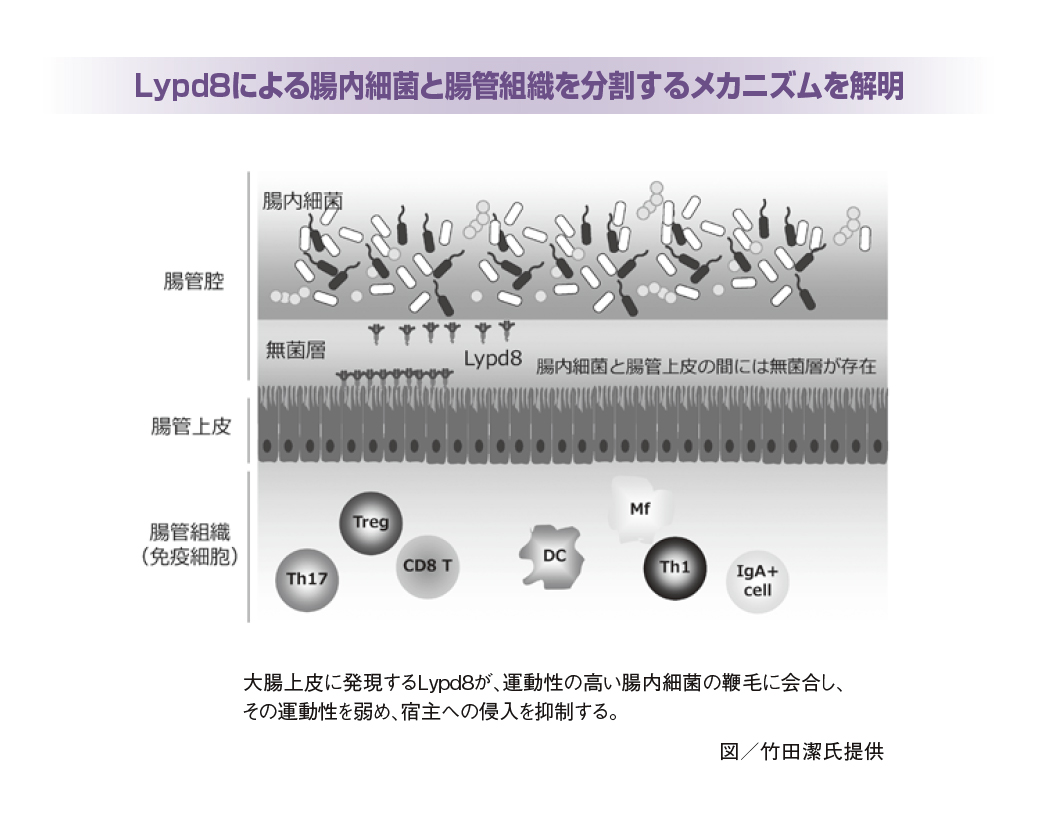
そこで着目したのが「大腸の上皮」でした。大腸の上皮だけに発現しているタンパク質があれば、それこそが腸内細菌を抑え込む役割を担っているのだろうと考えたのです。そうしたものを検索してみると、Lypd8というタンパク質の分子を見つけました。詳しく機能を解析すると、Lypd8が腸内細菌の鞭毛にくっつくことで細菌の運動性を止めていることがわかってきたのです。逆に、Lypd8遺伝子をなくすと、腸内細菌が鞭毛を使って運動し、どんどん大腸上皮の内側に侵入してきて、炎症性腸疾患が起きることがわかりました。さらに、大腸性腸疾患の患者の方ではLypd8の分子の発現量が激減していることもわかりました。これらから、「Lypd8が腸内細菌と免疫細胞をきれいに分け隔てることで、炎症を抑制しているのだ」ということがわかってきた次第です。
岸本 そうでしたか。従来、腸内細菌を抑える役割と考えられていた粘液は、ムチンというネバネバしたものだと聞きますが、竹田先生が見つけたLypd8もネバネバしているわけですか。
竹田 Lypd8分子自体には粘性はありません。けれども、ムチンとちょうど同じような具合に、Lypd8は糖鎖の修飾を高度に受けているのです。ですので、現段階ではまだ仮説ですが、腸内細菌と免疫細胞を分け隔てるのに本当に必要なのはLypd8というよりも糖鎖なのではないかと考え始めているところです。この仮説を証明すべく、実験を進めています。
岸本 マウスだけでなく、ヒトでもLypd8と炎症性腸疾患の関係性はわかってきているわけですか。
竹田 ヒトでは、Lypd8の遺伝子の変異は見つかってはいません。それはおそらく、生まれた時点でLypd8がない場合、幼少期にひどい炎症を起こして死亡してしまうからではないかと考えています。
岸本 けれども、成人でも炎症性腸疾患の患者はおられますよね。遺伝子変異はないけれど、Lypd8が減ってきているということですか。
竹田 すくなくとも、Lypd8が減っていくことによって症状が悪化するということはわかっています。
岸本 治療法は見つかりそうでしょうか。
竹田 製薬会社の方と議論を重ねているところです。これまでの研究でわかっているのは、「腸内細菌と免疫系をきれいに分け隔てることができさえすれば、炎症性腸疾患を免れられる」ということです。ですので、先ほど仮説として申し上げた糖鎖を用いて運動性の高い腸内細菌を抑え込むことで、その分け隔てができないだろうかと考え、企業とともに創薬に向けた話し合いをしているところです。
岸本 腸管免疫の研究については、竹田先生の研究のほか、竹田先生の下で研究していた慶應義塾大学の本田賢也先生(医学部微生物学・免疫学教室教授)も、T細胞が分化したTH17細胞による自己免疫性反応の増加が自己免疫性疾患を起こすといったことを研究しておられますね。それに理化学研究所の大野博司先生(生命医科学研究センター粘膜システム研究チーム・チームリーダー)も、腸内細菌と中枢神経系の炎症の関係などを研究しておられます。日本の腸管免疫研究のレベルはどのくらいの位置にあるのでしょうか。
竹田 腸内細菌や腸管免疫の研究では、日本全体としては世界をリードしていると思っています。日本としてさらに研究を発展させようということで、みんなで一緒になって研究を進めたりもしています。もちろん、世界的に関心をもたれている分野ですので、競争が極めて激しいことも身をもって実感しています。
岸本 竹田先生のLypd8についての研究も世界的に注目されていることを感じますか。
竹田 反響の大きさは感じています。2016年にこの研究成果を論文で発表してから、国際学会に招待されるようなことも増えてきました。
臨床経験と海外経験
それぞれの意義を論じ合う
岸本 熊ノ郷先生と竹田先生の研究の歩みを僕のものと比べてみると、共通するところもあれば、そうでないところもあります。共通するところとして感じるのは、臨床での経験を踏まえて、研究に取り組んでいるというところです。
熊ノ郷 臨床で患者さんの病気と向き合っていると、岸本先生がいつも問いかけてきた「なぜ」が無限といっていいくらいに満ち溢れていることを実感します。それに、まだなにも解決されていないという実感もあります。これらのことは、研究を継続していくための原動力にはなっていると思います。
竹田 私は岸本先生のおられた第三内科で臨床での研修を2年間しただけにすぎませんが、その2年間だけでも治すことのできない病気にいくつも出合いました。それ以来、「病気をなんとかしたい」という気持ちをもち続けています。病気を治すための根本的な原因を明らかにしようというモチベーションが常にあります。
岸本 他方で、僕と異なっている点は、僕は6年ほど外国で暮らして研究をしたことがあるけれど、お二人は基本的には国内で研究をしてきたというところです。外国に行って研究しようと思わなかったのか。行っておいたらよかったと思っているか、それとも別に構わないと思っているか。この記事の読者にも、留学について迷ったり考えたりしている人はいると思うのであえて聞きますが、どうでしょう。
熊ノ郷 大学院で研究を本格的に始める以前は、「大学院で学位論文をまとめて、それをもとに留学をするのかな」と自分ではイメージはしていました。けれども、大学院の時代にあまり大きな成果を出すことができなかったのと、先ほど申したとおり微生物病研究所に戻ってきたこともあり、留学の機会を逃したという実感は正直あります。セマフォリンのファミリーを次々と見つけだすことができ、自分に付いてきてくれる人も多くなってきたこともあり、留学には至りませんでした。
そんな私でも国際学会に出たり、岸本先生や竹田先生が率いてこられた免疫フロンティア研究センターに籍を置かせてもらったりして、海外研究者とやりとりする機会を多くもてているとは思います。ただし、海外の研究者たちと文化に根ざした会話までできているかといえば、そこまで至っていないのは残念なところとは思いますね。
竹田 私は親の留学先だった米国で生まれましたが、半年で帰国となったので、なにも記憶にありません。ただ、留学への強烈な憧れはありました。実際、兵庫医科大学で博士号の学位を取得したころ、留学しようと何件かコンタクトもしていました。そうしたとき、微生物病研究所にお戻りになることになった審良先生から、研究を手伝ってほしいと言われたのです。
岸本 審良先生は、普段そういうことをあまり言わない方ですね。
竹田 その通りです。そんな審良先生に手伝ってほしいと言われたので、なんの後悔もなく審良先生と自然免疫の研究をしていこうと決めました。後悔はまったくありませんでした。
その後、自然免疫の研究が開花し、審良先生が海外の学会や講演会に多く招待され、私もそうした機会でさまざまな国に行かせてもらいました。留学はしなかったので、そうした機会に交流しようと意識的に海外の研究者に話しかけたりはしました。
免疫学の継承・発展に向けて
牽引者としての決意
岸本 熊ノ郷先生は2021年より大阪大学の大学院医学系研究科長・医学部長をつとめておられます。また、竹田先生は2019年より大阪大学免疫学フロンティア研究センター(IFReC)の拠点長に就任され、僕はセンターの特任教授なのでいまや竹田先生の部下です(笑)。
それぞれリーダーとして、率いている組織をどう発展させていきたいと考えているか聞きたいと思います。
熊ノ郷 割と短期的なことでは、「一緒に仕事をしたい」と憧れるような素晴らしい研究者を大阪大学の仲間として迎えつづけたいというのがあります。
岸本 僕は感心していますよ。熊ノ郷先生は実際、優秀な人を次々と医学部の教授に呼んでおられる……。
熊ノ郷 岸本先生がおられた細胞工学センターは一つの理想的なモデルとなっています。岸本先生の研究室があって、そこに菊谷先生や審良先生、ほかに田賀哲也先生(現・東京医科歯科大学難治疾患研究所教授)や長澤丘司先生(現・大阪大学大学院生命機能研究科教授)もおられて、その隣には、谷口維紹先生(現・東京大学先端科学技術研究センターフェロー)の研究室があって、よいサイエンスとはどういうことかを叩き込まれるような場になっていた印象があります。いわば、ウィーンからよい音楽や音楽家が生まれつづけるのと同様のことが言えるのではないかと。
岸本 組織のリーダーには、自分よりも偉業のある人を迎えず「お山の大将」になっちゃう人も結構いて、日本の悪いところだと思います。熊ノ郷先生はそうならず、常に優秀な人を迎え入れようとしているように見えます。実際どうされているんですか。
熊ノ郷 広く研究分野を把握しているわけではないので、できるだけ論文を読むなどして、どんな方がどんな研究をしているかの情報収集はしています。それに、医学系研究科・医学部として、各専門分野の選考委員が外部の研究者の業績などをリストアップしてもいるので、そうしたことを踏まえてプレゼンテーションを見るようにはしています。
竹田 横から見ていて思うのは、熊ノ郷先生には人を見抜くセンスがあるということです。周囲の人があまり評価していないような人でも、熊ノ郷先生がその人の講演を聴いたりして「あの方は素晴らしい」と目をつけた方はやっぱり素晴らしい研究をしますし、逆もまた真なりです。
岸本 呼吸器・免疫アレルギー内科学教室からは、人が育ってきていますか。
熊ノ郷 日本リウマチ学会や日本呼吸器学会などで、新進気鋭の若手研究者としていつも名が挙がるような人物が育ってきていますし、基礎研究の道を志して大阪公立大学で早くも准教授として活躍している人物もいたりします。確実に人は育ちつつあると感じています。
岸本 長期的なことについても、発展させたいことはありますか。
熊ノ郷 長期的には、特定の分野の研究に憧れをもっているような学生のみなさんが自由に選んで出入りできるようなキャリアコースを構築できないかと考えています。現状だと、医学部卒業後、大学院で2年間は初期研修を受け、さらにもう3年間の専門研修が国の制度として義務づけられています。これだとどうしても職業専門学校的になってしまいがちです。そこで、学部生の時期に自分で基礎医学の研究室を選び自主的に研究をおこなう「基礎医学講座配属」や、初期臨床研修と大学院博士課程を同時進行する「MD研究者育成研修コース」といった制度をより充実させ、学生が自分の興味あることに打ち込める環境をさらに整えていければと思っています。
岸本 竹田先生は、免疫学フロンティア研究センター拠点長として4年目を迎えますね。免疫学でもとくに「ヒト」の付いた「ヒト免疫学」に重視していると発信していますが、どんな意味を込めているのでしょう。
竹田 これまで生命科学では、どの分野でもマウスなどの動物を用いて哺乳類の生体メカニズムを解明するという基本的な考え方がありました。けれども、とくに免疫学の場合、マウスの免疫機構とヒトの免疫機構には異なる点が多くあって、いくらマウスのモデルで免疫疾患の病態を明らかにしても、ヒトでは病態がちがってくるということが頻繁に起きています。私が研究している炎症性腸疾患でもそれがいえます。けれども、実際ヒトの免疫システムを解明するような研究を進めないことには、人びとの病気を治療し、社会に貢献する免疫学にはなりえません。そうした意味で、「ヒト」の免疫システムを理解していくことが必要であるという思いから、「ヒト免疫学」と表現しています。
「ヒト免疫学」を強調できるのは、さきほどお話のあった熊ノ郷先生たち医学系研究科・医学部がおこなっている病院で診療を受ける患者の方々の血清などのサンプルの提供があるからです。基礎研究の発展のためにと貴重なサンプルを使わせていただける環境があり、「ヒト免疫学」を実行できていると実感しています。
岸本 免疫学フロンティア研究センターは当初、国の総合科学技術会議で「世界トップクラスの研究拠点を国内に5つ程度つくる」といった目標が掲げられて企画された「世界トップレベル研究拠点プログラム」(WPI)の予算で創設されました。けれども予算期限は原則10年で、すでに国からの資金は出ていません。そうした中でどう発展させていきますか。
竹田 厳しい課題だと思っています。山村雄一先生、岸本先生、審良先生と継承されて花開いている「阪大の免疫学」をしぼませるわけにはいきません。その中心を担うのが免疫学フロンティア研究センターであり、免疫学を後世に向けて発展させていかなければならないと強く思っています。実際、新型コロナウイルス感染症(COVID-19)関連でも、免疫システムの重要性がクローズアップされ、感染症克服のための免疫学の必要性が改めて高まりました。免疫学の重要性は、大学としても認識してくれていると感じています。免疫フロンティア研究センターを「存続させる」のでなく「発展させる」という気概で運営に取り組んでいかなければなりません。
残念ながら、免疫フロンティア研究センターにはまだ定年まで役職を保証できるポストがありません。その点、阪大の医学研究科・医学部と連携して、研究科・学部に所属した研究者がセンターでの研究を一緒になってやっていただくといった方法もよいのかもしれないと思っているところです。
岸本 わかりました。最後に、「研究の進め方」ということで熊ノ郷先生と竹田先生が大切にしていることをお聞きします。
熊ノ郷 私は「師を目指すなかれ。師の目指しているものを目指せ」という先人の言葉を大切にしているつもりです。岸本先生は「こういったことをやらなあかん」「これがええ仕事や」と、目指しているものを言っておられました。菊谷先生も、審良先生も、それにいま隣にいる竹田先生も、「岸本先生のミニチュア」でなく、それぞれに独自の「研究の城」を築いてこられました。「師を目指すこと」と、「師の目指しているものを目指すこと」はちがうということを自分は学んできたので、それを大切にしています。
竹田 「真髄をついた研究こそが重要だ」と岸本先生が言っておられたことがありました。樹木でたとえると、枝葉に目をつけたような研究が多くなりがちななか、根幹になるような研究をしなければ分野の発展性はないということと捉えています。幹になるような研究を志すということだけは、常に考えています。
岸本 今日はさまざまなお話をお二人からお聞きすることができました。ありがとうございました。
(2022年6月発行のLF News No.96に掲載)
EYES
「黄金時代」を確実に継承する
21世紀の免疫学
神経系や代謝系との連関に光を当てる
腸管恒常性を維持する
分子の発見・同定と機構解明も
欧州を源流とする免疫学
日本でも発展
感染症などに一度かかると、二度目は軽く済んだり、かからなくなったりします。「疫病を免れる」の意味から「免疫」とよばれています。
免疫のさまざまな現象・機構を解明するための学問が「免疫学」です。世界を俯瞰すると、その先駆とされるのが英国の医師エドワード・ジェンナーです。ジェンナーは、牛痘にかかった人は天然痘にかからないという話を聞き、長年そのしくみを研究し天然痘を予防することに成功しました。そして、1798年にこの成果を論文発表しました。
さらに、フランスの化学者・微生物学者ルイ・パスツールは1879年、ニワトリコレラ菌の弱毒変異株をニワトリに接種することにより、ニワトリコレラの感染を予防することに成功しました。ジェンナーが天然痘の予防のヒントを得た牝牛(vacca:ラテン語)にちなみ、パスツールは免疫のしくみを用いた予防製剤を“vaccin”、その接種法を “vaccination”とよぶことを提案しました。
一方、日本では、北里柴三郎氏が1880年代後半、ドイツの留学先のロバート・コッホの研究室で、破傷風の免疫研究を進めました。1890年、北里氏はおなじくコッホに師事していたドイツのエミール・ベーリングと論文「動物におけるジフテリア免疫と破傷風免疫の成立について」を発表します。日本の免疫学の歩みが始まりました。
20世紀後半になると、1960年代に免疫のしくみを担うT細胞やB細胞といったリンパ球が発見され、細胞を研究対象とした免疫学がさかんになっていきます。こうした中で、日本の免疫研究者たちが数々の研究成果を出し、世界の免疫学の進歩に大きく寄与してきました。
1966年には、米国デンバー小児喘息研究所に所属していた石坂公成・照子夫妻が、免疫グロブリンE(IgE:Immunoglobulin E)の発見を報告します。免疫グロブリンは、抗体の本体に該当するもので、現在ではIgG、IgM、IgA、IgD、IgEの5種類に分類されています。
また1970年代中盤、スイス・バーゼル免疫学研究所に所属していた利根川進氏が、抗体をつくり出す免疫グロブリンのDNAが、みずから構成を再配列するしくみを明らかにしました。利根川氏は1987年、「抗体の多様性生成の遺伝的原理」で日本人初となるノーベル生理学・医学賞を単独受賞しています。
大阪大学の免疫学
継承される研究の系譜
日本国内からも、免疫学の歩みにおいて特筆すべき研究成果が次々と起こりました。とくにその牽引役となってきたのが大阪大学です。そこには「師から弟子へ」と表現するにふさわしい、研究の継承があります。
大阪大学名誉教授・元総長で、千里ライフサイエンス振興財団設立準備委員会の会長もつとめた山村雄一氏は、1970年代、免疫療法の研究を進め、結核予防用ワクチンBCG(Bacille de Calmette-Guérin)から免疫活性剤である細胞壁骨格成分(CWS:Cell Wall Skeleton)を開発しました。
山村氏に師事したのが、千里ライフサイエンス振興財団理事長の岸本忠三氏です。岸本氏は、1986年、B細胞が抗体をつくるために、T細胞からでる因子の一つ、インターロイキン-6(IL6:Interleukin 6)の遺伝子を発見。この成果は、IL-6の異常放出で生じる関節リウマチなどに対する治療薬「トシリズマブ」(商品名「アクテムラ」)の開発につながっています。岸本氏は、山村氏の助言により、米国ジョンズホプキンズ大学に所属していた石坂公成氏の研究室に留学してもいます。
さらに、岸本氏に師事した審良静男氏が、自然免疫に関する解明を進めました。自然免疫の細胞である樹状細胞の受容体が、特定の病原体の侵入を感知し、生態防御につなげるしくみに深く関わっていることを明らかにしました。その受容体は「トル様受容体」(TLR:Toll-like Receptors)とよばれています。
1970年代から90年代ごろの、免疫学が目覚ましく発展した時期は「免疫学の黄金時代」とも評されています。紹介した研究者たちが、この黄金時代の構築に貢献したのは言うまでもありません。
免疫セマフォリンから
免疫と神経・代謝との連関を解明
さらに、21世紀に入っても、岸本氏や審良氏らが築いた「大阪大学の免疫学」を継承する研究者たちが活躍し、免疫学を前進させる成果を出しています。その代表的な存在が、4ページから、岸本氏とともに鼎談に登場する、熊ノ郷淳氏ならびに竹田潔氏です。両氏とも、「岸本門下生」として免疫学研究の歩みをスタートさせ、以降この分野を牽引してきました。
熊ノ郷氏は、免疫系における「セマフォリン」とよばれる分子群の応答制御機構の解明をすすめてきました。セマフォリンファミリーは1990年代初頭、生命の発生過程で神経の進むべき方向性を決定する「ガイダンス分子」として同定された分子群です。そして、菊谷仁氏(大阪大学名誉教授)の下で免疫不全症に関する研究をしていた2000年、免疫応答に必要な副刺激分子として知られるCD40シグナル関連遺伝子として、「セマフォリンCD100/Sema4D」を同定し、セマフォリンの免疫系における役割を見出しました。
さらに、免疫系で機能するSema3AやSema4Aなどをはじめとするセマフォリン分子(Sema3A、Sema4A、Sema4B、Sema4G、Sema4F、Sema6A、Sema6B、Sema6D、Sema7A)を次々と見出します。これらは現在「免疫セマフォリン分子」とよばれています。
免疫セマフォリン分子にはそれぞれ特徴があります。たとえば、Sema3Aは、樹状細胞の所属リンパ節への遊走をガイドする役割が見出されています。また、Sema4Aは多発性硬化症の患者において血液中の量が増えるため、自己免疫疾患である多発性硬化症のマーカーとして応用されています。さらに、熊ノ郷氏は、Sema6Dが代謝調節の鍵分子の発現を調節しているなど、セマフォリンの代謝系への関与も明らかにし、「神経・免疫・代謝連関」の概念を提唱。免疫系と、神経系や代謝系といったほかの生命維持システムとのつながりに光を当て、免疫学をより高いステージに発展させています。
タンパク質Lypd8に着目
腸管恒常性維持のメカニズムを解明
一方、竹田氏は、岸本氏からの推薦で審良氏に師事し、免疫細胞が腸内細胞を攻撃してしまうことで腸に炎症を起こす「炎症性腸疾患」について研究するなかで、「なぜ健康なヒトでは腸内細菌が免疫細胞により異物と認識されないのだろうか」といった素朴な疑問をもとに、そのメカニズムの解明を進めます。そして、腸内細菌と腸管組織を隔てる腸管上皮細胞がバリア機能をもっているという仮説に立ち、遺伝子欠損マウスなどを用いて、「Lypd8」というタンパク質が細菌の鞭毛に結合してその運動性を抑制することを見出し、腸管恒常性の維持に関与することを明らかにしました。
竹田氏はさらに、腸内細菌依存的に腸管内で増加するアデノシン3リン酸(ATP:Adenosine tri-phosphate)が、腸管特有の自然免疫細胞を活性化し、炎症性T細胞(Th17細胞)を誘導することや、腸内細菌がつくり出す乳酸とピルビン酸が、マウス小腸のマクロファージの樹状突起の伸長を誘導し、腸管内の抗原の取り込みを促進し、獲得免疫応答を増強することを見出しました。これらの腸管恒常性を維持するメカニズムの解明により、炎症性腸疾患の治療法開発への応用も期待されています。
鼎談記事では、「大阪大学の免疫学」が世代を超えて脈々と継承されて発展していく様子を追うことができます。