LF対談
サイトカインを軸に据えれば、
血液学の研究を進められると感じました No.87(2019.6)

大阪大学大学院 生命機能研究科/医学系研究科・医学部 幹細胞・免疫発生研究室 教授
長澤丘司 氏
公益財団法人 千里ライフサイエンス振興財団
岸本忠三 理事長
サイトカインの観点から、血液の研究を志す
岸本 それでは、まず2019年の日本学士院賞の受賞おめでとうございます。
長澤 どうもありがとうございます。
岸本 先生は、大阪大学細胞生体工学センターの僕の研究室の大学院生そしてポスドクでしたね。大阪大学にくる前は名古屋大学の医学部で学んでこられた。僕の研究室に入られたのは、どういった経緯でしたか。
長澤 はい、私は血液学を研究したいと思っていました。たしかに名古屋大学も、戦前に東京帝国大学から移ってこられた勝沼精蔵先生の業績があり、血液学の研究が非常にさかんなところです。ただ、私は「医学の発展にも寄与するような研究をしたい」とも考えていたんです。名古屋大学の先生たちからは「阪大は分子生物学が進んでいる。最先端の研究をしたいなら阪大の研究室を探しては」と言われました。そこで調べてみると、岸本先生のチームがサイトカインの研究を世界的にリードしていると知りました。私が名古屋大学を卒業する前年の1986年は、岸本先生がインターロイキン6(IL6)をクローニングした時期でもあり、新聞記事なども目にしました。私は、ホルモンは血液とあまり関係ないだろうと思っていましたが、おなじ液性因子のサイトカインには新鮮な印象を持っており、「サイトカインを軸に据えれば、血液学の研究を進められるのではないか」と感じました。
そこで、「ぜひ岸本先生の研究室でサイトカインの研究をしたい」と考え、大阪大学医学部出身の先生に相談すると、「あんなトップのところに行きたいだなんて、軽々しく言うことじゃない。まずは、岸本先生に関連のある阪大医学部附属病院の『第三内科』で臨床研修をするといい」と言われ、そうすることにしました。
岸本 その臨床研修の期間を経てから、僕の研究室に入られたわけですね。僕はまだ覚えているけれど、長澤先生は自転車に乗ってナップサックを背負ってという出で立ちで「なんや。おかしな格好のやつがきたなぁ」と思っていました。そして、「この研究室入りたいと思うが、IL6の研究はしたくない。自分は自分のことをやりたい」と言ってましたね(笑)。
長澤 ええ……。やはり「自分は血液のことを研究したい」という気持ちが強くて、そうした発言をしたのではないかと思います。詳細は覚えていませんが(笑)。
岸本 そうですか(笑)。でも、研究者たちがみんな細胞を対象に造血系の研究をしていたなかで、サイトカインから着手したというのは長澤先生にとってもよかったのとちがいますか。
長澤 はい。その通りだと思います。
いち早くノックアウトマウスを利用し、B細胞の増殖メカニズムを解明
岸本 それで、血液細胞のなかでも、リンパ球のひとつであるB細胞に着目し、B細胞がどうつくられるかを研究しようとしたんでしたね。
長澤 はい。さまざまな血液細胞をつくるもととなる造血幹細胞そのものは、欧米の血液学の錚々たるグループがすでに活発に研究していました。そこで、私は、B細胞も骨髄でつくられ、かつ、免疫系の中心的細胞でもあるので、この細胞がつくられる環境について、分子の観点から研究しようと考えました。
岸本 それで、骨髄の細胞を培養して、そこからB細胞をつくる因子をとろうとされた。
長澤 はい。じつは当時、未分化なB細胞であるB前駆細胞が造血幹細胞からつくられる際、はじめはストローマ細胞という細胞との接着を担う接着分子が支えているという説が有力でした。でも、私はサイトカインに興味があり、その役割を担うのはサイトカインではないかと考えていました。そこで、ストローマ細胞のすぐ上に、細胞間の接着は遮断するがタンパク質だけが通る穴があいているフィルターを置き、その上側で骨髄の血液細胞を培養しました。何もおこらないのであれば、みなが言うように接着因子が大事やと。すると、B前駆細胞は増えていきました。それで「B前駆細胞を増やすのは接着分子でない。未知のサイトカインがあるはずだ」と確信しました。
岸本 私は横目で「なにやらがんばっとるなぁ。まぁ、やりたいようにやればいい」と見守るぐらいでしたが、サイトカインを見つけようとしていたんですね。ただ、長澤先生が見つけようとしていたサイトカインも含め、当時は本庶佑先生が研究を進めていて、片っ端からサイトカインをクローニングしていました。本庶先生は、なかでも2018年のノーベル賞でも話題となったPD-1の解明をとくに進めました。一方の長澤先生は、SDF-1というサイトカインがB細胞を増やすのではと考え、その解明を進められた……。
長澤 はい。SDF-1は、現在はCXCL12とよばれているサイトカイン分子ですが、たしかに発見したのは、本庶先生のチームでした。それでも、私はSDF-1の機能を解明しようと研究をしてきました。
なかなか決め手が見つからなかったとき、アメリカで開発された遺伝子欠損(ノックアウト)マウスの技術を岸本先生がちょうど導入されました。それで「SDF-1の遺伝子を欠損させたとき、B細胞がどうなるかをこの技術を使って確かめるしかない。結果いかんでは、自分が研究を続けられるかどうかも決まる」と決心して取り掛かりました。
すると想定どおり、SDF-1欠損マウスの骨髄では、B細胞の数が非常に少なくなりました。これでSDF-1は、B細胞の増殖を支える役割をもっているという確証が進みました。岸本先生から「長澤、SDF-1の機能を見つけたのは価値あることや」と言っていただけたのを覚えています。
岸本 そうでしたね。その研究成果を機に、長澤先生はさらにいろいろなことを解明していきましたね。『ネイチャー』にも論文が載って一気に長澤先生の名が知られるようになって……。
長澤 いま言った実験の結果に満足はしていましたが、さらにその解析過程で、B細胞だけでなく、骨髄の白血球全体の数が非常に少なくなっていることがわかりました。血球は、固体発生初期では肝臓でつくられ、その後、骨ができると骨髄でつくられるようになります。つまり、血球をつくる造血幹細胞が、肝臓から骨髄へと移動・定着するわけですが、このプロセスにも、SDF-1が大事な役割をもっていることを明らかにすることができました。1996年の『ネイチャー』に岸本先生たちと共著で論文を発表させてもらいましたが、造血幹細胞の研究者たちが探し求めていたものだったので、結果的に高い評価を得たのかもしれません。
岸本 そのとき長澤先生はすでに母子保健総合医療センターに移っていましたね。さらにどんな研究をしましたか。
長澤 今度は、SDF-1つまりCXCL12の受容体を特定することを目指すようになりました。B細胞の前駆細胞で高発現しているオーファン受容体として、すでにクローニングされているCXCR4に着目しました。この欠損マウスにCXCL12の遺伝子欠損時とおなじ表現型が出たため、CXCL12がリガンドで、その受容体がCXCR4だと解明することができました。
その後も、免疫系を徹底的に調べようということで、当時、京都大学にいた西川伸一先生から「パイエル板を見たらどうや」と言われ、ノックアウトマウスを用いて、パイエル板のある腸を見ていると、腸の血管がないことに気づきました。それで、CXCL12とCXCR4が腸の血管形成にも重要だということを発見しました。1998年のことです。
岸本 さまざまな成果を上げて、京大の教授になられたわけですね。いつでしたか。
長澤 2002年に、京都大学に移りました。CXCL12とその受容体CXCR4は、腸管という特定の臓器での血管形成に重要とわかったため、その後「臓器によって血管形成に必要な因子は異なる」というコンセプトが生まれました。そのときの『ネイチャー』の論文を評価していただいたことなどから、京都大学に呼んでいただいたと後で聞きました。
造血幹細胞を維持するニッチはCAR細胞が担っていた
岸本 その後、CXCL12をつくる細胞がどんなもので、さらにその細胞が造血系にどれだけ関わっているのかといったことを、長澤先生は解明していかれますね。骨髄で造血を担う幹細胞は分裂すると半分は自身と同じで個数を保ち、半分は赤血球や白血球などの血球に分化していく。研究者たちは、そうした造血幹細胞の働きを保つための細胞がどんなものかを突き止めようとしていったとも聞きます。
長澤 そのとおりです。造血幹細胞を維持する場所を「ニッチ」と呼びますが、一体、造血幹細胞ニッチをつくる細胞はなんなのかは大きな課題でした。
まず2003年、アメリカの研究チームが、Nカドヘリンという接着分子を高発現する骨芽細胞の一部が造血幹細胞ニッチをつくるとする論文を発表しました。折しも、世界の研究者たちは「造血幹細胞の数は少ないから、そのニッチとなる細胞の数も少ないだろう」と思い込んでおり、骨芽細胞の一部がニッチだとする説はその思い込みにも叶うものでした。
岸本 でも、長澤先生は、骨芽細胞の一部でなく、ほかの細胞がニッチなのだということで研究を進めてこられたわけですね。それが、さっきのCXCL12をつくる細胞というわけですか。
長澤 おっしゃるとおりです。CXCL12を高発現する突起をもった細網細胞ということで、この細胞を「CAR細胞」(CXCL12-Abundant Reticular Cells)と呼んでいます。当初、私はCXCL12を骨髄で発現させる細胞がなにであるかを解明しようとしていたわけですが、よい方法が見つからず困っていました。そうしたなか、血管を研究していたことから、たまたま発生生物学の研究者たちの集まりに加わっていたんです。そこである日、ショウジョウバエの研究者が緑色蛍光タンパク質(GFP)の遺伝子を特定の遺伝子座に挿入して、その遺伝子を発現する細胞のみを光らせる画像を示していたのです。そこで初めて、GFPを用いたこの様な手法を知りました。
岸本 GFPは2008年にノーベル化学賞を受賞された下村脩先生が発見したタンパク質ですね。これを使うと、特定の遺伝子を発現する細胞のみを緑色に輝かせられるという……。
長澤 そうです。ただちに私もCXCL12を発現する細胞のみを光らせるようにしてみました。するとCXCL12が、とりわけ骨髄で非常に高く発現しており、骨髄においてのみCXCL12を高発現させる特殊な細胞があるのだということが分かったわけです。さらに、造血幹細胞の大部分がCAR細胞と接着していました。
岸本 その細胞こそが、骨髄のなかで造血幹細胞を守るニッチを形成するCAR細胞だというわけですか。
長澤 そのとおりです。けれども、私のこの考え方は研究者たちの「思い込み」のなかではじめ無視されていました。2006年に私が『イミュニティ』という雑誌に論文を出したときも、まだ多くの研究者が半信半疑のようでした。しかし、2010年に骨髄でCAR細胞を薬剤で選択的に殺すと造血幹細胞が減少し造血が凄く障害されることを示し、自分たちの説を証明しました。さらに2012年、アメリカのショーン・モリソンらが、造血幹細胞の維持に必須のSCFというCXCL12とは異なるサイトカインの遺伝子をCAR細胞で欠損させたところ、造血幹細胞の数が低下したと論文で報告しました。これらにより、骨芽細胞の一部がニッチを形成すると考える研究者はかなり減りました。
岸本 長澤先生のCAR細胞が造血幹細胞ニッチだということが、世界で広く認めらるようになっていったわけですね。
長澤 そのように考えています。

長澤丘司 氏
大阪大学大学院 生命機能研究科/医学系研究科・医学部 幹細胞・免疫発生研究室 教授
1961年、滋賀県生まれ。87年名古屋大学医学部卒業。大阪大学医学部附属病院第三内科研修医を経て、同大学細胞生体工学センターへ。岸本忠三教授(当時)の研究室に在籍し、93年同大学医学研究科博士課程修了(医学博士)。日本学術振興会特別研究員を経て、95年大阪府立母子保険総合医療センター研究所免疫部門主任研究員。98年同部門部長。2012年京都大学再生医科学研究所生体システム制御学分野教授。16年より現職。17年同大学世界最先端研究機構免疫学フロンティア研究センター教授を併任。18年京都大学名誉教授。専門分野は免疫学、血液学、幹細胞生物学。造血幹細胞と造血、また骨を維持する骨髄微小環境(ニッチ)の解明などで世界的に知られる。1998年第1回日本免疫学会賞、2014年武田医学賞、19年学士院賞を受賞。
転写因子の働きにより
CAR細胞は骨芽細胞や脂肪細胞に
岸本 長澤先生は、発見したCAR細胞をめぐって、さらにおもしろいことを見出してきましたね。造血だけでなしに、骨や脂肪細胞をつくることにもCAR細胞は深く関わっていたという……。
長澤 はい。CAR細胞の性質をさらに解析していったなかで見つけられたことです。
以前から、骨髄には骨芽細胞や脂肪細胞のもととなる細胞があると知られていたので、培養系を調べてみました。すると、CAR細胞は脂肪細胞に分化する培養系では脂肪細胞になり、骨芽細胞に分化する培養系では骨芽細胞になったのです。
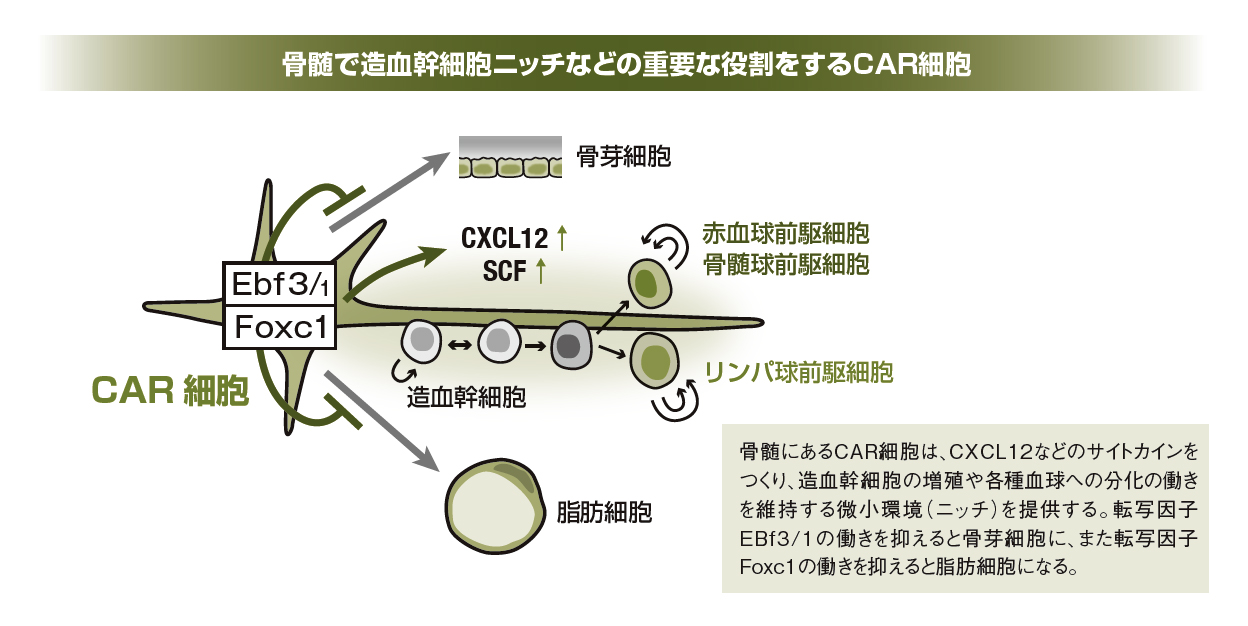
しかし、当時はそういう能力を持った細胞は体の至るところにあるということになっていました。それで私たちはなぜ骨髄のCAR細胞が特別か明らかにしたいと。そこでCAR細胞と骨芽細胞の遺伝子発現を精査して、CAR細胞で特異的に発現している、Foxc1とEbf3という二つの転写因子を特定しました。Foxc1を欠損させると、CAR細胞の大部分が脂肪細胞になるということがわかりました。また、Ebf3とそのファミリーの一つ、Ebf1の両方を欠損させるとCAR細胞の大部分が骨芽細胞になってしまうこともわかりました。体のほかのどこにも発現していない特徴的なFoxc1とEbf3という転写因子を特定し、これらの作用が欠損することでCAR細胞が脂肪細胞や骨芽細胞に分化するということがわかったのです。
岸本 逆に、その二つの転写因子が働くことで、造血の働きが保たれるともいえるのですね。
長澤 そのとおりです。
この研究では、特異的な転写因子を発見できたため、CAR細胞だけに印をつけ、それがどんな細胞を生み出すかを見ることができるようになりました。この方法を利用して、骨芽細胞はすべてCAR細胞が生み出しており、骨を維持するのに必須であることも証明できました。
CAR細胞の発生や疾患への関与のしくみ、
間葉系幹細胞の実態を解明していきたい
岸本 2016年、再び大阪大学に戻ってこられました。僕の研究室を訪れてから30年なんですね。今後、長澤先生の研究はどう発展していくのでしょう。
長澤 いまは大きく三つほど考えています。
一つは、CAR細胞が生体でどう発生するかを解明することは大切だと考えています。
岸本 わかってきたことはありますか。
長澤 個体発生の過程で、軟骨を囲む軟骨膜という組織からCAR細胞が生じるということが推測されています。では、軟骨膜という未分化な細胞からどうやってCAR細胞ができあがるのか。そのメカニズムを解明することが大事になると考えています。
岸本 なるほど。二つ目はどうでしょう。
長澤 白血病など血液系の難病の進展において、CAR細胞がどう関わっているのかを解明できればと考えています。白血病をはじめとする血液細胞疾患の病態は、当然ながら環境のなかで発展していきます。しかし、その環境については、なにを調べればよいのかわからず、研究が止まっている状況です。
岸本 骨髄性白血病とCAR細胞は、どのように関わっていそうなのでしょうか。白血病といったら、病気の白血球が無制限にただ増えていくというイメージをもちますが。
長澤 骨髄性白血病のなかでも、慢性白血病や、白血病の前段階の骨髄異形成症候群といったものは、スピードが遅いにもかかわらず進行していきます。それはなぜなのか。アメリカの専門家との共同研究でわかってきたのは、慢性骨髄性白血病をもたらす白血病細胞は、CAR細胞に対してCXCL12の発現を下げるように変化させているということです。CXCL12の発現が低下すると、白血病を生みだすがん幹細胞が増え、正常の造血幹細胞は減ってしまいます。これらのニッチのメカニズムを解明して、白血病の進行にとって都合の悪いように環境を変化させることで、病気の進行をより遅らせることができるのではと考えています。
岸本 白血病をもたらすがん幹細胞の働きを抑えるというわけですね。三つ目の研究というのは……。
長澤 間葉系幹細胞の実態を解明していくことです。私どもが解明したCAR細胞は、広くは間葉系幹細胞とよばれる細胞のひとつです。最近、腸や肺においても組織幹細胞があることがわかり、その幹細胞を支えるニッチをつくる細胞もやはりCAR細胞と同じような間葉系幹細胞の一種だろうということがわかってきました。ですので、組織幹細胞を育てる間葉系幹細胞を全身において捉えることができるのではないかと考えています。
岸本 今後も発展していきそうですね。長澤先生のますますのご活躍を期待しています。今日はありがとうございました。
EYES
骨髄での造血を維持する微小環境の解明 サイトカインから細胞、その転写因子へ
脂肪細胞や骨芽細胞の供給源にも……
CAR細胞の多様な働き
動物の骨の中心にある骨髄では、たえず血液がつくられています。ヒトを含む哺乳類の血液は、血球とよばれる細胞や血小板と、血漿とよばれる液体成分からなっていますが、とくに血球については、赤血球が酸素を運んだり、また各種の白血球が食菌や免疫作用を担ったり、さらに血小板が血液凝固のはたらきをしたりと、生命維持などに重要な役割がさまざま知られています。
これら赤血球、白血球、血小板などの供給源に当たるのが「造血幹細胞」です。造血幹細胞はみずから分裂をくりかえして増殖するとともに、前駆細胞などの段階を経て、赤血球、白血球、血小板などの細胞に分化していきます。
ヒトの造血幹細胞は、胎児期に大動脈周囲に生じ、やがて肝臓で活発に増殖しますが、その後は骨髄に移住(移動・定着)し、血球をつくりつづけます。
どうして造血幹細胞が骨髄にあるのか。それについては「骨髄にある造血幹細胞ニッチ」との深い関わりがいわれています。「ニッチ」とは「微小環境」のこと。それぞれの組織幹細胞はニッチにより維持され、また細胞数や増殖・分化が調節されていると考えられています。
研究者たちは1970年代から、造血幹細胞ニッチの存在に関心をもち、その正体やメカニズムを解明しようとしてきました。2003年には、米国の研究者が骨芽細胞の一部が造血幹細胞ニッチを構成していると発表し、一時期はこの説が広まりました。
しかし、現在では、別の細胞が造血幹細胞ニッチを構成していると考えられています。その細胞は「CAR細胞(CXCL12-Abundant Reticular細胞)」といいます。CAR細胞は、CXCL12とよばれるサイトカインを豊富に産生し(CXCL12-Abundant)、かつ網状(Reticular)の形態をしていることから名づけられました。
CAR細胞を発見するなど、造血幹細胞ニッチのしくみを詳しく解明したのが、対談記事に登場する長澤丘司氏です。長澤氏は1990年代より、サイトカインのSDF-1/CXCL12が白血球のひとつであるB細胞(Bリンパ球)の増殖を促進することを見出していました。また、CXCL12の受容体がCXCR4であることも証明しました。
そして2006年、骨髄において、CXCL12を大量につくっている網状の細胞を見出したのです。これがCAR細胞です。大部分の造血幹細胞がCAR細胞と接着していることなどから、長澤氏はCAR細胞こそが造血幹細胞ニッチを構成していると提唱。以降、国内外で広まっていたニッチは骨芽細胞だとする説は覆っていきました。
さらに長澤氏はCAR細胞の働きを詳細に研究。その結果、骨芽細胞や脂肪細胞の供給源となる間葉系幹細胞であることも解明しました。
CAR細胞が発見・解明されたことを機に、造血のメカニズムやその応用の研究はさらに進みました。長澤氏は、CAR細胞をもたらすものはなにかという謎についても解明に挑み、転写因子のFoxc1やFbf3/1がCAR細胞の維持などを制御していることも見出しました。医療への応用可能性という点では、骨髄性白血病をはじめとする血液の病気の深い理解やさらなる治療法開発への土台も築かれつつあります。
現在も、造血幹細胞ニッチがどのようなメカニズムで形成されるのか、造血幹細胞や免疫細胞がどのように維持・調節されるのか、また、幹細胞ニッチが血液・免疫・骨・代謝疾患の病因・病態にどのように関与しているのか、といった根源的な部分を明らかにするための研究が、長澤氏により進められています。