LF対談
Keap1-Nrf2系は、鋭敏なしくみを つくりあげているといえます。
No.89(2020.2)

東北メディカル・メガバンク機構 機構長/東北大学大学院医学系研究科 教授
山本 雅之 氏
公益財団法人 千里ライフサイエンス振興財団
岸本 忠三 理事長
転写因子Nrf2に次ぎセンサー分子Keap1を発見
岸本 本日は、山本雅之先生が発見・解明されたKeap1-Nrf2系を中心としたストレス応答のご研究についてと、いま先生が主導されている「東北大学 東北メディカル・メガバンク」の取り組みについて、お聞きしていきたいと思います。まず、Keap1-Nrf2のご研究については、どのような経緯で進められたのですか。
山本 赤血球などに含まれるヘムについての研究が原点にありました。東北大学大学院の医学研究科にいた時期、菊地吾郎先生からヘムの生化学を研究するようにとご指導いただきました。
ヘムは約8割が赤血球系の細胞においてつくられますが、残りは脳や肝臓などほかの部位でつくられます。赤血球でヘムをつくる酵素は特異的であり、ほかの部位でヘムをつくるハウスキーパー型の酵素とはちがうのだということを1985年に明らかにしました。では、どうして赤血球でのみ発現する遺伝子があるのでしょうか。遺伝子の細胞特異的な発現制御を決めるしくみはどうなっているのでしょうか。こうしたことに興味が移ってきました。
当時は転写因子のハンティング競争も起きていました。そうしたなか、赤血球に特異的な遺伝子発現を規定する転写因子群を1989年に見つけることができたのです。「GATA因子群」とよばれているものです。
岸本 たしか先生は「GATA」とはべつの名前をつけておられたのですよね。
山本 はい。論文には「NF-E1(Nuclear Factor-Erythroid 1)」と書いたのですが、米国ではハーバード大学やNIH(国立衛生研究所)のチームが、英国ではオックスフォード大学などのチームが研究を進めており、共通で「GATA-1」と呼ぶということになりました。科学研究における競争の厳しさを実感しました。
岸本 その後、Keap1-Nrf2系発見への道のりはどうでしたか。
山本 NF-E1(GATA-1)認識配列の隣にある遺伝子配列に結合する「NF-E2」という因子も赤血球の遺伝子発現を規定するということを明らかにしました。このNF-E2を同定したことが、Keap1‐Nrf2系の発見につながったのです。NF-E2因子群のなかで酸素毒性に対する応答に関わる因子として、まず転写因子のNrf2を見つけることができました。
岸本 どのようにNrf2の機能を見つけたのですか。
山本 Nrf2ノックアウトマウスをつくったとき、そのマウスが毒物や活性酸素種の刺激に対して反応しないということから見つけることができました。細胞が酸化ストレスを受けたり、多環芳香族の毒性分子に近づかれたりすると、普段は分解されてしまうNrf2が蓄積するようになり、細胞核で標的遺伝子の発現を誘導し、抗酸化タンパク質や解毒酵素などの誘導をもたらします。
岸本 さらに、そのNrf2を制御するタンパク質として……。
山本 Keap1を発見したということになります。Keap1は、Nrf2と直接結合して分解にもっていく因子です。けれども酸化ストレスや毒性分子を感知すると、Keap1はNrf2を壊すのを止めます。それでNrf2が増え、転写因子としてはたらくというしくみになっています。
私がKeap1-Nrf2系を発見する前段として、親電子性分子や環境毒物に対する生体応答に関する長い研究の歴史がありました。米国ジョンズ・ホプキンス大学のポール・タラレー先生や競合する研究者たちが、電子をほしがる性質をもった物質(親電子性分子)こそが真の化学発がん剤なのだということを突き止めるなど、素晴らしい生化学・毒性学の研究が進んでいました。そうした一連の研究のなかで、私が見つけたKeap1-Nrf2系は、多くの方が探し求めていた転写因子であり制御系でした。これら研究の蓄積こそが、自分自身の研究の発展を支えてくれてきたものだと考えています。
岸本 解毒という点では、AhR(芳香族炭化水素受容体:Aryl hydrocarbon Receptor)という転写因子のはたらきについてもよく聞きます。これと、Keap1-Nrf2系とではどうちがいますか。
山本 解毒の過程において、AhRはシトクロムP450の制御を主にしています。そして、P450の代謝産物をさらに転移酵素群、例えば、グルタチオンS-トランスフェラーゼやグルクロン酸転移酵素、硫酸転移酵素などが水溶性にします。これらの転移酵素群の発現の方をNrf2が制御します。
つまり、まず第1相としてAhRがシトクロムP450の制御をし、つぎの第2相でNrf2が転移酵素などを制御するという、きれいな役割分担ができています。
合わせ鏡のような酸化ストレスと低酸素ストレスの応答機構
岸本 先ほどの、常にKeap1がNrf2を壊しているというお話を聞いて、よく似ているなぁと思ったのが、今年(2019年)のノーベル医学・生理学賞で話題になった「低酸素応答」のしくみです。酸素が十分あるときは、HIF1αという転写因子が常に壊されているけれど、低酸素になるとHIF1αが壊されず核内に移って、低酸素応答にかかわる遺伝子群の転写を活性化させるのですよね。
つまり、常にすみやかに壊されている転写因子が壊されずに増えてはたらくという点では、山本先生のNrf2もノーベル賞のHIF1αも共通していますね。
山本 まさにそうなのです。酸化ストレス応答を研究する私どもと、低酸素ストレス応答を研究する人たちが、まったく別々にしくみを追究していったら、じつは似ていたというわけです。
Nrf2にしてもHIF1αにしても、合成されてはすぐに壊されてしまうので、経済的には無駄なことをしています。
岸本 どうして、無駄に思えるしくみがあるのでしょう。
山本 急激な環境変化にあっても、それに対応する遺伝子発現の応答が素早くできるからだと考えます。このようなしくみにより、酸化ストレスや低酸素ストレスが生じたとき、転写因子のメッセンジャーRNAをつくってタンパク質にするという段階をスキップすることができます。経済性を犠牲にして、迅速なストレス応答のしくみを獲得しているのです。
岸本 酸素が多いときと少ないときとで、真逆のようなしくみではたらく転写因子の組み合わせというのは、他にもあるのですか。
山本 これほどきれいに鏡のようなイメージではたらいているというのは、これだけだと思います。本当に学術の世界でユニークな成果になったと思います。
岸本 では、Nrf2とHIF1αのしくみで、ちがう点はなにかありますか。
山本 ストレス感知のメカニズムがちがいます。Keap1-Nrf2系の方が鋭敏なしくみをつくりあげていると考えています。
岸本 と、おっしゃいますと……。
山本 まずHIFの場合は、プロリン水酸化酵素の基質にあたる(分子状)酸素そのものの濃度低下が感知の対象となっています。しかし、基質は酵素にくらべて過剰にありますから、基質の量的変化を感知するセンサーというのは、酵素反応速度論のミカエリス・メンテン式から考えてもあまり効率が良いとはいえません。
これに対し、Nrf2の場合には、活性酸素種を酵素にあたるKeap1に含まれるシステインの酸化修飾を通して感知するということが、最近の私どもの研究でわかりました。過剰にある基質ではなく、量のかぎられた酵素の修飾を感知するので、こちらのほうがセンサーメカニズムとしては良くできていると思っています。
医薬品への応用も続々と宇宙ストレスの軽減にも
岸本 Nrf2は、毒性物質などを防御する遺伝子の転写を活性化させるわけですが、それゆえに、がんの悪性化などにもつながるとも聞きます。
山本 そのとおりです。実際、Nrf2を非常に多くもっているがん細胞があります。そのようながん細胞は、肺がんでは3〜4割にものぼります。Nrf2高活性系を獲得したがん細胞は、抗がん剤や周囲の微小環境からの攻撃を防御するようになります。それにより、がんの悪性化が生じます。
岸本 そうすると、がんについてはKeap1-Nrf2系の阻害剤というものが考えられますか。
山本 はい。2017年に化合物ライブラリーをスクリーニングしてアカデミア創薬として阻害剤を1つ見つけました。確かにそのようなNrf2活性化型のがんには良く効きます。
岸本 逆に、Keap1-Nrf2系のはたらきを誘導するような薬の状況はいかがですか。
山本 すでに認可されているNrf2誘導剤があります。フマル酸ジメチル(商品名テクフィデラ)という多発性硬化症の治療薬で、世界中で第一選択薬として使われています。 それから、糖尿病性腎症に対する利尿剤として、バルドキソロンメチルという薬があり、日本で第3相の臨床試験まで進んでいます。世界に先駆けて日本で認可されればと期待しているところです。
ところで、Nrf2誘導剤に炎症抑制の効果が見出されています。じつは、岸本先生が発見されたインターロイキン6(IL-6)の遺伝子の発現を直接抑制するのです。そこで、Nrf2誘導剤がアルツハイマー病やパーキンソン病など、炎症をともなう中枢性の疾患に対する治療薬としても臨床試験が進められているところです。
岸本 そうでしたか。Keap1-Nrf2系の研究から、さまざまな応用がされようとしているわけですね。
山本 はい。もうひとつ、ぜひ紹介したいのが、Nrf2が宇宙環境下でのストレスを軽減させるのに役立つのではないかというお話です。
岸本 宇宙、ですか。
山本 はい。宇宙放射線は酸化ストレスを誘導します。また、合わせて微少重力ストレスをNrf2が抑制するという仮説を立てました。そして2018年4月、Nrf2ノックアウトマウスを6匹と野生型マウス6匹を、米国のジョン・F・ケネディ宇宙センターから国際宇宙ステーションに送り、日本実験棟「きぼう」で31日間にわたり滞在させたのです。行き2日と帰り1日を合わせて34日間の“宇宙旅行”です。宇宙に運んだ遺伝子組換えによる病態モデルマウスを地球に帰還させたのは人類史上初めてのこと。それがNrf2ノックアウトマウスたちだったことを、とてもよろこんでいます。
岸本 どんな成果が上がりそうですか。
山本 いまお話しした宇宙ストレスの軽減の効果がありそうです。それと、宇宙で早く進行する加齢変化に対しても、抑制するような効果を得られるのではと期待しているところです。この研究は私が機構長をしている「東北大学 東北メディカル・メガバンク機構」の活動として取り組みました。

山本 雅之氏
東北メディカル・メガバンク機構 機構長/東北大学大学院医学系研究科 教授
1954年、群馬県生まれ。79年東北大学医学部卒業。83年東北大学大学院医学研究科修了。米国ノースウエスタン大学に博士研究員。91年東北大学医学部講師。95年筑波大学 先端学際領域研究センター教授。2007年東北大学医学系研究科教授。08年東北大学副学長、大学院医学系研究科研究科長・医学部長。10年東北大学Distinguished Professor。12年東北メディカル・メガバンク機構機構長。 環境発がん物質と酸化ストレスのセンサーであるKeap1と、その指令に応答する転写因子Nrf2を発見。研究目標は、複数の転写因子による協調的な生命現象調節機構の解明、また、環境ストレス適応・応答の分子機構の解明。東日本大震災後、被災地の住民たちを対象とした健康調査を含む「東北メディカル・メガバンク」の機構長として活躍。受賞は、日本学士院賞、紫綬褒章、東レ科学技術賞、上原賞、高峰記念第一三共賞、日産科学賞、つくば賞、井上賞、北米毒性学会基礎科学賞、日本腎臓財団賞など。Highly Cited Researchers 2019にも選出される。
東北の「創造的復興」目指しバイオバンクを創設
岸本 いま山本先生がおっしゃった、東北メディカル・メガバンクの取り組みについても伺います。東北地方の住民みなさんの生体試料や医療情報をもとに、バイオバンクの構築に取り組んでおられると聞きます。2011年の東日本大震災を受けて始まったとのことですが、どんな経緯でしたか。
山本 2007年に、12年間つとめていた筑波大学から東北大学へ復帰しました。そして、2008年から医学系研究科長・医学部長をつとめるようになり、その3年目に震災に遭いました。
岸本 どこで地震に遭われたのですか。
山本 東京に滞在していました。すぐ仙台に帰りたかったのですが、交通がすべて遮断されてしまっていまして。それで、知り合いの病院に貸し布団を収めている大手の業者さんに「東京の倉庫にある布団と毛布をできるかぎり貸していただけませんか。お金はあとで払います」と、お願いをしました。それで、布団と毛布を積んだトラックに同乗して翌日には仙台に帰り、寒い思いをされている方々に届けてまわったのです。震災直後から、若手の医師たちも、大学の公用車で沿岸部まで医療支援に行ってくれました。
岸本 研究科長ですと、たいへんだったでしょう。
山本 はい。電子顕微鏡なども壊れてしまい、医学系研究科全体では40億円を超える被害となりました。けれども、総長だった井上明久先生が「壊れたのを直すだけでなく、元のものを上回る『創造的復興』をしていこう。日本の将来に役立つような事業をやろう」と話されていて、それで私は東北メディカル・メガバンク計画を手がけさせていただいたのです。計画期間を経て、2013年4月から事業を始めました。
岸本 震災とバイオバンクにどういう関係があるのかと思っていましたが、震災が契機となったわけですね。
山本 はい。被災地において、コホート調査とバイオバンク構築は「一丁目一番地」の課題と思っています。宮城県だけで1万人以上、東北全体で1万8000人以上の方がお亡くなりになり、残った方々は大きなストレスを受けておられます。そうした方々のストレスと健康について調べる責任があると思って取り組んでいます。
予防と医療の「個別化」を発展させる
岸本 具体的には、どのようなことを目指しておられるのですか。
山本 「個別化予防」と「個別化医療」を発展させるということがいちばんの目的です。そのために、合計約15万人を対象としたコホート研究をおこない、調査票情報や遺伝子情報などをお預りしています。
岸本 15万人というのはどんな方々で……。
山本 約8万人は、宮城県と岩手県の地域住民の方々です。残りの約7万人は宮城県の妊婦さんや、そのご家族、そして生まれてくる赤ちゃんたち、つまり三世代にわたる方々です。英米でも三世代コホートの試みはあったもののうまくいっておらず、日本のみが成功したといってよいと思います。
岸本 成功したというのは、どんな理由でですか。
山本 一つには震災直後に始めたため、みなさんの健康に対する意識が高かったことがあると思います。もう一つは、「ゲノム・メディカルリサーチコーディネーター」という医療系スタッフが参加協力病院に常駐し、妊婦さんが来院されるたびに「ご協力いただけませんか」と直接リクルートをしたことが挙げられます。英米の場合には手挙げ方式であったため、妊婦さんは参加しにくく、また、健康に興味のある集団に偏ってしまっています。その点、私どもの研究では、悉皆性に優れたコホートをつくりあげることができたと考えています。
岸本 三世代コホート研究では、子どもたちの成長のしかたなども追跡するわけですね。
山本 はい。少子化が進んでいく日本の子どもたちを追跡する調査は、しっかりやるべきだと考えています。岸本先生もご存知のように、昔から日本人は骨格が小さいため「小さく産んで大きく育てる」といったことが言われてきました。その影響で、日本における2500グラム未満の低出生体重児の割合はOECD参加国のなかで最悪のレベルにあります。低栄養で生まれてくることが、大きくなったときの発達障害や若年性成人病などとどう関係するのか、大きな心配があります。三世代コホートに参加していただいているお子さんたちをしっかりフォローアップしていきたいと考えています。
岸本 「個別化予防」や「個別化医療」に向け、なにか見えてきたことはありますか。
山本 Nrf2関連で言いますと、一塩基多型と肺がんの罹患率の関係性が明らかになりました。Nrf2遺伝子の転写開始点から見て617ベース上流にrSNP-617という一塩基多型があります。多くの人の塩基はシトシン(C)ですが、アデニン(A)の方もおられます。父由来も母由来もアデニンというAAの方のNrf2発現量は、CCやCAの方の半分ほどしかありません。このNrf2の発現低下と肺がん発症率の関系を、国立がん研究センターの研究者たちと協力して調べたところ、普通の集団ではAAの方は5%程度であるのに対し、肺がん患者の集団ではAAをもっている方が8%程度おられることがわかりました。
この結果を見て、私が思ったのは、rSNP-617がAAである方に対しては、医師が「たばこを吸ってはいけません」と強く指示することができるということです。これが、私どもの目指している個別化予防の例です。遺伝子を見ることからできる個別化予防をやっていこうと考えました。
岸本 Keap1-Nrf2、ストレス、震災、バイオバンク。山本先生のなかではすべてがつながっているわけですね。
山本 都合よく話していけばということもありますが、たしかにしっかりとつながっていると思います。
岸本 今日はありがとうございました。
EYES
酸化ストレスや毒物に対する 生体の応答のしくみKeap1-Nrf2系を解明
治療薬の開発や新たな医療の確立にも貢献
私たちヒトを含む多くの動物は、酸素を体内にとり込んでいます。生体内でのエネルギー貯蔵、供給、運搬を仲介するATP(Adenosine TriPhosphate)の合成に酸素が必要だからです。
一方で、酸素を多くとり込み過ぎると、活性酸素種が生成し、生体内の細胞の核酸やタンパク質などで酸化反応が進み、病気や老化を引き起こすことが知られています。こうした有害な酸素が過剰にある状態を、「酸化ストレス」状態と言います。
つまり、動物は必要ではあるが有害にもなる酸素に囲まれながら生きていることになります。また、環境中にはほかにも植物由来や人工物由来の毒性のある物質が多くあり、細胞はそれらにも晒されています。
それでも動物が生きつづけられるのは、こうした酸化ストレスや毒物を感知し、これらに応答するしくみが生体内にあるからです。酸化ストレスや毒物に対して、解毒や代謝を司る生体防御遺伝子群が発現するのです。
では、そうした生体防御遺伝子は、どのようなしくみで発現するのでしょうか。
遺伝子が発現する過程では、DNA塩基配列をメッセンジャーRNAに写しとる「転写」がおこなわれます。この遺伝子の転写を制御するタンパク質が多数あることが知られ、それらは「転写因子」とよばれています。さまざまな転写因子のなかで、酸化ストレスや毒物に対する生体防御で重要な役割を果たしているのが「Nrf2」(NF-E2-related Factor 2)です。Nrf2がsMafとよばれる小因子と二量体をつくり、これが標的である遺伝子の発現をもたらします。
しかし、Nrf2は、酸化ストレスや毒物に晒されていない平常時には、迅速に分解されてしまいます。このNrf2の分解を指令しているのが「Keap1」(Kelch-like ECH-associated protein 1)というタンパク質です。
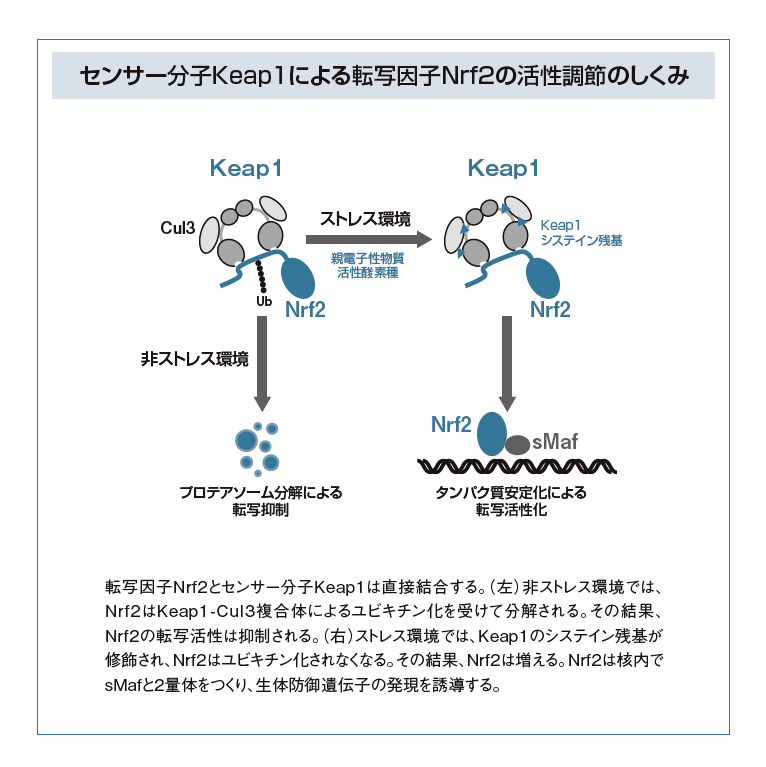
酸化ストレスや毒物のない平常時、Keap1はCul3というタンパク質と協力してNrf2のユビキチン化を促進することで、Nrf2を分解へと導きます。しかし、細胞が酸化ストレスや親電子性の毒物などに晒されたときは、Keap1のシステイン残基が修飾されて、Nrf2をユビキチン化できなくなり、Nrf2は分解されなくなります。これにより、Nrf2が増えていき、細胞核内へ移行して生体防御遺伝子の発現を誘導するようになるのです。
Nrf2とKeap1をともに発見し、Keap1-Nrf2系とよばれるこの生体防御のしくみを解明したのが、対談記事に登場する山本雅之氏です。
長らく赤血球の分化を制御する転写因子を研究していた山本氏は、赤血球の運命を決める「NF-E2」というヘテロ二量体型の転写因子の実体を解明し、その1つの構成因子の仲間として、1995年にNrf2を発見しました。さらにNrf2による活性化制御のしくみを探るなかで、1999年にKeap1を発見しました。
ついで、Keap1のシステイン残基の化学修飾と、それによるNrf2の分解抑制が、この一連のストレス感知から遺伝子誘導発現制御のしくみの基盤となっていることを解明しました。
直近の2019年にも、Keap1が親電子性毒物の感知とは異なる部位のシステイン残基で酸化ストレスを感知していることや、Keap1の酸化ストレス感知がフェイルセーフ能力を備えていることなどを発表し、精力的に研究を進めています。
山本氏のこれらの研究成果は、ストレスを原因とする病気などに対する治療薬開発などの応用にもつながっています。また、関連する遺伝子も特定されており、個人の遺伝子情報をもとに個別に予防や治療の戦略を立てるといった、新たな医療の確立にも貢献するものと注目されます。