LF対談
オルガネラに出合ったのが「私のすべて」だと思っています No.105(2025.6)

九州大学高等研究院 特別主幹教授・名誉教授
兵庫県立大学大学院理学研究科 特任教授
藤木幸夫 氏
公益財団法人 千里ライフサイエンス振興財団
審良静男 理事長
一期一会的な出会いからペルオキシソーム研究へ
審良 今日は藤木幸夫先生にペルオキシソーム研究のお話を聞けることを楽しみにしています。ペルオキシソームは、細胞小器官ともばれるオルガネラのひとつですね。いまでこそオルガネラ研究は盛んですが、先生が研究された当初はさほどでもなかったと思います。あまりほかの研究者がオルガネラを強調していなかったなか、藤木先生はオルガネラを大切にされ、発信されてこられました。
藤木 そうですね。審良先生の仰るとおりです。オルガネラに出合えたのは、正直「私のすべて」だと思っています。
審良 どのように藤木先生がオルガネラ、具体的にはペルオキシソームと出合われたのかからお聞きします。
藤木 私の研究自体は、「生物を化学という虫眼鏡で見るおもしろさ」に惹かれ、自然と「タンパク質の研究がしたい」と意識するようになり、入学した九州大学では船津勝先生の生物化学教室を選びました。博士論文「米ヌカリパーゼ1の化学構造に関する研究」で学位を得ました。
船津研究室では学位取得後は海外留学が基本路線でしたし、私自身も海外での研究に興味をもっていたことから、1976年に米国コーネル大学に留学しました。「脳下垂体ホルモンFSHの構造と機能の解明」を研究テーマにし、成果を上げることができました。
以降が、オルガネラとの出合いの話になります。1978年の暮れ、おなじニューヨーク市内ですが、マンハッタンにあるメモリアルスローンケタリングがんセンターのカフェテリアで、一人でランチをとっておいでのスタンフォード・ムーア先生をたまたま見かけました。ムーア先生は、がんセンターの向かいにあるロックフェラー大学の生化学者で、1972年にノーベル化学賞を受賞なさっています。私は教科書で2、3回見て、知っていたくらいでしたが、思い切って声をかけたのです。英語に不安はあったものの、私のコーネル大学での研究成果を伝え、「細胞生物学を研究したい」と訴えると、驚いたことに「履歴書と論文リストを送るように」と言ってくださったのです。
この出会いがきっかけとなり、1979年、同じロックフェラー大学のクリスチャン・ド・デューブ先生の研究室で研究できることとなりました。ド・デューブ先生は1974年、オルガネラの構造と機能に関する発見でノーベル生理学・医学賞を受賞なさった方です。研究室に入れたことが、私の研究におけるオルガネラとの出合いとなります。
審良 まさに一期一会ですね。運をよぶのが一期一会だと私は思いますが、藤木先生はムーア先生に声をかけられたのが素晴らしいと思います。そこで、ペルオキシソームの研究に入っていかれるわけですね。どんなことから着手されたのですか。
藤木 当時、ペルオキシソームは小胞体から出芽するという仮説がありましたので、ド・デューブ先生からの提案で、この仮説を生化学的に検証することになりました。
とはいえ「大変そうだ。どうしたら検証できるか」と思案し、「オルガネラ同士の膜を比較すればよいのでは」と考えるに至り、膜を得るための方法として、炭酸ナトリウム溶液中で氷上に30分ほど放置し、超遠心分離機にかけると膜だけが落ちてくるという方法を見出したのです。「炭酸ナトリウム法」とよんでいます。この方法で調べると、ペルオキシソームの膜組成は小胞体膜とまったく異なる組成であることがわかりました。そして、ペルオキシソームのマトリックスおよび膜タンパク質は小胞体膜結合型でなく、遊離型ポリソームで合成されることもわかりました。ポリソームは、多数のリボソームがメッセンジャーRNAでつながれたものです。さらに、新規合成ペルオキシソームタンパク質は、試験管中でペルオキソシームへ移送されることも見出しました。
6年かかりましたが、こうしてペルオキシソームに関する「生合成・翻訳後輸送・成長と分裂モデル」を提唱することができました。
ペルオキシソーム欠損症の分子メカニズムを解明
審良 藤木先生は一方で、ペルオキシソームの異常で起きる病気についても興味をもって研究にとりくまれてこられましたね。
藤木 はい。小児科医のハンス・ツェルベーガーにより、先天性の小児疾患が報告され、ツェルベーガー症候群と呼ばれました。患児は出生直後から筋緊張低下や異常顔貌を呈し、重篤な場合は乳幼児期に死亡します。1973年シドニー・ゴールドフィッシャーらはツェルベーガー症候群の患者組織ではペルオキシソームが形態的に欠損していることを報告しました。ペルオキシソーム欠損症ともよばれ、詳細を調べてみると、ペルオキシソームを構成するカタラーゼなどの要素は合成されているのに、オルガネラができないということです。ペルオキシソームの形成・構築とともに、この病気の分子メカニズムも明らかにしたいと思ったのです。
1985(昭和60)年に帰国し、明治乳業ヘルスサイエンス研究所に所属しました。会社の仕事もちゃんとするので、この病気の研究もさせて頂くということを認めてもらいました。
審良 ここで、ペルオキシソーム欠損症など病因遺伝子を解明していかれたのですね。ペルオキシソーム研究では酵母を使う研究者が多いなか、藤木先生はハムスターを使われたと聞きます。どうしてですか。
藤木 ペルオキシソームの形成や構築と、病気のしくみの両方を調べるには、哺乳類の細胞のほうが有利だと考えてのことです。変異細胞株を得やすいとされるチャイニーズ・ハムスター卵巣(CHO)細胞を用いました。
ペルオキシソーム欠損性変異細胞をいろいろと分離できたので、これにプラスミドベクターを使って遺伝子を導入し、野生型に復帰させることを考えました。オカヤマ・バーグ・ベクターの開発者として知られる岡山博人先生にファックスでその構想を伝えて相談すると、「ひょっとしたら上手くいくかもしれませんね」と言われて勇気づけられ、そのベクターにcDNAライブラリーを構築し、全体を“大プール”と称しました。
この中から“小プール”ライブラリーを一つずつ変異細胞Z65に導入し正常細胞への回復を検定します。一回のサイクルに4週間かかりましたが、“小プール”導入を繰り返した結果、野生型の細胞と同様に、ペルオキシソームに含まれる酵素カタラーゼが顆粒状に見られるcDNAのクローニングに成功し、コードされる因子を(哺乳類)ペルオキシソーム形成因子PAF1と名付け発表しました。その後、多くの必須形成因子を統一名ペルオキシン(PexまたはPEX)と称し、遺伝子をPEXと表すことになり、PAF1は酵母系を含めてPex2となりました。このCHO変異細胞と同じ相補性群の欠損症患者細胞にこのPAF1(Pex2)cDNAベクターを入れるとペルオキシソームがつくられたのです。患者PAF1(PEX2)遺伝子を調べてみると、305アミノ酸残基中119番目のアルギニンが正常な人ではCGAの塩基配列なのに、患者ではTGAの終止コドンとなっていました。こうして、ペルオキシソーム形成に必須なペルオキシン遺伝子PEX2を発見するに至りました。ペルオキシソーム欠損症病因遺伝子としては世界初の発見です。
審良 PEX2の発見を皮切りに、次々とペルオキシソーム欠損症の病因遺伝子を解明していかれたのですよね。
藤木 はい。2003年4月にPEX26を発見し、これでPEX2の発見以来、13種類の遺伝子を発見・同定し、探究完了となりました。ただし、2012年にPEX11β遺伝子変異が患者の方から見つかり、現在は14種類の遺伝子となっています。14種類のPEX遺伝子のうち、どれか一つが変異するとペルオキシソーム欠損症になるし、逆にこの14種類の遺伝子翻訳産物が集まって、ペルオキシソームというオルガネラを造りあげているともいえます。
ちなみに、ペルオキシソームに関連する病気として、副腎白質ジストロフィー(ALD)というものがあります。ABCD1遺伝子の変異により、ぺルオキシソームの膜に存在するタンパク質ABCD1に異常が生じ、神経系細胞膜の機能異常を引き起こします。1992年に公開された米国映画『ロレンツォのオイル 命の詩』という作品で扱われ、この病気に冒された息子を救うため、両親が奮闘する姿を描いた実話ベースの映画で、最終的に両親は「ロレンツォのオイル」という治療法を開発します。ALD治療に関しては、遺伝子治療の最初の事例といえるものがハーバード大学のチームにより数名の小児患者におこなわれた成功例が、2017年に報告されてもいます。
カタラーゼ研究のパラダイムシフトを起こす
審良 1994年から、学生時代を過ごした九州大学に戻られました。近年はどのような研究課題に取り組まれているのでしょうか。
藤木 ペルオキシソームに多量(16%)に含まれる酵素であるカタラーゼを題材に、その細胞内局在調節メカニズムを解明しようと取り組んできました。カタラーゼは、過酸化水素2分子から水2分子と酸素1分子ができる反応を触媒する酵素です。つまり、ペルオキシソーム内酸化反応で発生する過酸化水素を無害にする役目をもっています。
分離した多くのペルオキシソーム形成障害性チャイニーズ・ハムスター卵巣(CHO)細胞変異株のなかに、まだ相補遺伝子を明らかにできていないZP114とよんでいるものがありました。ZP114に対し原因遺伝子はなにかと根気強く調べてみると、驚いたことに、ミトコンドリア外膜タンパク質ポーリンの遺伝子VDAC2だったのです。
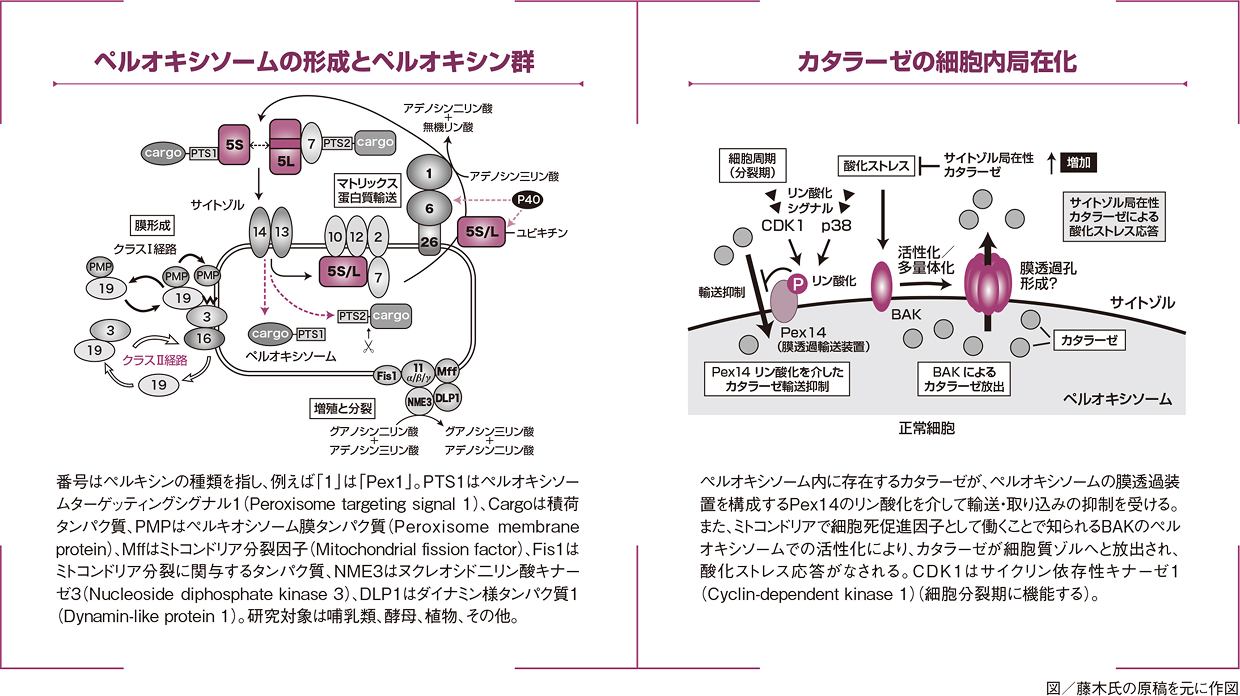
そして、VDAC2の喪失により、細胞死促進因子の一つであるBAKの局在性がミトコンドリアでなくペルオキシソームに移行していることがわかりました。多量なBAKがペルオキシソーム膜に局在化することによって新規合成されるペルオキシソームマトリクス酵素の取り込みを妨げていることが判明しました。ヒト正常細胞でも内在性のBAKは一部がペルオキシソーム膜にも局在し、外側である細胞質ゾルへのカタラーゼの放出を介在していたのです。加えて、ペルオキシソームの膜透過装置を構成するPex14がリン酸化されることにより、カタラーゼのペルオキシソームへの輸送・取り込みの抑制がなされていることもわかりました。これらにより、酸化ストレスがかかっても、細胞質ゾルで増大するカタラーゼがそれに対処しているのです。
つまり、カタラーゼのペルオキシソームから細胞質ゾルへ放出およびPex14のリン酸化によるカタラーゼの輸送・取り込みの抑制は、細胞の恒常性維持にとても重要であり、そのはたらきが破綻すると細胞死に至ることを発見しました。お蔭様で、これらのカタラーゼのオルガネラと細胞質ゾルの両局在性を軸にした生理調節作用の発見は、カタラーゼ研究のパラダイムシフトと位置づけて頂いています。
審良 カタラーゼに着目し、パラダイムシフトと評される研究を進めてこられたのですね。ペルオキシソーム欠損症の解明についても、近年、進展した点はありますか。
藤木 「この病気で患者の方は、どうして重篤な神経疾患でお亡くなりになるのか」という疑問に答えたかったのです。
そこで、さきほどPex14の話をしましたが、このPex14を欠損させたマウスをつくって調べてみました。すると、小脳プルキンエ細胞の発達が非常に悪いことがわかりました。
さまざま調べた結果を述べますと、Pex14欠損マウスでは、脳由来神経栄養因子(BDNF)が異常発現によって増加していました。一方、その受容体であるTrkBは不活性型TrkB-T1(細胞内キナーゼドメインが欠失)が主に発現・増加することで、自己リン酸化能が低くシグナル伝達活性が低下し、プルキンエ細胞の発達が悪くなっていたのです。つまり、ペルオキシソーム欠損マウスの小脳では、BDNF-TrkBシグナル系の伝達障害が起き、これによりプルキンエ細胞の形態形成の障害、樹状突起の形態異常になっていました。では、どうしてBDNFの異常発現が起きるのか。さきほど、カタラーゼの局在化を話題にしましたが、患者の方の細胞を見ると、カタラーゼは100%が細胞質ゾルのほうに局在化し、還元状態をもたらし、これによりBDNFの異常な発現上昇を誘導していたのです。
私は当初、ペルオキシソームのほうにカタラーゼが100%存在するのが通常だと思っていたのですが、以上の結果から細胞質ゾルに5~10%がいつも保たれていることが最も大事なのだという考えに至りました。これも大きなカタラーゼ研究のパラダイムシフトだと思っています。

藤木幸夫 氏
九州大学高等研究院 特別主幹教授・名誉教授
兵庫県立大学大学院理学研究科 特任教授
1948年、福岡県生まれ。71年九州大学農学部農芸化学科を卒業。76年九州大学大学院農学研究科博士課程を修了。76年コーネル大学医学部博士研究員。79年ロックフェラー大学上級研究員、助教授。85年明治乳業ヘルスサイエンス研究所主任研究員、研究室長、94年九州大学理学部生物学教室教授。99年同大学院理学研究院生物科学部門教授。2009年同主幹教授、2010年同理事・副学長。14年同名誉教授、特任教授。24年高等研究院特別主幹教授。この間、2002~07年21世紀COEプログラム拠点リーダー、07~12年グローバルCOEプログラム拠点リーダーをつとめ、21年兵庫県立大学理学研究科特任教授にも就任。専門分野は細胞生物学、生化学、分子生物学。オルガネラの一つペルオキシソームの創生機構と欠損症の研究を一貫として行い、数々の成果を挙げる。おもな受賞歴は、日本生化学会柿内三郎記念賞、西日本文化賞、武田医学賞、藤原賞、日本学士院賞、瑞宝中綬章。趣味はテニス、水泳、現在はウォーキング。
プラズマローゲンの恒常性維持に着目し、研究
審良 ペルオキシソームは、最近よく認知機能を改善するなどの効果をうたう食品に含まれる「プラズマローゲン」を合成するはたらきをもっているのですね。
藤木先生は、プラズマローゲンにも着目され、研究されているとお聞きします。
藤木 はい。プラズマローゲンはリン脂質ですが、一般的なリン脂質と異なり、グリセロール骨格のsn-1位に長鎖アルコールがビニルエーテル結合を介して結合しています。プラズマローゲンが合成される7段階の反応うち、初期2段階をペルオキシソームが担っています。
ペルオキシソーム欠損症の話を致しましたが、それら症候群だけでなく、プラズマローゲンだけができないような遺伝子も5種類あり、関節点状石灰化や重度精神運動発達遅滞などを発症します(RCDPと称されます)。
また、報告ではアルツハイマー病の患者の方々ではプラズマローゲンの量がとても減りますし、健常者でも加齢とともに量は減ります。このことから、プラズマローゲンをアルツハイマー病などの認知症の患者の方への治療につなげられないかとか、アンチエイジングに利用できるのではないかと話題になっているのだと思います。
私たちは、チャイニーズ・ハムスター卵巣(CHO)細胞の変異細胞やペルオキシソーム欠損症患者由来細胞などを用いて研究しており、重要なこととしてプラズマローゲン生合成の律速段階は、アシルコエンザイムエー(Acyl-CoA)から還元酵素(FAR1)により長鎖アルコールがつくられペルオキシソームに提供されるということを見出しました。そして、プラズマローゲンは合成後、細胞膜の内側(内葉)に局在化されます。そこでのプラズマローゲン量を細胞が感知することで、FAR1タンパク質の発現量を調整しており、これによりプラズマローゲンの恒常性を保っているということもわかってきました。
審良 今後のご研究の進捗が楽しみです。ほかにも研究課題にされていることはありますか。
藤木 ペルオキシソームの分裂・増殖機構も研究しています。一つは、高度不飽和脂肪酸の一種であるドコサヘキサエン酸(DHA)が、ペルオキシソームの分裂因子の一つであるPex11の多量体形成を促して、ペルオキシソーム膜上にPex11に富んだ膜領域を形成させることで、ペルオキシソームの伸長化や分裂を制御していることを示せました。
また、日本女子大学の黒岩常祥先生の研究室などと共に、ペルオキシソームやミトコンドリアの分裂に重要な分子装置の構成因子として、DYNAMO1というタンパク質を紅藻を用いて新たに同定しています。DYNAMO1はアデノシン三リン酸(ATP)をグアノシン三リン酸(GTP)に変換して、これを分裂させるためのエネルギーとして使っているのです。また、その哺乳類版といえるのが、ヌクレオシド二リン酸キナーゼ3(NME3)です。
審良 ペルオキシソームを研究対象の中心に、その形成や構築、また関連する疾患のメカニズムを網羅的に解明されてきたことがわかりました。
好奇心に基づく基礎科学を受容する社会であってほしい
審良 最後に、藤木先生が、日本のいまのライフサイエンス研究の状況に、どのような思いをもっておられるかお聞きします。ノーベル賞受賞者が日本から輩出されなくなると、危惧を抱いておられるそうですね。
藤木 私自身が研究生活で大切にしてきたことは、「知的好奇心あるいは興味や疑問に基づいて研究すること」です。現状では興味・関心から研究を始める若い研究者が減っているといわれ、「この研究をやってなんの役に立つのですか」と質問する学生も多いようです。たしかに目的思考の研究も大切ですが、自分自身の純粋な好奇心・興味に基づく研究をしたいという若い研究者が減っているとされる点は気がかりです。
研究者の好奇心に基づく純粋な基礎科学が軽視されがちな傾向は、すでに表れています。2022年のデータでは、日本の大学や企業の研究開発費は米国、中国に次いで3位ですが、論文数はこの20年で世界2位から5位に落ちました。引用率トップ10%に入る重要論文数は、G7の中で最下位、世界12位です。日本の各種科学研究システムは、どうも目的・応用性の高いものに資金をたくさん注ぎ込む傾向にあるように感じます。
役に立つことがわかっているということは「わかっていること」の応用に過ぎません。純粋な好奇心に基づく探究なしに、人類の知の地平線を広げることはできません。好奇心に基づく純粋な基礎科学を社会が容認し、応援する文化をもつことが重要と思います。
審良 若い研究者たちにどのようなメッセージを送られますか。
藤木 研究の世界ではチャンスが平等にあり、そして夢があります。自分の興味・関心に基づいて研究してほしいと思います。
審良 今日は数多くのお話をいただき、ありがとうございました。
(対談日/2025年3月5日)
EYES
細胞内の小器官ペルオキシソームの形成・構築と
欠損疾患のメカニズムを解明
新たな生理作用調節機構の確立で
「パラダイムシフト」起こす
細胞の中には、一定の働きをもつ機能的・構造的に分化した器官がいくつも存在しています。これらを総称して、オルガネラ、あるいは細胞小器官といいます。
オルガネラはDNAをもつことで自己増殖するものと、DNAをもたないものに大別されます。前者には、核、ミトコンドリアを挙げることができます。後者には、小胞体、微小管、リソソーム、ゴルジ体、そして今回とくに着目するペルオキシソームなどを挙げることができます。
ペルオキシソームは、動物、植物、酵母、真菌類といった真核生物の細胞にあるオルガネラで、直径は0.5~1.5㎛ほど。楕円形または球形をしています。1954年、スウェーデンのカロリンスカ研究所に所属していた大学院生のヨハネス・ローディンにより、マウスの腎尿細管の上皮細胞に未知の小顆粒があるとして発見されました。この発見で、形状的に「マイクロボディ」の呼称がつきました。
一方、ペルオキシソームが生化学的に発見されたのは、ベルギー出身で米国などで研究をおこなったクリスティアン・ド・デューブによってです。別のオルガネラであるリソソームの発見後、ド・デューブにより“不要物”的なものとして見出されたものがペルオキシソームだったのです。「ペルオキシソーム」という呼称は1965年、ド・デューブにより命名されました。このオルガネラが含んでいる酸化還元酵素「ペルオキシダーゼ」と、「袋」を指す接尾辞「ソーム」が由来となっています。
1979年、米国ロックフェラー大学のド・デューブの研究室に、30歳代前半の日本の研究者が所属しました。本対談に登場する藤木幸夫氏です。その後のペルオキシソームの全容解明は、藤木氏によりなされたといっても過言ではありません。
藤木氏はまずド・デューブの指導のもと、ペルオキシソームの形成機構として当時提唱されていた「小胞体発芽説」の検証を行い、独自に開発した炭酸ナトリウム法という膜単離法を用いてペルオキシソーム膜と小胞体膜のタンパク質組成は全く異なること、ペルオキシソームの構成タンパク質が遊離型ポリソーム上で生合成されることなどを、解明しました。以降も研究をつづけ、ペルオキシソームの形成機構をめぐる「生合成・翻訳後輸送・成長と分裂モデル」を提唱するに至ります。
その後、藤木氏はペルオキシソームの形成に関与する必須因子「ペルオキシン」を発見し、現在ペルオキシン遺伝子としてわかっている14種類の遺伝子の多くを発見するに至りました。この成果の過程には、ペルオキシソームの形成・構築だけでなく、欠損などの異常でもたらされる「ペルオキシソーム欠損症」あるいは報告者の名をとった「ツェルベーガー症候群」のメカニズム解明の成果が多分に含まれます。さらに藤木氏は、ペルオキシソームの膜形成や分裂・増殖などのメカニズムの解明も進めました。
ペルオキシソームに含まれる酵素には、酸素分子を使って物質代謝を行う酸化酵素(オキシダーゼ)群のほか、その過程で生成する毒性の高い過酸化水素を酸素と水とに分解する酵素「カタラーゼ」があります。藤木氏はペルオキシソームの酵素カタラーゼに着目し、その局在化、つまり移動して特定の場所に多くとどまることが、細胞の恒常性を保つうえで重要な役割を果たしていることを明らかにします。つまり、ペルオキシソーム内に存在するカタラーゼが、ペルオキシソームの膜透過装置を構成するPex14のリン酸化を介して輸送・取り込みの制御を受けること、また、細胞死促進因子として知られていたBAKの介在によってペルオキシソーム外の細胞質ゾルへと放出されることを見出したのです。そして、これらの結果、カタラーゼが細胞質ゾルでの局在性を増大させ、酸化ストレス対処戦略や細胞生存機構を発揮するという生理機構を発見しました。これら一連の成果は、カタラーゼがオルガネラの内部と外部の両方に局在化することを基軸とした生理作用調節のしくみを見出したことを意味し、「カタラーゼ研究のパラダイムシフト」が起きたと評されています。
藤木氏は、その後も一貫して、ペルオキシソームに関連する研究を積み重ねてきました。本対談記事では最近(対談日/2025年3月5日当時)の話題を含む数々の研究成果が語られています。